Clear Sky Science · it
Il tessuto adiposo peritumorale guida l’evasione immunitaria nel cancro colorettale tramite la trasformazione adiposa–mesenchimale
Perché il grasso addominale attorno ai tumori è importante
Il cancro colorettale cresce all’interno della parete intestinale, ma si trova immediatamente accanto a un consistente cuscinetto di grasso addominale. La maggior parte delle persone considera questo tessuto adiposo come un semplice ammortizzatore passivo. Questo studio rivela qualcosa di sorprendente: il grasso avvolto attorno al tumore può silenziosamente sottrarre cellule immunitarie che combattono il cancro, aiutando il tumore a nascondersi dal sistema immunitario. Comprendere questa lotta nascosta suggerisce nuovi modi per prevedere chi risponderà all’immunoterapia e come rendere questi trattamenti più efficaci.
Un quartiere immunitario vivace accanto al tumore
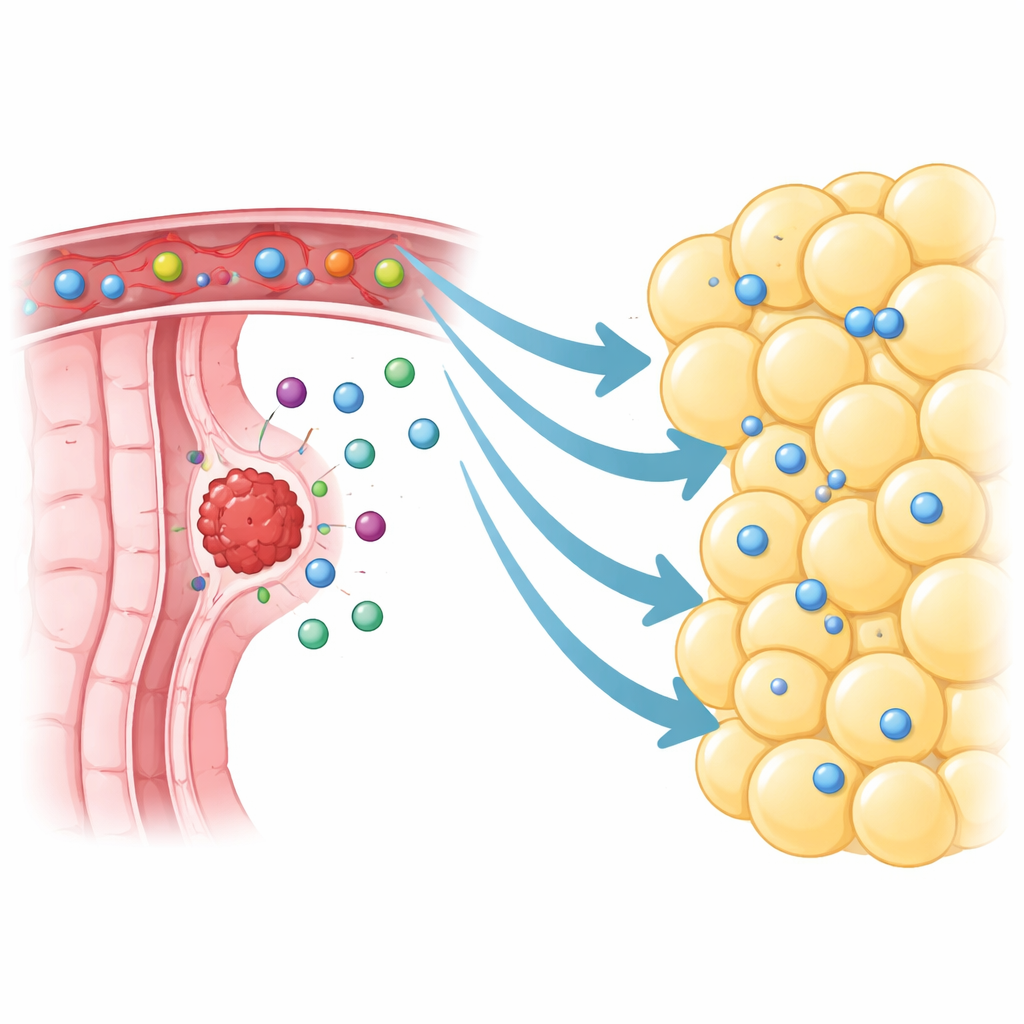
I ricercatori si sono concentrati sul grasso viscerale che circonda direttamente i tumori colorettali, chiamato tessuto adiposo viscerale peritumorale. Utilizzando il sequenziamento dell’RNA a singola cellula, hanno mappato oltre 370.000 singole cellule provenienti da tumori, grasso vicino, grasso distante e tessuto normale. Anziché essere silenzioso e inerte, il grasso vicino ai tumori era brulicante di cellule immunitarie, in particolare cellule T e cellule B. Hanno persino trovato agglomerati organizzati che somigliavano a mini linfonodi, un segno che questo tessuto può ospitare reazioni immunitarie attive. Rispetto al grasso prelevato più lontano, il tessuto peritumorale conteneva molte più cellule linfocitarie, incluse cellule T della memoria e cellule T citotossiche specifiche per il tumore che, in linea di principio, dovrebbero pattugliare alla ricerca del cancro.
Quando le cellule immunitarie utili finiscono nel posto sbagliato
Per capire se questo grasso ricco di cellule immunitarie aiutasse o danneggiasse, il team ha utilizzato modelli murini in cui i tumori venivano impiantati vicino a una papilla adiposa che riproduceva la situazione umana. Hanno poi rimosso chirurgicamente questo grasso vicino o lo hanno dissolto chimicamente. Controintuitivamente, asportare il tessuto peritumorale rallentò la crescita tumorale. I tumori nei topi a cui era stato tolto quel grasso contenevano più cellule T CD4 e CD8, incluse cellule T che riconoscevano antigeni tumorali. Esperimenti aggiuntivi che tracciavano cellule immunitarie donatrici mostrarono che, quando il grasso era presente, molte di queste cellule si accumulavano nella papilla adiposa invece che nel tumore. Rimuovere il grasso ha reindirizzato le cellule verso il tumore, rafforzando la risposta anticancro. In altre parole, il grasso fungeva da serbatoio competitivo che assorbiva le cellule immunitarie e impediva loro di raggiungere il vero bersaglio.
Un richiamo chimico creato dalle cellule adipose trasformate
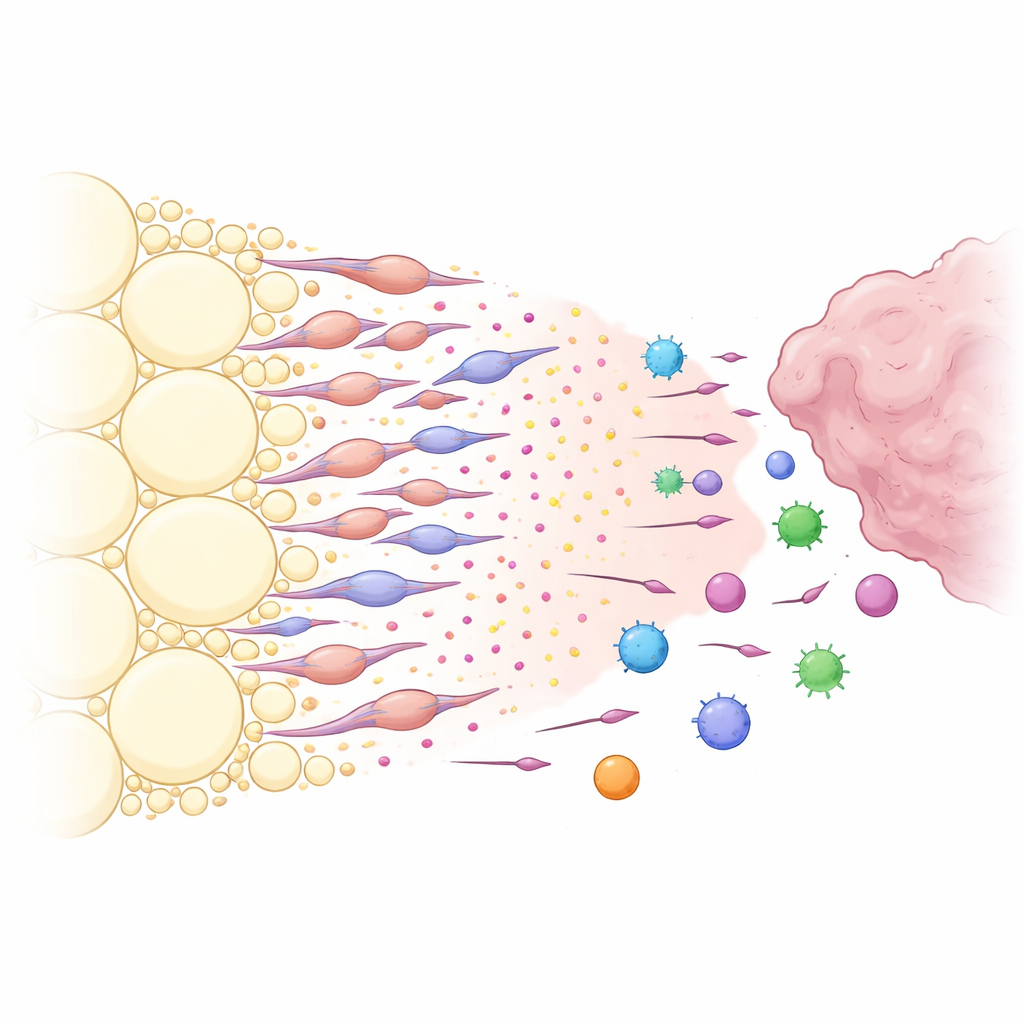
Cosa rendeva il tessuto peritumorale così bravo a catturare le cellule immunitarie? Analizzando i segnali di comunicazione tra i tipi cellulari, i ricercatori hanno identificato una potente via chimica centrata sulla molecola CXCL12 e sul suo recettore CXCR4. Le cellule stromali nel grasso vicino al tumore producevano elevati livelli di CXCL12, mentre molte cellule immunitarie esprimevano CXCR4, rendendole sensibili a questo segnale. Bloccare localmente CXCL12 nel grasso, o eliminarlo geneticamente nello stroma adiposo, portò alla riduzione dei tumori e permise a più cellule immunitarie CXCR4-positive di entrare nel tumore anziché essere deviate. Il team scoprì poi che i principali produttori di CXCL12 non erano adipociti ordinari, ma un gruppo speciale di cellule fibroblasto-simili derivate dal tessuto adiposo che hanno definito fibroblasti associati al cancro di derivazione adiposa. I fattori rilasciati dal tumore, in particolare il fattore di crescita TGF-β1, spinsero le cellule stromali adipose locali a trasformarsi in queste cellule fibroblasto-simili, le quali a loro volta secrete grandi quantità di CXCL12 e altri segnali che favoriscono la crescita.
Trasformare uno scudo in un punto debole
Poiché queste cellule trasformate aiutano a convogliare le cellule immunitarie lontano dai tumori, i ricercatori hanno testato se smantellare questo “pozzo immunitario” potesse migliorare l’immunoterapia. In topi ingegnerizzati in modo che i fibroblasti associati al cancro di derivazione adiposa potessero essere eliminati selettivamente, il trattamento con un anticorpo inibitore di PD-1 divenne molto più efficace: i tumori crebbero meno e più cellule T specifiche per il tumore e positive per CXCR4 infiltravano il cancro. Analogamente, farmaci o anticorpi che bloccavano sia CXCL12 sia il suo recettore CXCR4 agirono in sinergia con il blocco di PD-1 in modelli di cancro colorettale sia sottocutanei sia ortotopici. Queste combinazioni non solo ridussero le dimensioni tumorali ma rimodellarono anche il panorama immunitario all’interno del tumore.
Indizi dalle scansioni dei pazienti e prossimi passi
Il team si è poi chiesto se le loro scoperte avessero rilevanza clinica. In un gruppo di pazienti con cancro colorettale localmente avanzato trattati con chemioterapia combinata, radioterapia e immunoterapia anti–PD-1, coloro che avevano una risposta completa tendevano ad avere un volume minore di grasso viscerale peritumorale alla risonanza magnetica prima del trattamento. In termini quantitativi, l’area di questo grasso prediceva la risposta alla terapia meglio di alcuni marcatori tissutali standard, e i pazienti con grandi volumi di grasso peritumorale avevano tassi di risposta molto più bassi. Per un non specialista, la conclusione è sorprendente: non solo il tumore in sé, ma anche il grasso che lo circonda immediatamente, può determinare quanto bene funziona l’immunoterapia. Focalizzandosi su questo tessuto adiposo—misurandolo per indirizzare le decisioni terapeutiche o mirando alle sue cellule stromali trasformate e al segnale CXCL12–CXCR4—potrebbe essere possibile trasformare uno scudo protettivo del tumore in un punto debole terapeutico.
Citazione: Wang, JH., Zheng, YQ., Qian, ZY. et al. Peritumoural adipose tissue drives immune evasion in colorectal cancer via adipose–mesenchymal transformation. Nat Cell Biol 28, 581–595 (2026). https://doi.org/10.1038/s41556-026-01885-0
Parole chiave: cancro colorettale, microambiente tumorale, grasso viscerale, immunoterapia, CXCL12 CXCR4