Clear Sky Science · it
Il rimodellamento del RE è una caratteristica dell’invecchiamento e dipende dalla ER-fagia
Perché contano le pieghe interne della cellula con l’avanzare dell’età
Le cellule del nostro corpo sono attraversate da un sistema membranoso labirintico chiamato reticolo endoplasmatico, o RE. Questa struttura aiuta a sintetizzare lipidi e proteine, gestisce zuccheri e calcio e comunica costantemente con le altre parti della cellula. Poiché così molte funzioni vitali passano attraverso questa rete, qualsiasi ristrutturazione a lungo termine del RE potrebbe influenzare il modo in cui i tessuti invecchiano, la loro resilienza allo stress e, in ultima analisi, la durata del mantenimento della salute. Questo studio pone una domanda apparentemente semplice: il RE invecchia in modo specifico e organizzato, e se sì, questo cambiamento è un danno accumulato o una strategia protettiva incorporata?
Un cambiamento nascosto nel banco di lavoro cellulare
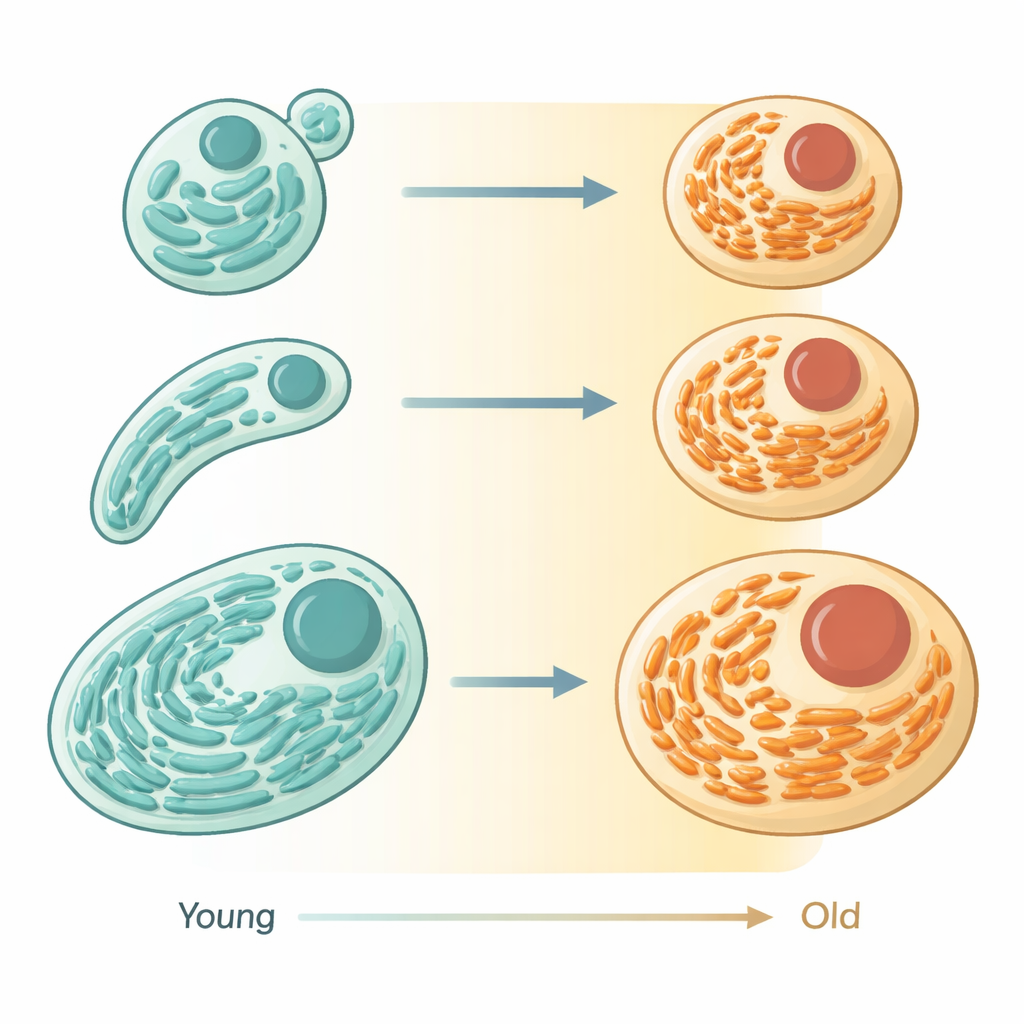
Usando microscopi avanzati e sonde fluorescenti nel piccolo verme Caenorhabditis elegans, gli autori hanno seguito il RE all’interno di animali viventi mentre passavano dalla giovane età adulta alla vecchiaia. Nelle cellule giovani, il RE forma ampie lamelle impilate punteggiate da macchinari per la sintesi proteica, che ricordano pavimenti di fabbrica ordinati. Con l’età, quelle lamelle si riducono in volume e lasciano il posto a una maglia più sottile e tubulare che occupa meno spazio. Le misure hanno mostrato che il contenuto complessivo di RE diminuisce notevolmente mentre la sua forma cambia, indicando non solo danno casuale ma un ridimensionamento e una riconfigurazione coordinati dell’organulo.
Dal fare proteine al gestire i grassi
La forma in biologia spesso segnala funzione, e qui ciò si è dimostrato vero. I ricercatori hanno confrontato come le proteine correlate al RE cambiano nel tempo nei diversi tessuti del verme. Le proteine coinvolte nella costruzione, nel ripiegamento e nel controllo di altre proteine declinano con l’età, in parallelo con la perdita del RE a lamelle. Al contrario, molte proteine del RE legate al metabolismo dei lipidi e delle membrane rimangono costanti o addirittura aumentano. Nel complesso, questi schemi suggeriscono che le cellule invecchianti riducono la produzione proteica di massa e riallocano le risorse del RE verso la gestione di lipidi e membrane. Colpisce che, esaminando grandi dataset di topi invecchiati, gli autori hanno osservato una storia simile: le proteine del RE per la secrezione e l’elaborazione delle proteine tendevano a diminuire, mentre quelle coinvolte nel metabolismo lipidico e nell’autofagia erano relativamente preservate o aumentate.
Una via di riciclo cellulare dietro il rimodellamento
Cosa guida questo rimodellamento su larga scala? Il team ha ricondotto i cambiamenti all’ER-fagia, una forma di auto-digestione selettiva nella quale la cellula incapsula porzioni di RE in vescicole di riciclo per la degradazione nei lisosomi. Bloccando geni fondamentali per l’autofagia nei vermi si è impedita la normale perdita di massa del RE correlata all’età e lo spostamento da lamelle a tubuli, dimostrando che questa via di riciclo non si limita a ripulire detriti ma scolpisce attivamente l’organulo. Esperimenti indipendenti nel lievito hanno confermato che i componenti del RE vengono reindirizzati al centro di riciclo cellulare con l’età, di nuovo in modo dipendente dall’autofagia. La microscopia elettronica ha rivelato frammenti di RE all’interno di compartimenti degradativi, fornendo evidenza fisica che porzioni della rete vengono rimosse intenzionalmente.

Controllo specifico per tessuto di un programma d’invecchiamento comune
Benché il rimodellamento del RE sia stato osservato in molti tessuti del verme—intestino, ipoderma simile alla pelle, muscolo e neuroni—i trigger si sono rivelati specifici per tessuto. Nell’ipoderma, una proteina di membrana precedentemente poco nota chiamata TMEM-131 ha collegato il turnover del RE alla gestione del collagene. Quando TMEM-131 è stata ridotta, la perdita di RE correlata all’età in questo tessuto è stata in gran parte prevenuta, implicando che il RE si ridimensiona quando i suoi “clienti” di collagene diminuiscono. Nell’intestino, invece, il regolatore chiave è stato il braccio IRE-1–XBP-1 della risposta a proteine non ripiegate, una via centrale di rilevamento dello stress. Silenziare questo ramo di segnalazione ha preservato il RE intestinale durante l’invecchiamento, suggerendo che, in questo organo, la segnalazione di stress del RE contribuisce a decidere quando parti del RE debbano essere sacrificate.
Riprogrammare il RE per una vita più lunga
Lo studio collega inoltre il rimodellamento del RE alla longevità. Nei vermi, diverse note interventi che allungano la vita—attenuare i segnali simili all’insulina, ridurre il sensing nutrizionale mTOR, rimuovere le cellule germinali o rallentare leggermente la sintesi proteica—hanno tutti indotto un ridimensionamento del RE e un aumento delle reti tubolari presto nell’età adulta, anziché aspettare la vecchiaia. Importante, quando l’ER-fagia è stata disattivata, le vite prolungate normalmente prodotte dall’inibizione di mTOR sia nel lievito sia nei vermi sono state drasticamente ridotte o perse. Ciò indica che un potatura accuratamente gestita del RE non è solo un effetto collaterale dell’invecchiamento o del trattamento, ma uno dei meccanismi attraverso cui le cellule raggiungono uno stato più durevole.
Cosa significa per un invecchiamento sano
Per un osservatore non esperto, perdere una frazione sostanziale di una struttura cellulare chiave durante l’invecchiamento potrebbe suonare come un danno puro. Il lavoro qui dipinge un quadro più sfumato. Il RE sembra essere attivamente rimodellato—tramite auto-digestione selettiva e regolatori specifici per tessuto—in modo che le cellule invecchianti producano meno proteine nuove, investano di più nella gestione di lipidi e membrane e possibilmente riducano il rischio di stress cronico. Questo rimodellamento appare conservato dal lievito ai mammiferi ed è richiesto per almeno alcune forme di estensione della vita. Sul lungo periodo, tuttavia, il ridimensionamento del RE può comportare compromessi, influenzando quanto bene le cellule riparano altri organelli e gestiscono il declino tardivo. Rivelando l’ER-fagia e la dinamica del RE come caratteristiche centrali dell’invecchiamento normale e ritardato, questa ricerca mette in luce una nuova serie di leve che un giorno potrebbero essere modulati per promuovere tessuti più sani e resistenti.
Citazione: Donahue, E.K.F., Hepowit, N.L., Ruark, E.M. et al. ER remodelling is a feature of ageing and depends on ER-phagy. Nat Cell Biol 28, 449–464 (2026). https://doi.org/10.1038/s41556-025-01860-1
Parole chiave: reticolo endoplasmatico, autofagia, invecchiamento cellulare, omeostasi delle proteine, metabolismo dei lipidi