Clear Sky Science · it
Genomica funzionale risolta nel tempo mediante deep learning rivela un controllo gerarchico globale dell’autofagia
Come le cellule si riciclano — e come sanno quando fermarsi
Le nostre cellule sopravvivono ai periodi di scarsità riciclando parti di sé attraverso un processo chiamato autofagia — letteralmente “mangiare se stessi”. Un riciclo insufficiente porta all’accumulo di componenti danneggiati; un riciclo eccessivo porta l’elemento cellulare ad auto‑cannibalizzarsi. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni per l’invecchiamento e le malattie: come fa una cellula vivente ad attivare e disattivare l’autofagia nei momenti giusti, mentre i nutrienti aumentano e diminuiscono?
Seguire migliaia di cellule attraverso un ciclo da festa a carestia
Per affrontare la questione, i ricercatori hanno usato il lievito di birra come modello e hanno osservato quasi seimila diversi ceppi mutanti mentre attraversavano fame e recupero. Ciascun ceppo di lievito portava marcatori fluorescenti che evidenziavano strutture coinvolte nell’autofagia, permettendo a un microscopio ad alta risoluzione di catturare immagini ogni ora mentre i nutrienti venivano rimossi e poi ripristinati. Invece di classificare manualmente queste immagini, il gruppo ha addestrato algoritmi di deep learning a riconoscere quando una cellula si trovava in uno stato autofagico, basandosi interamente su caratteristiche dell’immagine piuttosto che sul giudizio umano. Questo ha prodotto curve temporali precise dell’attività autofagica per quasi l’intero genoma del lievito, rivelando quanto rapidamente e quanto intensamente ogni mutante rispondeva ai cambiamenti dei nutrienti. 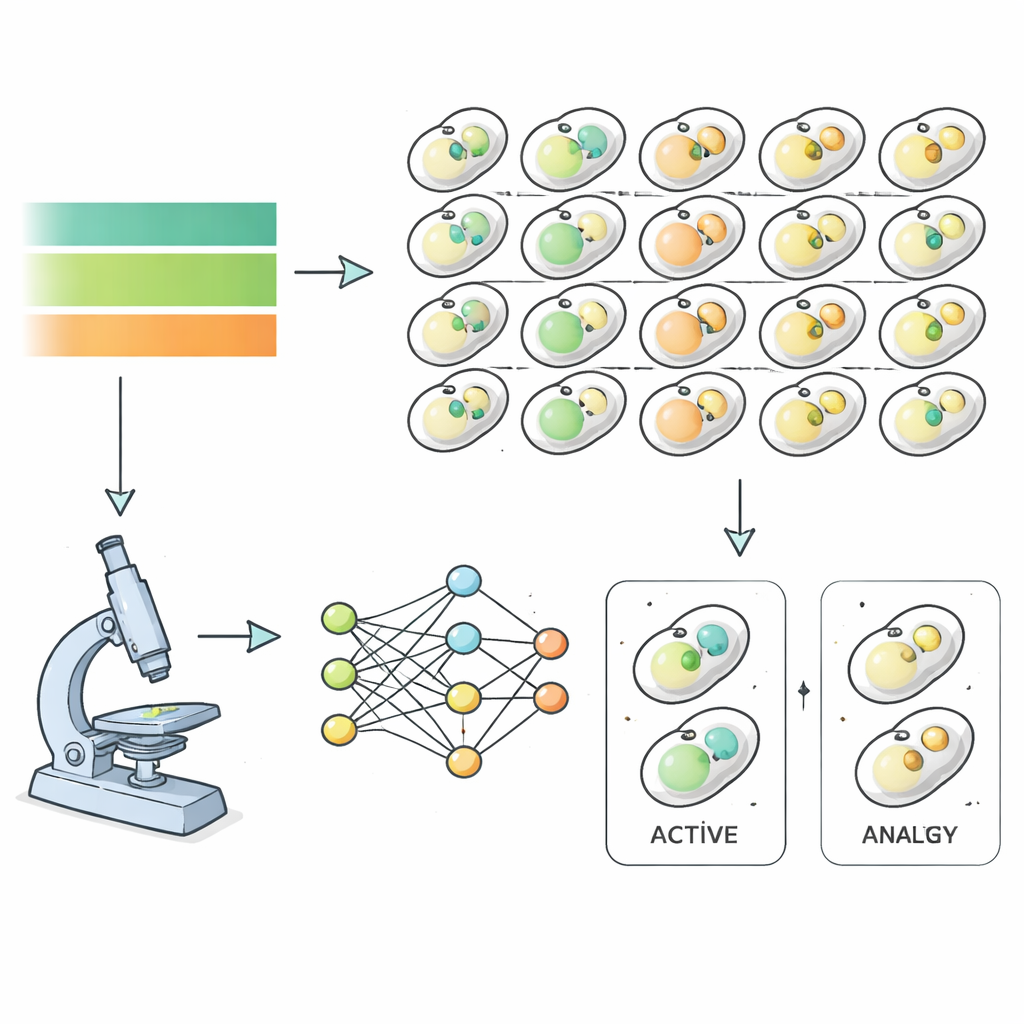
Sei modi distinti in cui le cellule gestiscono male il riciclo
Adattando matematicamente queste curve temporali, gli autori hanno estratto dettagliate “impronte cinetiche” per ogni mutante — quanto velocemente l’autofagia si accendeva, quanto a lungo restava elevata e con quale rapidità si spegneva. Raggruppando queste firme sono emersi sei tipi comportamentali ampi. Alcuni mutanti erano “ultrasensibili”, rispondendo molto rapidamente sia alla fame sia al ritorno dei nutrienti. Altri erano “iposensibili”, reagendo con lentezza. Un gruppo “iperattivo” presentava un riciclo basale anormalmente elevato, mentre diversi gruppi mostravano vari gradi di incapacità a montare una risposta adeguata. Importante, geni noti del nucleo dell’autofagia ricadevano nelle classi più gravi, convalidando che il metodo cattura biologia reale piuttosto che rumore di misura.
Mappare una gerarchia di controllo sull’autofagia
L’autofagia non avviene in isolamento; è collegata alle reti regolatorie più ampie della cellula. Il team ha sovrapposto i loro profili dinamici su ampie mappe di interazioni genetiche e proteiche nel lievito. I geni la cui perdita causava forti difetti autofagici tendevano a trovarsi vicini al noto “macchinario centrale” dell’autofagia in queste reti, mentre i mutanti più sottili erano più distanti, coerente con un controllo più indiretto. Esaminando quali processi cellulari erano arricchiti in ciascuna classe di comportamento, hanno scoperto che l’attivazione scatenata dalla fame è fortemente modellata da vie che gestiscono RNA, sintesi proteica e metabolismo energetico, mentre lo spegnimento dell’autofagia dopo il ritorno dei nutrienti dipende maggiormente dal traffico e fusione di membrane che liberano le vescicole di riciclo.
Avvicinandosi a come si formano e si eliminano le vescicole
L’autofagia procede attraverso due fasi principali: costruire vescicole cariche di materiale e poi fonderle con il compartimento di riciclo della cellula per la degradazione. Per dissezionare queste fasi, i ricercatori hanno esplorato lo “spazio latente” all’interno della loro rete neurale — la rappresentazione compressa che usa per distinguere le immagini. Proiettando questa rappresentazione interna su una mappa bidimensionale, hanno potuto vedere le popolazioni cellulari muoversi da una regione senza vescicole, attraverso una con molte vescicole libere, fino a una regione in cui le vescicole erano state eliminate. Usando confronti statistici con mutanti di riferimento bloccati a diversi stadi, hanno quantificato per ogni gene se esso influenzava principalmente la formazione delle vescicole, la loro eliminazione o entrambi. Questa analisi ha mostrato che il controllo della formazione delle vescicole è altamente sensibile ai livelli di azoto nel tempo, mentre il macchinario di eliminazione si comporta in modo più costante ed è spesso il principale fattore limitante del flusso di riciclo complessivo. 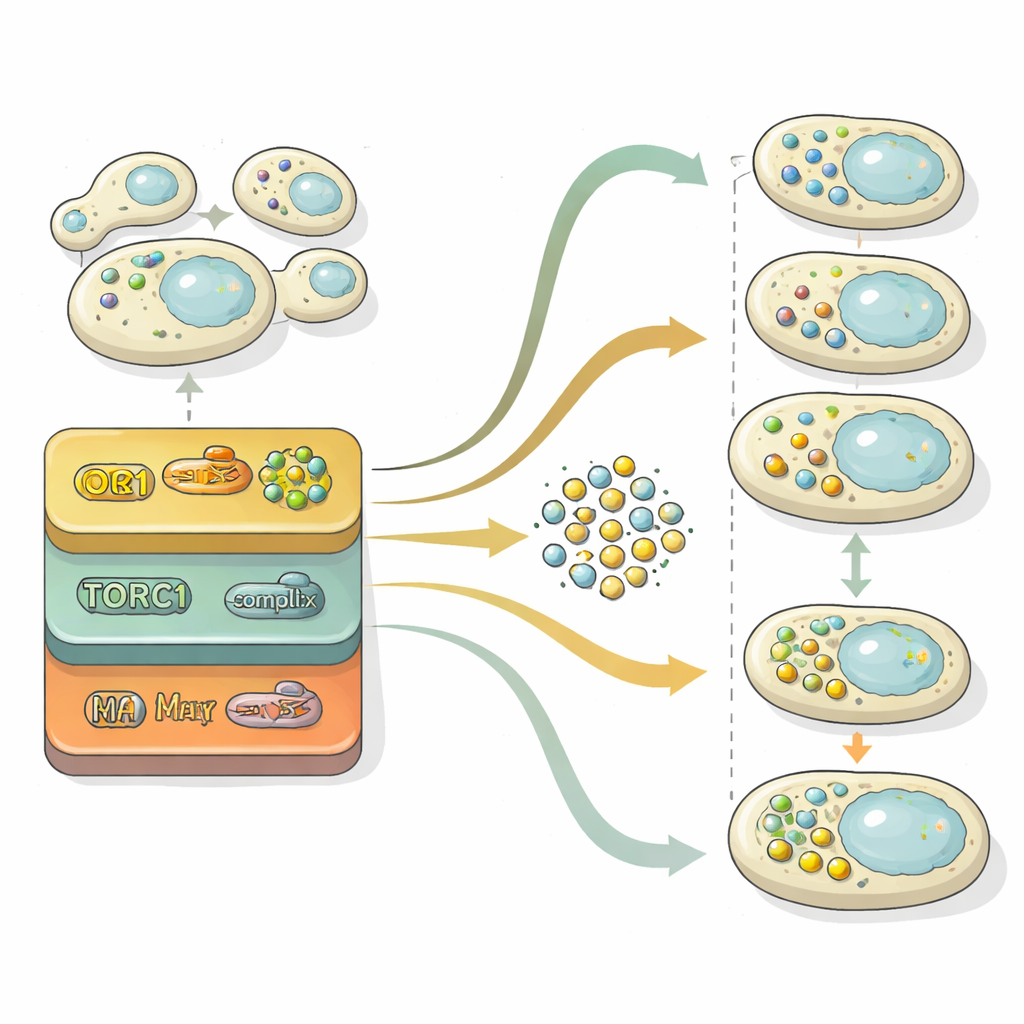
Un freno nascosto sul riciclo: la via retrograda
Una delle scoperte più sorprendenti riguardava la cosiddetta via retrograda (RTG), che trasmette segnali dai mitocondri al nucleo. Le cellule di lievito prive di componenti RTG producevano troppe autofagosomi anche quando i nutrienti erano abbondanti e faticavano a eliminarli una volta tornati i nutrienti. Esperimenti di follow‑up dettagliati hanno mostrato che questa via controlla l’espressione di geni chiave dell’autofagia, in particolare il fattore iniziatore maestro ATG1, in larga parte indipendentemente dal noto sensore dei nutrienti TORC1, bersaglio di farmaci come la rapamicina. In sostanza, il segnale RTG agisce come un freno variabile nel tempo che previene l’autofagia incontrollata in condizioni ricche e aiuta a terminare la risposta quando le condizioni migliorano.
Perché questo è importante per la salute e la terapia
Nel complesso, questo lavoro fornisce una mappa genomica, risolta nel tempo, di come le cellule modulano l’autofagia in condizioni di nutrienti variabili. Rivela che attivazione e spegnimento non sono immagini speculari: molti più geni influenzano l’avvio del riciclo rispetto alla sua interruzione, e l’equilibrio a lungo termine dipende fortemente dall’eliminazione delle vescicole e da freni trascrizionali come la via RTG. Per il lettore generale, il messaggio chiave è che l’auto‑cannibalismo cellulare è sottoposto a un controllo stratificato e gerarchico, e che ora siamo in grado di mappare questi strati con alta precisione. Questa visione a livello di sistema potrebbe un giorno guidare terapie più sfumate che modulano l’autofagia in fasi specifiche — potenziando il riciclo benefico senza innescare gli effetti dannosi di un’autodigestione cronica e incontrollata.
Citazione: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
Parole chiave: autofagia, deep learning, genetica del lievito, rilevamento dei nutrienti, riciclo cellulare