Clear Sky Science · it
Fenotipizzazione raffinata delle risposte vaccinali rivela determinanti trascrittomici dell’eterogeneità degli anticorpi neutralizzanti
Perché alcuni vaccini funzionano meglio per certe persone
Quando ci facciamo la vaccinazione contro il COVID-19, potremmo supporre che il sistema immunitario di tutti reagisca allo stesso modo. In realtà, le persone differiscono molto nella rapidità e nell’intensità con cui sviluppano anticorpi protettivi. Questo studio ha seguito adulti che hanno ricevuto vaccini inattivati contro SARS-CoV-2 e mostra che le risposte vaccinali seguono schemi distinti, ciascuno guidato da segnali immunitari precoci diversi, scritti nei nostri geni e nelle cellule del sangue. Comprendere questi schemi potrebbe un giorno aiutare a personalizzare i calendari vaccinali in modo che tutti ottengano la protezione necessaria.
Tre percorsi verso la protezione dopo la stessa iniezione
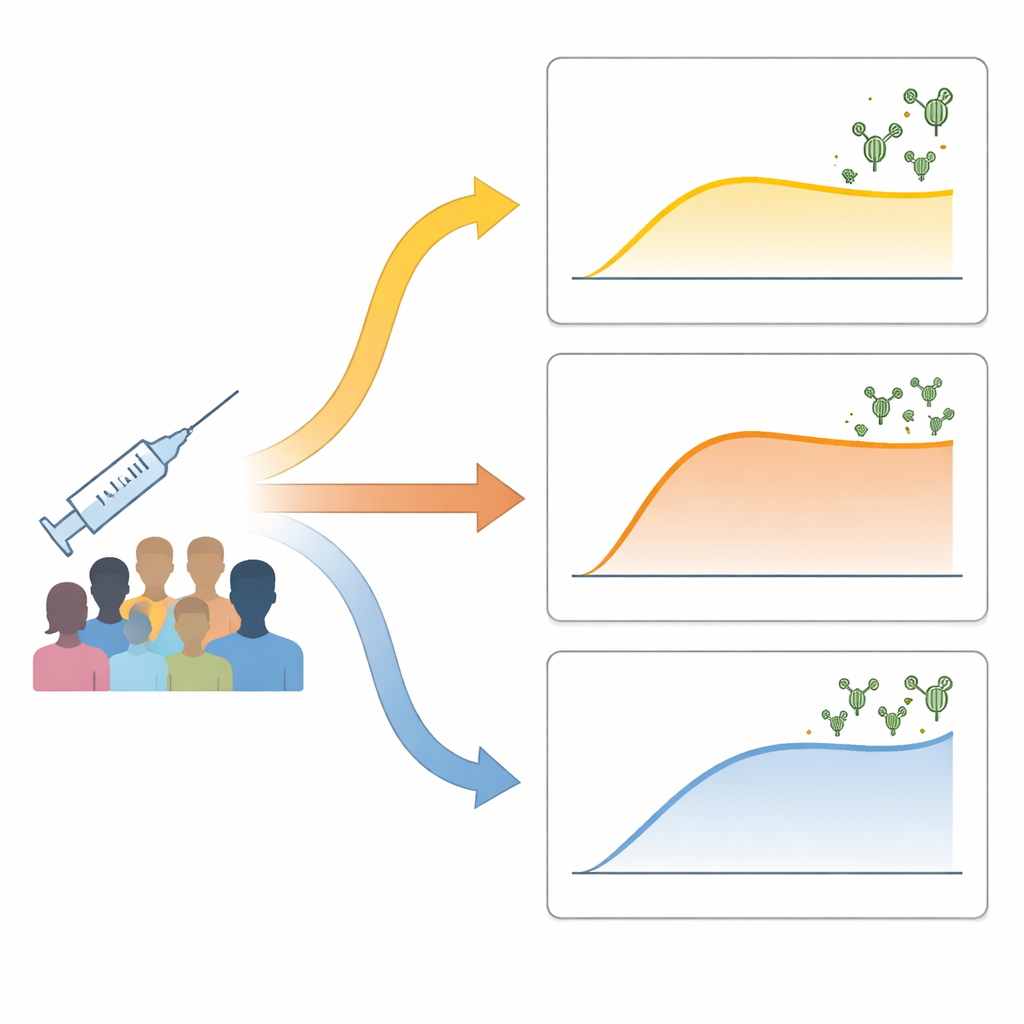
I ricercatori hanno monitorato 73 adulti sani che hanno ricevuto due dosi di un vaccino COVID-19 inattivato. Hanno misurato gli anticorpi neutralizzanti — quelli in grado di bloccare il virus — prima della vaccinazione, una settimana dopo la seconda dose e di nuovo circa un mese dopo. Invece di dividere semplicemente le persone in “rispondenti alti” e “bassi”, hanno usato metodi guidati dai dati per raggruppare le persone in base a come variavano i livelli di anticorpi nel tempo. Sono emersi tre schemi chiari: un gruppo “basso–ritardato” con un aumento lento e modesto degli anticorpi; un gruppo “rapido–stabilizzante” i cui anticorpi sono aumentati rapidamente per poi stabilizzarsi; e un gruppo “aumento continuo” i cui anticorpi sono continuati a salire fino ai livelli più alti. Questi schemi non erano spiegati dall’età, dal sesso o dal peso corporeo e solo in parte dal marchio del vaccino inattivato ricevuto.
Come l’attività immunitaria precoce modella l’esito
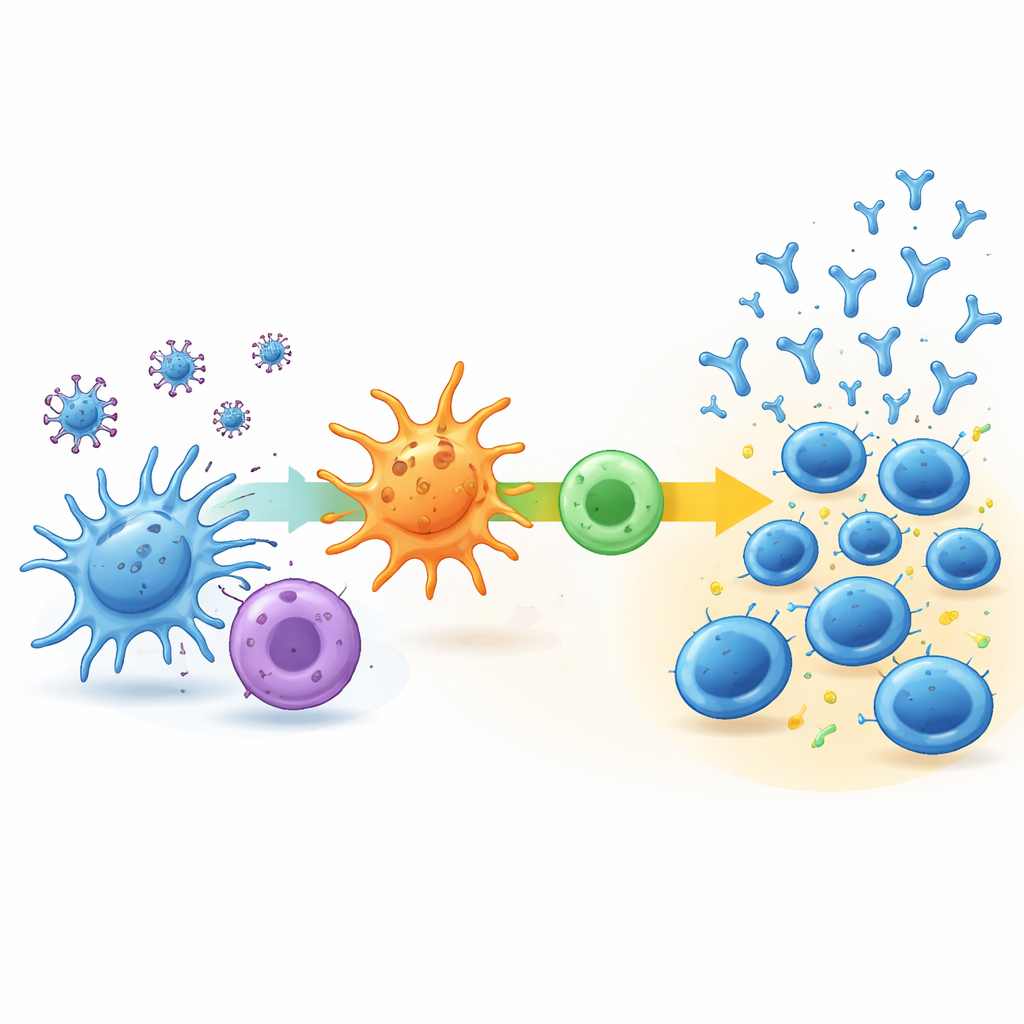
Per capire cosa guida questi percorsi differenti, il team ha analizzato l’attività genetica delle cellule immunitarie nel sangue all’inizio e una settimana dopo la seconda dose. Nel gruppo basso–ritardato, è cambiato molto poco: le principali vie immunitarie si sono attivate a malapena e la composizione dei tipi cellulari immunitari nel sangue è rimasta per lo più invariata. Al contrario, nei gruppi rapido–stabilizzante e aumento continuo si sono osservati chiari segni di attivazione immunitaria precoce. Nei rispondenti più forti c’è stata un’attività coordinata nelle vie che processano frammenti virali, li presentano ad altre cellule immunitarie e supportano un tipo di risposta delle cellule T helper nota per potenziare la produzione di anticorpi. Queste persone tendevano anche ad avere più cellule B naïve e cellule T helper pronte a rispondere e successivamente mostravano un’attività delle cellule T specifica per il virus leggermente più forte.
Strati nascosti di controllo nell’RNA e nelle cellule B
Oltre ai semplici cambiamenti on–off dei geni, gli scienziati hanno esaminato livelli più sottili di regolazione incorporati nell’RNA, le molecole intermedie tra DNA e proteina. Nel gruppo con risposta massima, i geni immunitari coinvolti nella presentazione di frammenti virali al sistema immunitario mostravano diversi schemi di “splicing” e regioni terminali (tail) più corte nei loro RNA. Queste caratteristiche si ritiene facilitino la produzione di certe proteine e il mantenimento di un segnalamento robusto. Il team ha anche ricostruito il repertorio dei recettori delle cellule B — le antenne uniche delle cellule produttrici di anticorpi — dagli stessi campioni di sangue. Pur con una diversità complessiva simile tra i gruppi, ogni schema di risposta utilizzava combinazioni e conformazioni leggermente diverse di questi recettori, e i rispondenti più forti favorivano tipi di recettori precedentemente associati ad anticorpi potenti contro la proteina spike del coronavirus.
Individuare i probabili rispondenti deboli prima della vaccinazione
Poiché le persone del gruppo basso–ritardato potrebbero essere meno protette dopo un programma vaccinale standard, i ricercatori si sono chiesti se fosse possibile identificarle in anticipo. Si sono concentrati su un piccolo insieme di geni che differivano modestamente a baseline tra i rispondenti più deboli e quelli più forti. Utilizzando metodi di apprendimento automatico, hanno costruito un modello basato sull’attività di appena otto geni misurati prima della vaccinazione. Questo modello è stato in grado di distinguere i rispondenti basso–ritardato con alta accuratezza nel loro set di dati, con due geni coinvolti nella segnalazione cellulare di base e nell’infiammazione che fornivano la maggior parte del potere predittivo. Sebbene questo lavoro debba essere testato in gruppi più ampi e diversificati, suggerisce che un semplice esame del sangue potrebbe un giorno guidare piani vaccinali più personalizzati.
Cosa significa per i vaccini futuri
Complessivamente, questo studio mostra che le persone non si limitano a montare risposte anticorpali “forti” o “deboli”; seguono corsi temporali diversi plasmati da eventi immunitari precoci e difficili da osservare. Gli individui più protetti attivano reti coordinate di geni e cellule che li aiutano a riconoscere rapidamente il vaccino e costruire anticorpi duraturi, mentre i rispondenti deboli mostrano una reazione precoce attenuata. Mappando queste differenze interne e sviluppando strumenti per prevedere chi risponderà poco, il lavoro pone le basi per la vaccinazione personalizzata — come richiami anticipati o formulazioni alternative per soggetti a rischio — in modo che i benefici dei vaccini possano essere condivisi in modo più equo.
Citazione: Wu, Q., Hu, H., Qin, L. et al. Refined phenotyping of vaccine responses reveals transcriptomic determinants of neutralizing antibody heterogeneity. npj Vaccines 11, 61 (2026). https://doi.org/10.1038/s41541-026-01386-z
Parole chiave: risposte vaccinali, anticorpi neutralizzanti, vaccinazione COVID-19, eterogeneità immunitaria, vaccini personalizzati