Clear Sky Science · it
Immunogenicità e protezione di candidati vaccinali antinfluenzali ottavalenti usando proteine adiuvate o mRNA-LNP in topi naïve
Perché un colpo influenzale migliore è importante
I vaccini stagionali contro l’influenza salvano molte vite, ma la loro efficacia può variare molto di anno in anno. Una ragione è che le formulazioni attuali allenano soprattutto il sistema immunitario a riconoscere una singola proteina virale, lasciando sottoutilizzati altri bersagli utili. Questo studio nei topi esplora vaccini antinfluenzali di nuova generazione che insegnano al sistema immunitario a riconoscere due proteine virali chiave contemporaneamente e confronta un approccio tradizionale a base di proteine con una più recente tecnologia a mRNA simile a quella impiegata nei vaccini COVID‑19 recenti.
Due bersagli invece di uno
Gli attuali vaccini influenzali si concentrano principalmente sull’emagglutinina, o HA, una proteina che aiuta il virus ad attaccarsi alle nostre cellule. I ricercatori hanno aggiunto una seconda proteina virale, la neuraminidasi, o NA, che favorisce l’uscita del virus dalle cellule infette e la diffusione. Combinando quattro varianti di HA e quattro varianti di NA provenienti dai ceppi stagionali 2018–2019, hanno costruito un vaccino “ottavalente” pensato per coprire due tipi di influenza A e due linee dell’influenza B. Hanno poi confezionato questi otto componenti in due modi diversi: come proteine purificate miscelate con un ingrediente che potenzia la risposta immunitaria, e come mRNA avvolto in piccole bolle lipidiche (mRNA‑LNP) che stimolano le cellule dell’organismo a produrre le proteine virali.
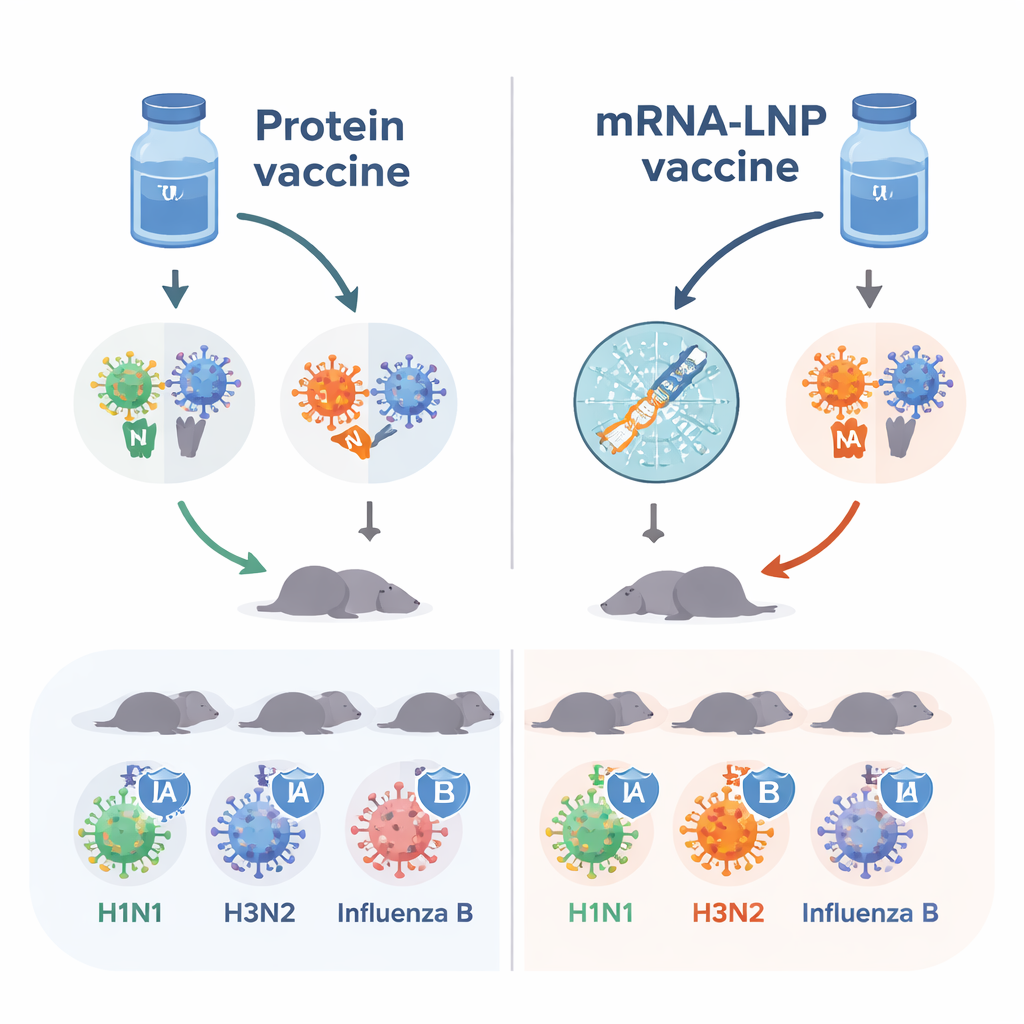
Risposte anticorpali più forti con l’mRNA
Topi naïve — animali che non avevano mai incontrato virus influenzali o vaccini — hanno ricevuto due dosi sia del vaccino a proteine sia della versione mRNA‑LNP. Il team ha misurato gli anticorpi che riconoscono HA e NA nel sangue. Entrambi i vaccini hanno generato risposte utili, ma le somministrazioni mRNA‑LNP hanno prodotto costantemente livelli più elevati di anticorpi contro la maggior parte dei componenti HA e NA. In particolare, gli anticorpi che bloccano l’attività della NA, noti per contribuire in modo indipendente alla protezione, risultavano generalmente più forti dopo la vaccinazione con mRNA‑LNP. Questi risultati suggeriscono che, almeno in questo modello animale, la piattaforma mRNA rende gli stessi bersagli virali più visibili al sistema immunitario.
Protezione contro ceppi corrispondenti e attuali
La prova del nove è stata se questi vaccini potevano salvare i topi da malattie gravi. A dosi scalate per essere simili a quelle di un vaccino umano, entrambi i formati vaccinali hanno protetto completamente gli animali da infezioni letali da virus H1N1 e da virus di influenza B strettamente corrispondenti ai componenti del vaccino, così come da virus di tipo H3N2 ingegnerizzati usati quando i ceppi umani standard non rendono i topi malati. I topi vaccinati hanno mantenuto il peso corporeo e sono sopravvissuti, mentre gli animali non vaccinati hanno perso peso e spesso sono morti. Per questi ceppi strettamente correlati, i vaccini tradizionali a proteine e i vaccini mRNA‑LNP hanno avuto prestazioni simili in termini di sopravvivenza, anche se i dettagli degli anticorpi differivano.
Vantaggio contro virus influenzali più vecchi e discordanti
Dove l’approccio mRNA‑LNP si è distinto è nelle prove più difficili di “mismatch”. I ricercatori hanno sfidato i topi vaccinati con ceppi H3N2 storici del 1968, 1975 e 1982 — virus che differiscono dai ceppi moderni che il vaccino era progettato a imitare. Tutti i topi non vaccinati e la maggior parte degli animali immunizzati con vaccini a proteine sono morti, ma ogni topo che aveva ricevuto il vaccino ottavalente mRNA‑LNP è sopravvissuto, anche se ha mostrato segni di malattia. Questo vantaggio in termini di sopravvivenza è persisito quasi per un anno dopo la vaccinazione, indicando una protezione duratura. Quando il team ha trasferito il siero sanguigno di animali vaccinati in topi non vaccinati, solo il siero contenente anticorpi indotti dagli mRNA‑LNP contro HA ha protetto dalla morte causata da un virus non corrispondente, suggerendo che gli anticorpi cross‑reattivi contro HA siano un fattore chiave.
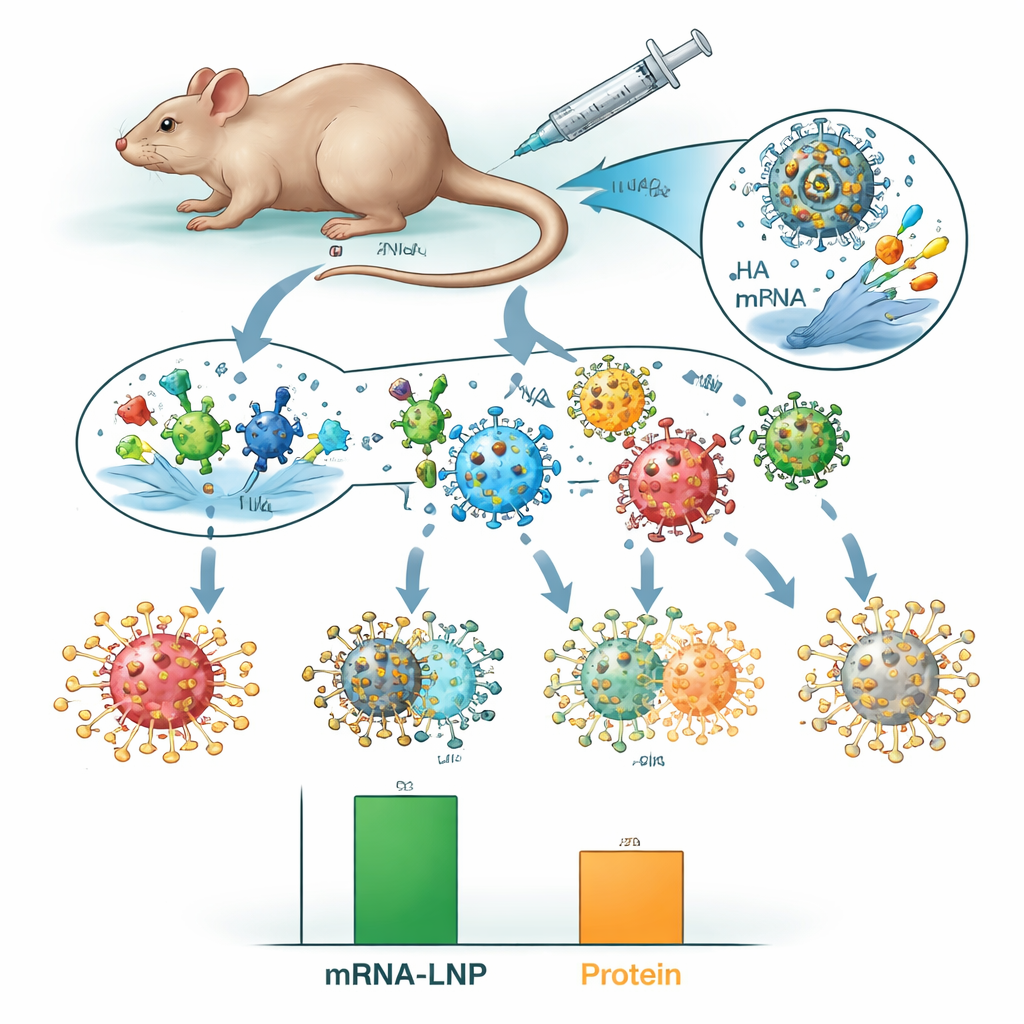
Cosa significa per i futuri vaccini antinfluenzali
Per un lettore non specialista, il messaggio è che entrambi gli stili vaccinali hanno protetto i topi dai tipi di ceppi influenzali per cui erano stati progettati, ma la versione mRNA‑LNP ha offerto anche una protezione più ampia e duratura contro virus più vecchi e obsoleti. Includendo entrambe le principali proteine di superficie dell’influenza e usando mRNA per presentarle al sistema immunitario, questa strategia potrebbe contribuire a ridurre la variabilità tra stagioni influenzali buone e cattive. Sebbene i risultati nei topi non garantiscano il successo nell’uomo, e adiuvanti più efficaci possano ancora migliorare i vaccini a proteine, il lavoro supporta l’idea che vaccini antinfluenzali multicomponenti a mRNA potrebbero un giorno fornire una protezione più affidabile su un più ampio spettro di ceppi influenzali circolanti ed emergenti.
Citazione: Catani, J.P.P., Smet, A., Ysenbaert, T. et al. Immunogenicity and protection of octavalent influenza vaccine candidates using adjuvanted proteins or mRNA-LNPs in naïve mice. npj Vaccines 11, 57 (2026). https://doi.org/10.1038/s41541-026-01378-z
Parole chiave: vaccino antinfluenzale, mRNA-LNP, emagglutinina, neuraminidasi, protezione crociata