Clear Sky Science · it
Superare la resistenza ai TKI mediata dal nicchia vascolare nella leucemia mieloide acuta tramite inibizione di miR-126
Perché questo è importante per i pazienti oncologici
La leucemia mieloide acuta (LMA) è uno dei tumori ematologici più aggressivi e, nonostante i farmaci mirati moderni, molti pazienti vanno incontro a recidiva. Questo studio pone una domanda apparentemente semplice ma di grande portata: parte del problema riguarda non solo le cellule tumorali, ma anche il “quartiere” in cui vivono nel midollo osseo? Costruendo un modello computazionale dettagliato radicato in dati di laboratorio, gli autori esplorano come i piccoli vasi sanguigni possano proteggere le cellule staminali leucemiche dai farmaci—e come bloccare un singolo piccolo RNA potrebbe smantellare quella protezione.
La base sicura nascosta nel midollo osseo
La LMA origina nel midollo osseo, dove le cellule blastiche maligne soppiantano la normale produzione ematica. All’interno di questo sovraffollamento si nasconde una popolazione più piccola di cellule staminali leucemiche in grado di auto-rinnovarsi e sopravvivere ai trattamenti, seminando la recidiva. Queste cellule staminali non stanno libere al caso; si infilano in nicchie specializzate attorno ad arteriole e capillari, note collettivamente come nicchia vascolare. Lo studio si concentra su pazienti le cui cellule leucemiche portano la mutazione FLT3-ITD, trattata con inibitori delle tirosin-chinasi (TKI). Sebbene questi farmaci possano ridurre drasticamente il carico tumorale, molti pazienti recidivano, suggerendo che alcune cellule siano nascoste o protette.
Un effetto terapeutico a due facce
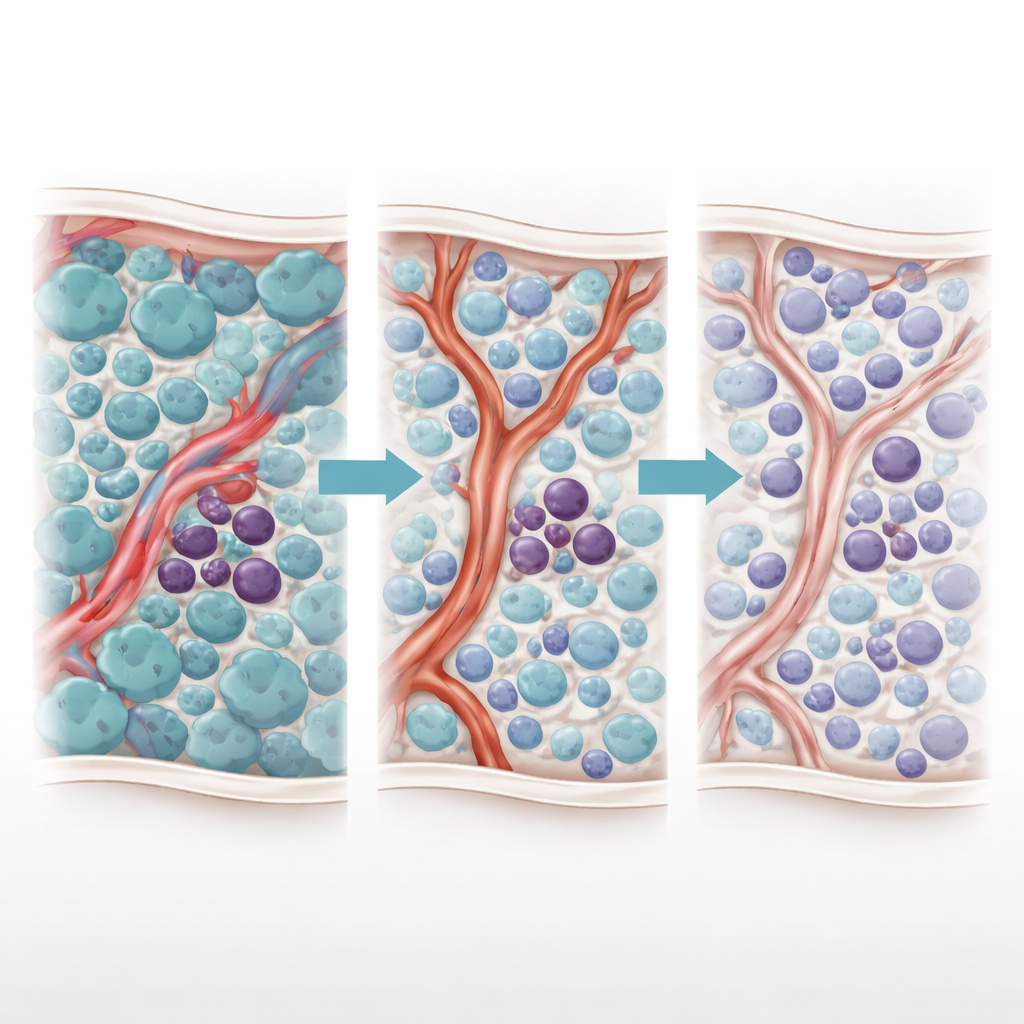
Gli autori avevano precedentemente descritto un curioso “fenomeno di Giano”—una risposta bifronte alla terapia con TKI. Quando i TKI eliminano le blastiche a rapida proliferazione, i livelli di una molecola infiammatoria, il TNF-α, diminuiscono. Questo calo consente inaspettatamente alle cellule endoteliali vascolari vicine di aumentare la produzione di un piccolo RNA regolatorio chiamato miR-126. Quel miR-126 viene trasferito dalle cellule endoteliali alle cellule staminali leucemiche, spingendole in uno stato quiescente e non proliferativo che le rende altamente resistenti ai farmaci. In altre parole, lo stesso trattamento che libera il midollo dalla maggior parte delle cellule cancerose rimodella l’ambiente midollare in modo da proteggere le più pericolose.
Costruire un midollo osseo virtuale
Per analizzare questa dinamica, il team ha creato un modello computazionale basato su agenti del midollo osseo affetto da LMA. Ogni attore chiave—cellule blastiche, cellule staminali leucemiche e cellule endoteliali che rivestono i vasi—è rappresentato come un singolo “agente” che segue regole informate biologicamente. Molecole che diffondono, come TNF-α, miR-126, il TKI AC220 e un farmaco bloccante di miR-126 chiamato miRisten, si propagano attraverso il tessuto simulato. Il modello è stato calibrato con dati di imaging murino che mappano i reali pattern vascolari, incluse aree ricche o povere di vasi produttori di miR-126. Nelle simulazioni, il trattamento standard con TKI ha riprodotto in modo affidabile l’effetto di Giano: le blastiche sono diminuite, il TNF-α è calato, il miR-126 vascolare è aumentato, le cellule staminali si sono ritratte nelle nicchie protettive e la malattia è poi ricomparsa.
Spegnere lo scudo con tempi precisi
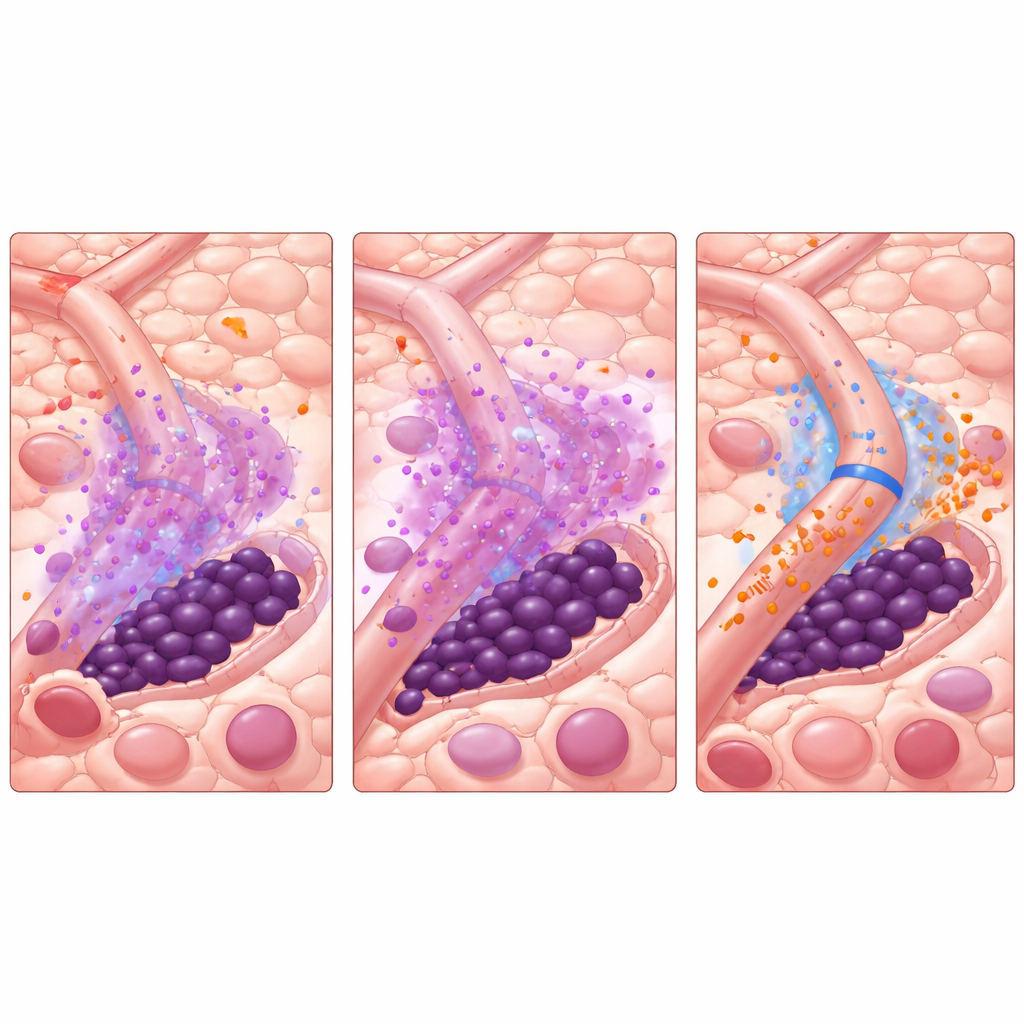
Con questo sistema virtuale, i ricercatori hanno testato modi per interrompere il circolo vizioso. Aggiungere semplicemente miRisten insieme al TKI aiutava ma raramente guariva la malattia nel modello. Un approccio più strategico si è rivelato più efficace: un breve “pretrattamento” con miRisten da solo per attenuare il miR-126 vascolare, seguito dal TKI da solo o da una terapia combinata continuata. In numerosi layout vascolari simulati, anche pochi giorni di pretrattamento con miRisten prima di iniziare AC220 riducevano o eliminavano drasticamente le recidive, limitando al contempo l’esposizione totale ai farmaci. Il modello ha anche mostrato che la distanza delle cellule staminali leucemiche dai vasi influisce fortemente sul loro destino—le cellule aderenti ai vasi ottengono la protezione maggiore, a meno che miR-126 non venga bloccato.
Cosa potrebbe significare per le cure future
In termini concreti, lo studio suggerisce che alcune cellule staminali leucemiche sopravvivono non perché i TKI siano inefficaci, ma perché i piccoli vasi del midollo temporaneamente passano in modalità “protettiva” durante il trattamento. Spegnendo brevemente un singolo segnale, miR-126, prima di somministrare il TKI, potrebbe essere possibile rimuovere questo scudo, costringere le cellule staminali a uscire dal nascondiglio e renderle vulnerabili ai farmaci esistenti. Benchè questo lavoro si basi su simulazioni informatiche ancorate a dati di laboratorio—non ancora su trial clinici—offre una strategia concreta: somministrare un farmaco che mira il microambiente appena prima e durante la terapia standard. Se validato, questo approccio potrebbe non solo migliorare gli esiti per le persone con LMA portatrice di mutazione FLT3, ma anche ispirare tattiche analoghe in altri tumori ematologici e solidi in cui il “quartiere” tumorale favorisce l’evasione terapeutica.
Citazione: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
Parole chiave: leucemia mieloide acuta, cellule staminali leucemiche, microambiente del midollo osseo, resistenza agli inibitori delle tirosin-chinasi, inibizione di miR-126