Clear Sky Science · it
Sviluppo di un modello severo di sindrome da realimentazione nel ratto e modellizzazione matematica dell'ipotassiemia associata
Perché ricominciare a mangiare può essere pericoloso
Quando persone gravemente malnutrite ricevono finalmente cibo o nutrizione per via endovenosa, i medici devono procedere con cautela. Una brusca immissione di calorie può scatenare la “sindrome da realimentazione”, una complicanza che altera gli equilibri elettrolitici e può danneggiare cuore, muscoli e polmoni. Un attore chiave è il fosforo, un minerale necessario per l’energia in ogni cellula. Questo studio ha usato ratti e modellizzazione al computer per chiarire perché il fosforo nel sangue può precipitare così drasticamente durante la realimentazione e come potremmo prevenire meglio questa caduta pericolosa.
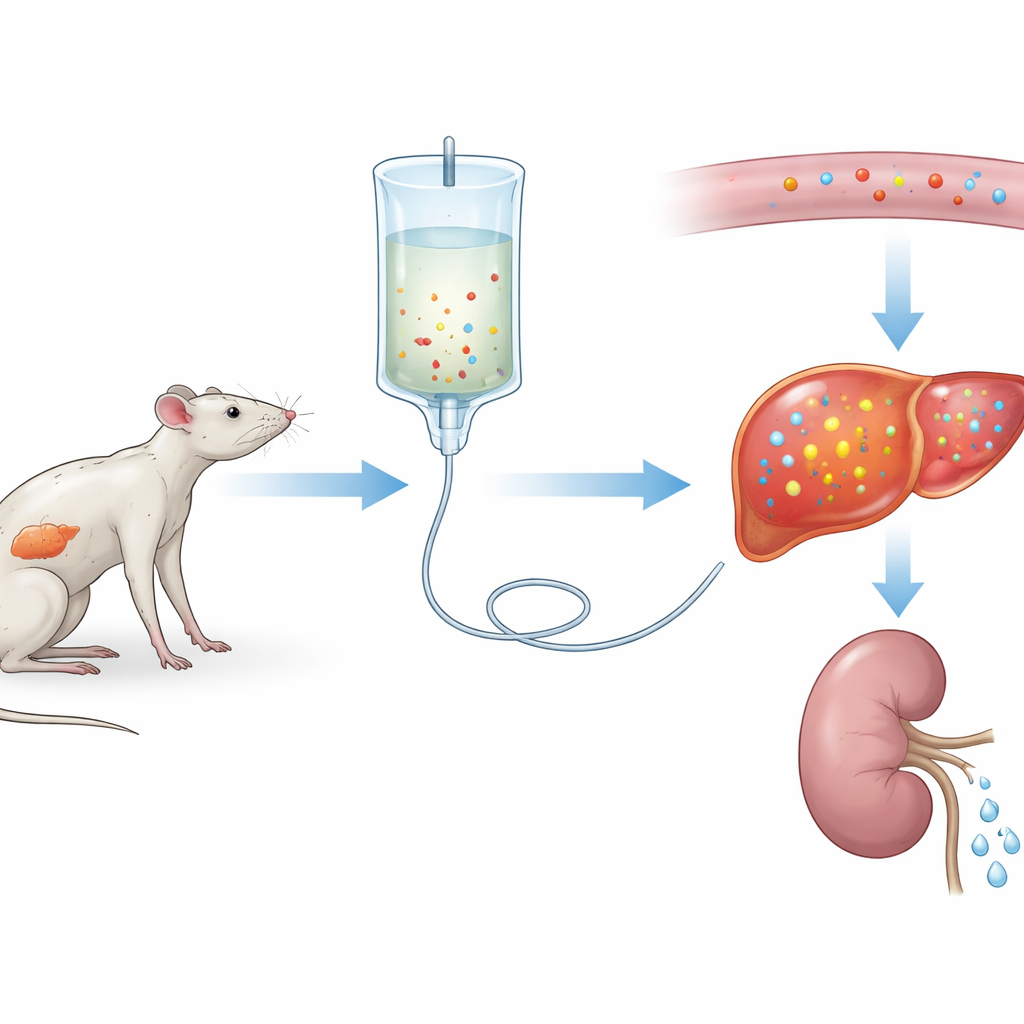
Uno sguardo più approfondito ai problemi della realimentazione
I ricercatori hanno prima creato una versione grave di sindrome da realimentazione nel ratto. Per tre settimane, un gruppo ha mangiato una dieta normale mentre un altro ha ricevuto pochissime proteine, simulando una malnutrizione prolungata. Entrambi i gruppi hanno poi ricevuto la stessa nutrizione endovenosa per tre giorni. I ratti con dieta a basso contenuto proteico hanno mostrato un calo brusco del fosforo ematico—circa il 75%—insieme a spostamenti di altri elettroliti e segni di danno d’organo, soprattutto al fegato e ai muscoli. Questi cambiamenti somigliavano a una severa sindrome da realimentazione nei pazienti, suggerendo che il team avesse costruito un modello sperimentale fedele.
Cosa succede al fosforo durante la realimentazione
Per capire come il fosforo si muove nell’organismo nel tempo, gli scienziati hanno prelevato ripetutamente campioni di sangue e urine dagli stessi ratti. Hanno scoperto che i livelli di fosforo ematico scendevano sia negli animali normali sia in quelli denutriti dopo l’inizio della realimentazione, ma la caduta è stata molto più profonda e prolungata nel gruppo malnutrito. Sorprendentemente, i reni ridussero effettivamente la perdita di fosforo nelle urine subito dopo la realimentazione, quindi il minerale non veniva eliminato. Invece, il fosforo veniva prelevato dal flusso sanguigno verso i tessuti, in particolare il fegato, dove le riserve erano state svuotate da settimane di dieta insufficiente. I calcoli informatici hanno confermato che i ratti sottopeso iniziavano con molto meno fosforo all’interno delle cellule e poi lo assorbivano aggressivamente una volta arrivate le nutrienti.
L’insulina non è tutta la storia
Poiché la realimentazione aumenta la glicemia e l’ormone insulina, da tempo si è ritenuto che l’insulina spinga il fosforo nelle cellule. Il team ha messo alla prova questa idea attenuando il rilascio di insulina con l’ormone somatostatina. Come previsto, la glicemia è aumentata, ma il crollo del fosforo ematico è migliorato di poco. Allo stesso tempo, i livelli di amminoacidi liberi—i mattoni delle proteine—sono aumentati. In un esperimento separato, gli scienziati hanno rimosso gli amminoacidi dalla infusione. In questo caso, i livelli di fosforo sono rimasti molto più stabili e il crollo severo è stato prevenuto, anche se i livelli di insulina erano simili. Questi risultati indicano un effetto combinato: sia l’insulina sia gli amminoacidi, non solo l’insulina, spingono le cellule a catturare fosforo extra durante la realimentazione.
Una rete di controllo nascosta in fegato e rene
Approfondendo, i ricercatori hanno esaminato le proteine epatiche coinvolte nel rilevamento dei nutrienti, concentrandosi su una via nota come mTOR, che risponde a insulina e amminoacidi. Nei ratti a basso contenuto proteico, la realimentazione ha attivato fortemente questa via e aumentato i livelli di un trasportatore di fosfato chiamato Pit2, che aiuta le cellule del fegato a prelevare fosforo. Lo schema corrispondeva al comportamento previsto dal loro modello matematico, che raggruppava questa rete in un unico segnale di controllo chiamato “simTOR”. Il modello richiedeva anche un fattore di feedback separato per spiegare come i reni regolano la perdita di fosforo nelle urine. Le misurazioni di un ormone derivato dall’osso, FGF-23, si adattavano bene a questo ruolo: i suoi livelli precipitavano quando iniziava l’alimentazione, limitando l’escrezione di fosforo, poi divergevano tra ratti normali e malnutriti in modo che rispecchiava il segnale di feedback simulato.
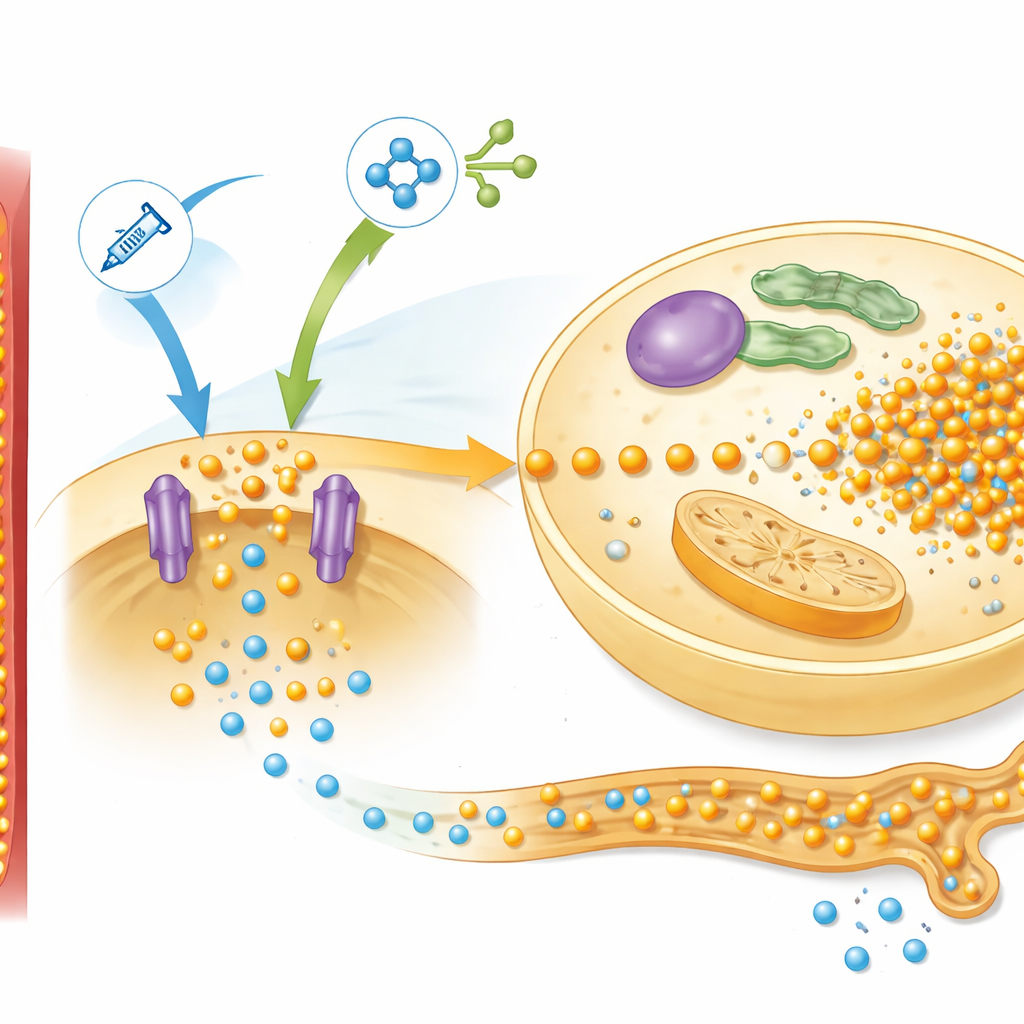
Usare la matematica per testare strategie di prevenzione
Regolando varie manopole nel loro modello al computer, gli autori hanno potuto porre domande “e se” difficili o rischiose da testare direttamente nei pazienti. L’analisi ha evidenziato tre influenze principali sulla profondità e sulla ripresa della caduta del fosforo: il fosforo intracellulare iniziale, la forza del sistema di captazione guidato da mTOR e la velocità di apporto di fosforo dalla nutrizione. Le simulazioni hanno suggerito che aggiungere semplicemente una grande quantità di fosfato al momento della realimentazione sarebbe difficile da bilanciare in sicurezza. Tuttavia, somministrare fosforo extra prima della realimentazione—permettere agli organi di ricostruire silenziosamente le loro riserve interne—potrebbe attenuare il successivo crollo dei livelli ematici. Ridurre il carico di amminoacidi, specialmente quelli che attivano fortemente mTOR e l’insulina, è risultato anch’esso protettivo negli esperimenti sugli animali.
Cosa significa per i pazienti
Per le persone a rischio di sindrome da realimentazione—come chi soffre di disturbi alimentari di lunga durata o di grave fragilità—questo lavoro suggerisce che il pericolo deriva da più di un semplice picco di glicemia. Gli organi denutriti iniziano la realimentazione con serbatoi di fosforo vuoti e, sotto la spinta combinata di insulina e amminoacidi, assorbono rapidamente il minerale dal sangue mentre i reni temporaneamente lo trattengono. Il risultato è una carenza circolante acuta e temporanea che può danneggiare tessuti vitali. Il modello nel ratto e il quadro matematico sviluppati qui indicano strategie di prevenzione più mirate: uso cauto e precoce di integratori di fosforo, controllo attento di nutrizioni ricche di amminoacidi e attenzione agli ormoni che governano l’escrezione renale. Insieme, questi approcci possono aiutare i clinici a nutrire in sicurezza i pazienti vulnerabili.
Citazione: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
Parole chiave: sindrome da realimentazione, ipofosfatemia, metabolismo del fosforo, segnalazione mTOR, nutrizione parenterale