Clear Sky Science · it
Spatial FBA rivela nicchie Warburg eterogenee nei tumori renali e consumo di lattato nel cancro colorettale
Perché il metabolismo tumorale nello spazio è importante
Le cellule tumorali non si comportano tutte allo stesso modo, nemmeno all'interno di uno stesso tumore. Alcune vivono vicino ai vasi sanguigni, altre in regioni più interne e poveramente irrorate; queste collocazioni influenzano il modo in cui ottengono e utilizzano il carburante. Questo studio introduce un nuovo modo di leggere quella «mappa metabolica» nascosta a partire da dati avanzati di espressione genica spaziale. Così facendo, gli autori scoprono schemi sorprendenti su come tumori diversi gestiscono una molecola chiave, il lattato, mettendo in discussione la visione classica secondo cui i tumori espellono semplicemente il lattato come rifiuto.
Trasformare mappe geniche in attività metabolica
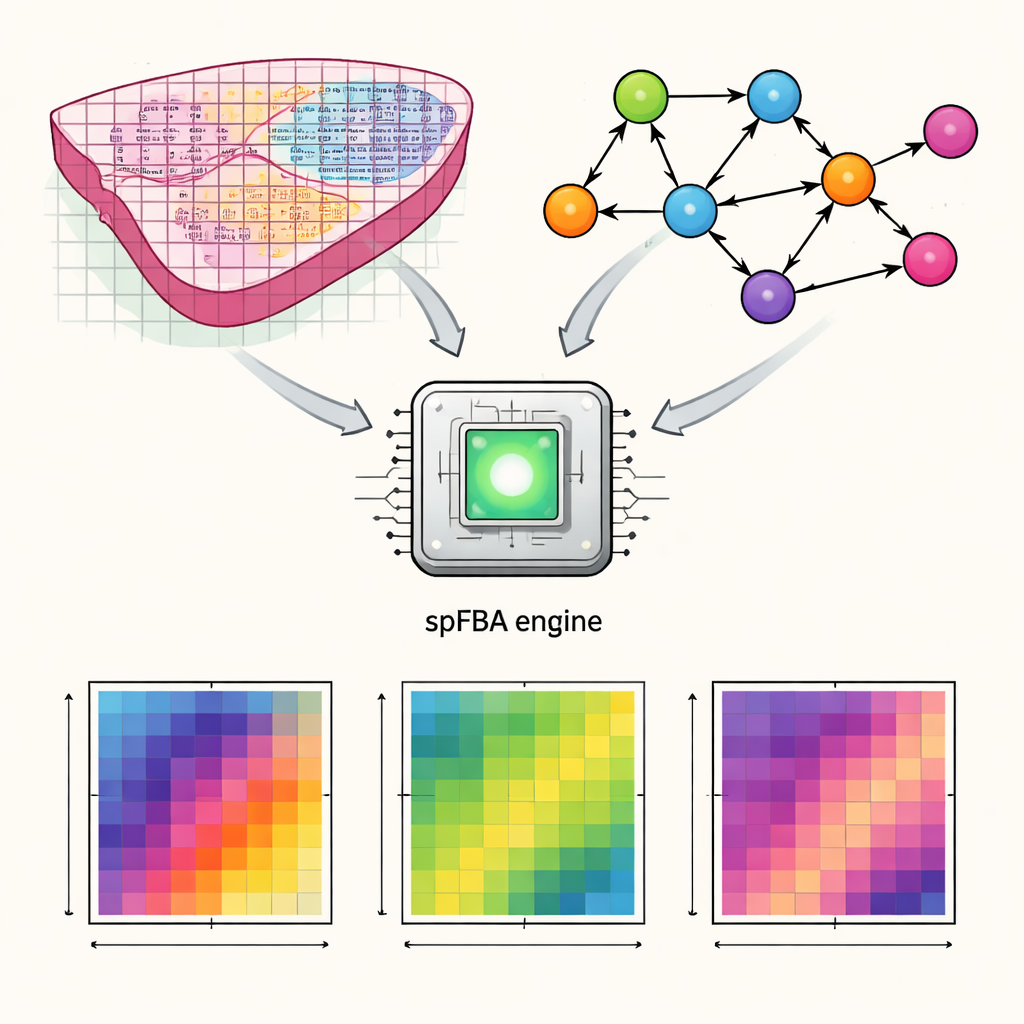
Gli autori hanno sviluppato un quadro computazionale chiamato spatial Flux Balance Analysis, o spFBA. Le tecnologie di trascrittomica spaziale misurano quali geni sono attivi in migliaia di piccoli punti attraverso una sottile sezione di tessuto. spFBA combina queste mappe spaziali di attività genica con modelli dettagliati del metabolismo umano, che descrivono come nutrienti come glucosio, ossigeno e amminoacidi vengono trasformati nelle cellule. Invece di assumere che ogni regione di un tessuto condivida lo stesso obiettivo metabolico, spFBA tratta ogni spot in modo indipendente, esplorando quali schemi di reazione sono possibili lì in base alle leggi della chimica e dell'equilibrio di massa. L'output è un insieme di “punteggi di arricchimento del flusso” che indicano, per ogni posizione, quanto probabilmente fluiscono diverse reazioni metaboliche e in quale direzione.
Testare il metodo sui tumori renali
Per verificare se spFBA producesse risultati biologicamente sensati, il team ha prima analizzato il carcinoma a cellule renali chiare, un tumore renale noto per dipendere fortemente dalla degradazione dello zucchero (glicolisi) e dal rilascio di lattato, un fenomeno chiamato effetto Warburg. Utilizzando dati spaziali pubblicati di dieci campioni di tumore renale, hanno chiesto se i pattern metabolici previsti corrispondessero alla struttura tissutale nota. Hanno riscontrato che gli spot raggruppati in base ai flussi metabolici inferiti si allineavano bene con l'organizzazione istologica osservata al microscopio e con i cluster basati solo sull'espressione genica. Importante, spFBA ha recuperato il contrasto metabolico atteso tra tessuto tumorale e rene normale: le regioni tumorali mostravano un maggiore utilizzo del glucosio, una più forte produzione di biomassa (un proxy della crescita cellulare) e una robusta secrezione di lattato. Allo stesso tempo, l'uso di ossigeno rimaneva sostanziale, rivelando che diverse parti dello stesso tumore possono mescolare fermentazione e respirazione a seconda dell'apporto locale di sangue.
I tumori colorettali raccontano una diversa storia del lattato
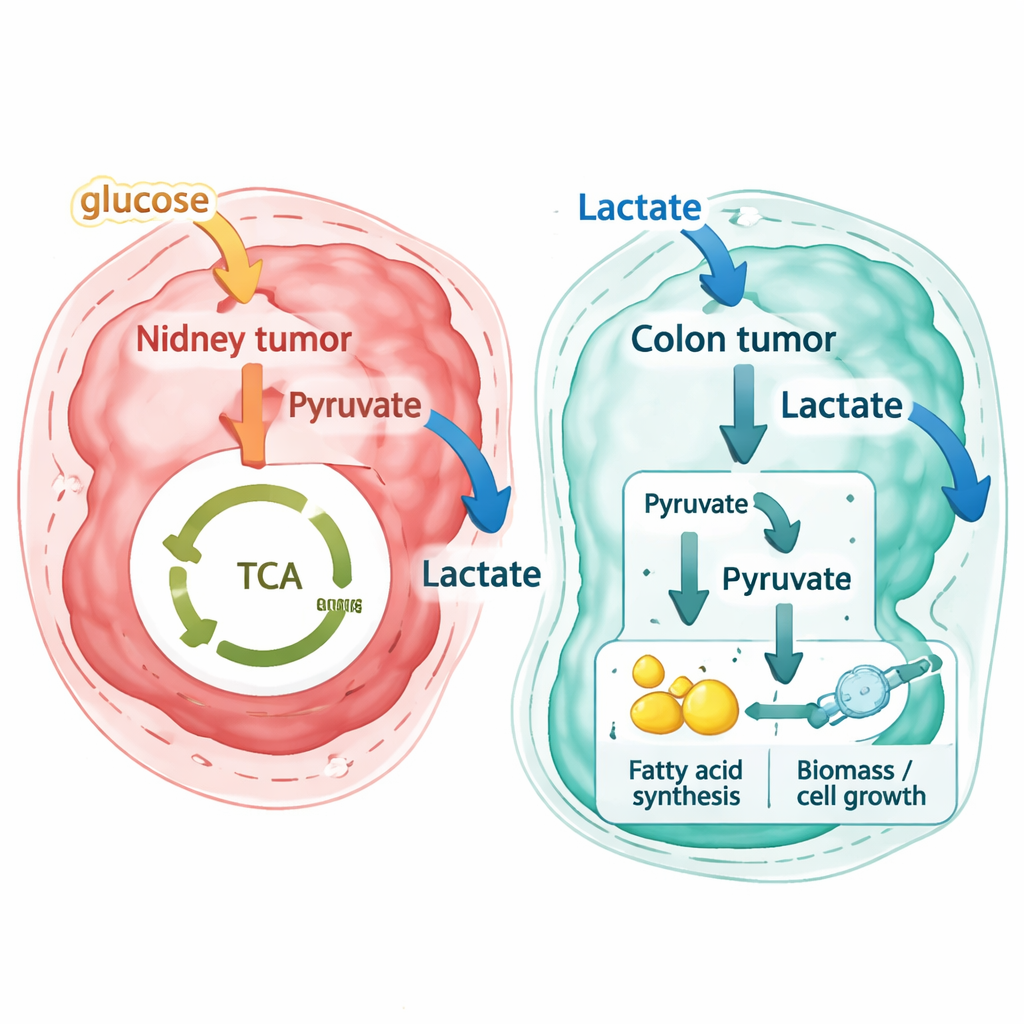
I ricercatori hanno quindi applicato la stessa pipeline a nuovi dataset spaziali ad alta risoluzione provenienti da un paziente con cancro colorettale primario e metastasi epatiche abbinate, oltre che a un dataset colorettale pubblico indipendente generato con un'altra tecnologia. Qui i risultati sono stati sorprendentemente diversi. Invece di esportare il lattato come rifiuto, la maggior parte delle regioni del cancro colorettale—sia nel tumore colon-primario originale sia nelle metastasi epatiche—sono state previste come importatrici di lattato dall'ambiente circostante. Le cellule stromali nel tessuto di supporto vicino tendevano a rilasciare piccole quantità di lattato, mentre le cellule tumorali agivano da forti consumatrici. Tracciando i pattern di flusso a livello di reazione, gli autori mostrano che queste cellule metastatiche non si limitano a bruciare il lattato nel consueto ciclo energetico mitocondriale. Piuttosto, convertono il lattato in mattoni di base che alimentano vie per la sintesi di lipidi e altri componenti necessari per la crescita cellulare, un «pseudo–reverse Warburg effect» in cui il lattato diventa materia prima per la biosintesi.
Nicchie metaboliche e la frontiera tumore-stroma
Poiché spFBA mantiene la disposizione spaziale, può individuare dove avvengono scambi metabolici particolari. Nei tumori renali, il metodo ha rivelato «quartieri» metabolici coesistenti: interfacce ricche di sangue e meglio ossigenate dove le cellule cancerose sia respirano sia fermentano, e noccioli più profondi e scarsamente vascolarizzati che dipendono maggiormente dalla fermentazione. Nelle metastasi epatiche colorettali, spFBA ha evidenziato contrasti netti al confine tra tumore e stroma, dove la gestione di glutammato e lattato cambiava direzione, suggerendo uno scambio intenso nella frontiera invasiva. In tutti i dataset, i flussi predetti correlavano con misure indipendenti basate sui geni della proliferazione, supportando il realismo biologico del modello. Crucialmente, lo stesso algoritmo prevedeva secrezione di lattato nel cancro renale ma captazione di lattato nel cancro colorettale, indicando che le differenze osservate emergono dai dati e non da un bias intrinseco del modello.
Cosa significa per comprendere e trattare il cancro
Per i non specialisti, il messaggio chiave è che il metabolismo del cancro non è solo anomalo—è anche altamente locale. Lo stesso tumore può ospitare più nicchie metaboliche, e tumori dall'aspetto simile in organi diversi possono usare le stesse molecole in modi opposti. Questo lavoro mostra che sovrapponendo l'espressione genica spaziale a modelli metabolici dettagliati, i ricercatori possono inferire dove i tumori sono probabilmente affamati di nutrienti particolari come il lattato. Nel cancro colorettale, la scoperta che le cellule tumorali consumano estensivamente il lattato e lo convogliano verso processi legati alla crescita solleva nuove domande su come la dieta, i microbi intestinali e il metabolismo epatico influenzino la progressione della malattia, e se bloccare l'uso del lattato potrebbe rendere questi tumori più vulnerabili alle terapie.
Citazione: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
Parole chiave: metabolismo del cancro, trascrittomica spaziale, lattato, effetto Warburg, cancro colorettale