Clear Sky Science · it
L’analisi dinamica delle reti rivela accoppiamenti a lunga distanza tra residui all’interfaccia pMHC alla base di un’aumentata immunogenicità
Come minuscoli frammenti virali guidano le nostre difese immunitarie
Le nostre cellule T citotossiche pattugliano l’organismo alla ricerca di segnali di infezione o tumore. Lo fanno scandagliando minuscoli frammenti proteici, detti peptidi, esposti sulla superficie delle cellule da molecole note come MHC di classe I. Questo studio pone una domanda sottile ma cruciale: come può una singola piccola modifica in uno di questi peptidi far sì che le cellule T rispondano molto più intensamente — o per nulla? La risposta coinvolge non solo la struttura statica, ma anche come l’intero complesso molecolare si muove e si flette nel tempo.
La serratura, la chiave e le parti in movimento
Per capire il lavoro conviene immaginare il complesso peptide–MHC (pMHC) come una serratura e il recettore delle cellule T (TCR) come una chiave. Il peptide si adagia in una gola sull’MHC e insieme formano la superficie che il TCR esplora. Ricerche precedenti hanno mostrato che sia la sequenza esatta del peptide sia la variante di MHC influenzano fortemente se una cellula T risponde. Gli scienziati hanno anche progettato “ligandi peptidici alterati” che portano piccole modifiche per modulare le risposte immunitarie, anche nella immunoterapia oncologica. Ma mentre conosciamo molto delle forme statiche di questi complessi, sappiamo molto meno su come i movimenti in un punto del peptide possano influenzare parti remote dell’interfaccia dove il TCR si lega effettivamente.
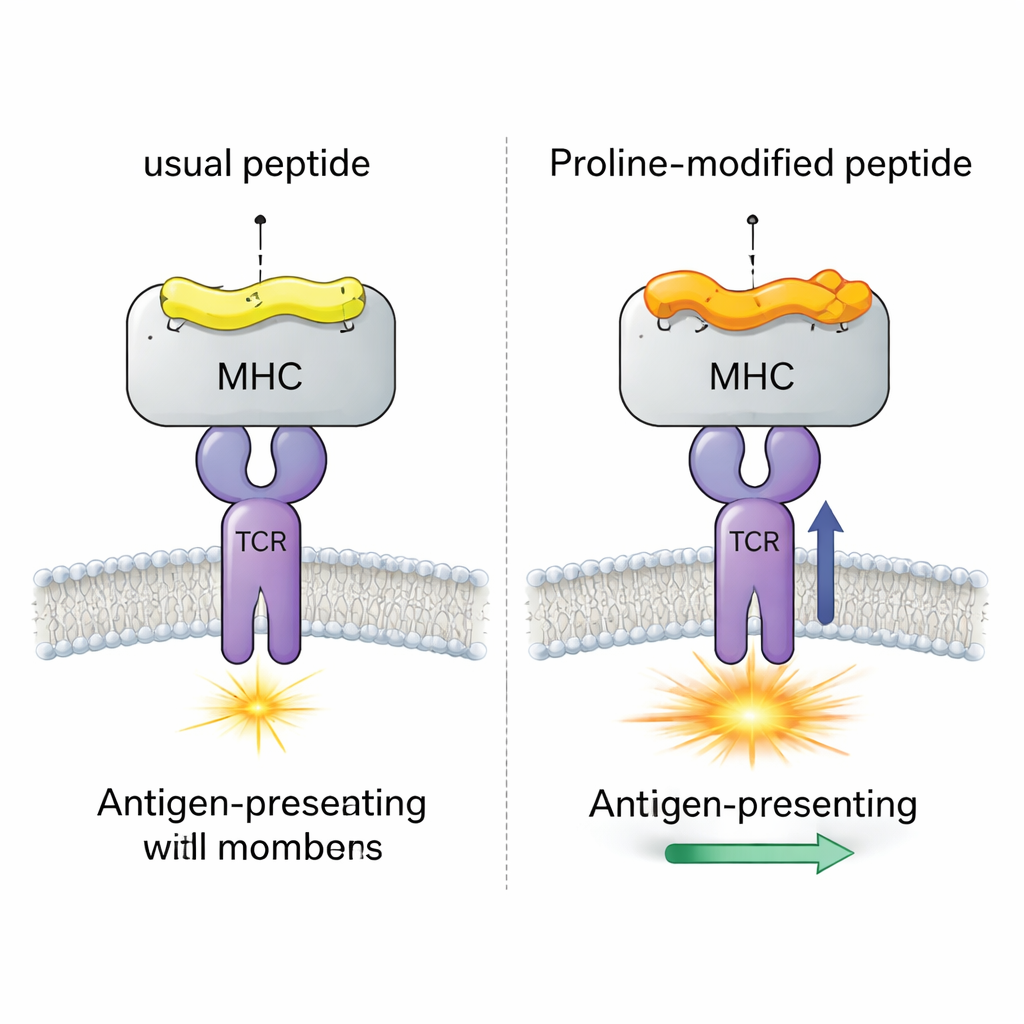
Un caso virale con quattro peptidi quasi identici
Il gruppo si è concentrato su un sistema ben studiato nel topo (LCMV) che coinvolge il peptide gp33, che normalmente induce forti risposte delle cellule CD8+. Hanno confrontato quattro versioni strettamente correlate di questo peptide, tutte legate allo stesso molecola MHC (H-2Db). Una versione è il peptide virale originale; una porta una mutazione di fuga immunitaria che le cellule T riconoscono a malapena; e due sono candidati vaccinali “alterati con prolina” dove un singolo amminoacido vicino all’inizio del peptide è stato sostituito con una prolina. Esperimenti precedenti avevano mostrato che questo scambio con la prolina aumenta la tenuta del complesso peptide–MHC e la risposta di un TCR modello (chiamato P14), ma il meccanismo dettagliato rimaneva poco chiaro.
Osservare le molecole che oscillano: simulazioni e cristallografia
Per scoprire cosa succede, gli autori hanno combinato strutture cristalline ad alta risoluzione con lunghe simulazioni atomiche al computer di ciascun complesso pMHC in movimento. Hanno esaminato quanto ciascun residuo amminoacidico fluttui nel tempo e come queste fluttuazioni cambino quando la terza posizione del peptide viene convertita in prolina. Correlando pattern di movimento attraverso molte simulazioni abbinate, hanno costruito una “mappa dinamica” di quali residui si muovono insieme, anche quando sono lontani nello spazio. Hanno poi trasformato questa mappa in una rete, dove ogni residuo è un nodo ed i collegamenti rappresentano movimenti statisticamente correlati, e hanno analizzato questa rete usando strumenti della teoria dei grafi simili a quelli impiegati nell’analisi delle reti sociali.
Comunicazione a lunga distanza all’interno della serratura immunitaria
La scoperta principale è che alterare il terzo residuo del peptide introducendo una prolina fa più che semplicemente irrigidire quel punto locale. Cambia il modo in cui il moto viene trasmesso lungo una delle eliche dell’MHC che bordano la gola di legame del peptide. Questo a sua volta influenza il comportamento di un altro residuo del peptide, la posizione sei, che si trova proprio sotto l’impronta del TCR ed è critico per il riconoscimento. Nelle versioni “buone” modificate con la prolina, questo residuo esplora una gamma più ampia di conformazioni, incluse quelle ottimali per il legame con il TCR. Nella variante di fuga immunitaria senza prolina, quel residuo è più bloccato e raramente assume l’orientamento favorevole al TCR. L’analisi di rete rivela che questa influenza viaggia attraverso specifici amminoacidi nella gola dell’MHC, formando una catena di residui dinamicamente accoppiati che collega il sito della modifica con la regione di contatto del TCR.
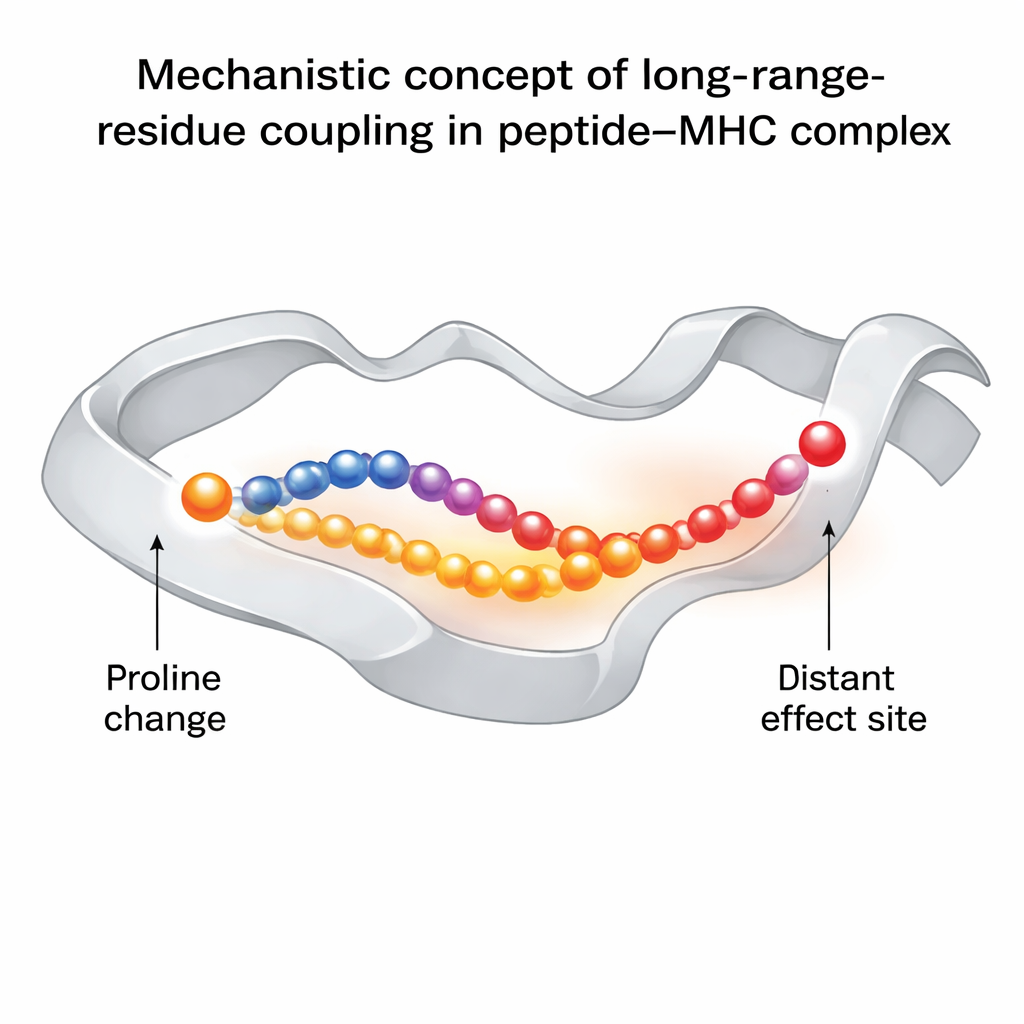
Perché questo importa per vaccini e immunoterapia
Questi risultati dimostrano che l’immunogenicità — quanto intensamente un peptide attiva le cellule T — non riguarda solo se le forme combaciano in un singolo istante, ma anche come il complesso respira e si flette nel tempo. Una modifica sottile in una posizione può propagarsi attraverso la rete molecolare, rendendo i residui chiave di contatto più propensi a mostrarsi in pose compatibili con il TCR. Il flusso di lavoro computazionale degli autori offre un modo per individuare sistematicamente tali accoppiamenti a lunga distanza, il che potrebbe aiutare a guidare la progettazione di peptidi alterati per vaccini e terapie oncologiche. In termini semplici, dimostrano che scegliendo con cura dove intervenire su un peptide, possiamo spingere l’intera serratura in uno stato dinamico più “pronto ad essere aperto” dalla chiave del sistema immunitario.
Citazione: Resink, T., Sala, B.M., Sun, R. et al. Dynamical network analysis reveals long-range residue couplings at the pMHC interface underlying enhanced immunogenicity. npj Syst Biol Appl 12, 15 (2026). https://doi.org/10.1038/s41540-026-00653-y
Parole chiave: riconoscimento delle cellule T, peptide MHC, dynamica delle proteine, ligandi peptidici alterati, immunogenicità