Clear Sky Science · it
Modellazione in silico della differenziazione dell’endoderma del proencefalo anteriore verso progenitori epiteliali polmonari
Trasformare le cellule staminali in costruttrici del polmone
Gli scienziati stanno imparando come indurre le cellule staminali di un paziente a diventare tessuto polmonare sostitutivo, che un giorno potrebbe riparare danni dovuti a malattie come BPCO, fibrosi o infezioni gravi. Questo articolo esplora come i ricercatori abbiano utilizzato la modellazione al computer per mappare e ottimizzare un passaggio cruciale in questo percorso: la trasformazione di un tipo cellulare intermedio, chiamato endoderma anteriore dell’intestino primitivo, in progenitori epiteliali polmonari precoci — le cellule iniziali che possono poi formare le vie aeree e gli alveoli polmonari.
Perché i progenitori polmonari sono importanti
Le cellule staminali pluripotenti indotte umane (iPSC) possono essere riprogrammate da tessuti adulti e poi guidate verso molti diversi organi. Per ricostruire tessuto polmonare, queste cellule attraversano prima diversi punti di sviluppo. Uno di questi è l’endoderma anteriore dell’intestino primitivo, uno strato che normalmente dà origine a parti del sistema respiratorio e digestivo nell’embrione. Da lì, con i segnali chimici corretti, le cellule possono diventare progenitori epiteliali polmonari, che esprimono marcatori polmonari precoci e possono successivamente maturare in cellule di vie aeree o alveolari specializzate. Poiché le future terapie cellulari richiederanno miliardi di queste cellule, i ricercatori necessitano di metodi per aumentare in modo affidabile le rese e adattare i protocolli a diverse linee cellulari di pazienti senza un laboratorio pieno di tentativi ed errori continui.
Costruire una versione virtuale della differenziazione cellulare
Il gruppo ha ampliato un quadro matematico precedente per costruire quello che, a loro conoscenza, è il primo modello a livello di popolazione di questa specifica transizione dall’endoderma anteriore ai progenitori polmonari. Hanno considerato due modi di rappresentare le cellule: una versione semplice che traccia solo il numero totale di cellule vive e una versione più dettagliata che segue separatamente le cellule dell’endoderma anteriore e i progenitori polmonari. In entrambi i casi, il modello segue anche il glucosio e il lattato nel mezzo di coltura, rappresentando nutrienti e rifiuti. Utilizzando strumenti della biologia dei sistemi, i ricercatori hanno costruito molte equazioni candidate su come le cellule crescono, muoiono e si differenziano, quindi hanno usato test di identifiability per scartare i modelli i cui parametri non potrebbero mai essere determinati in modo univoco, anche con dati perfetti.
Progettare esperimenti più intelligenti con il modello
Invece di adattare semplicemente i dati disponibili, i ricercatori hanno lasciato che il modello guidasse come condurre nuovi esperimenti. Hanno usato dati simulati per chiedersi quanto spesso fosse necessario misurare il numero di cellule e i livelli di nutrienti per stimare accuratamente i parametri del modello, bilanciando la precisione statistica con i costi e il lavoro delle frequenti misurazioni. Questo li ha portati a un piano pratico: misurazioni giornaliere per glucosio e lattato e conteggi cellulari ogni uno o due giorni, in quattro condizioni che variavano l’intensità della diluizione delle colture il giorno 10 e se il mezzo di crescita fosse rinnovato quotidianamente. Hanno poi eseguito questi esperimenti, misurando sia la popolazione cellulare totale sia, tramite citometria a flusso, le frazioni che restavano cellule dell’endoderma o che erano diventate progenitori polmonari.
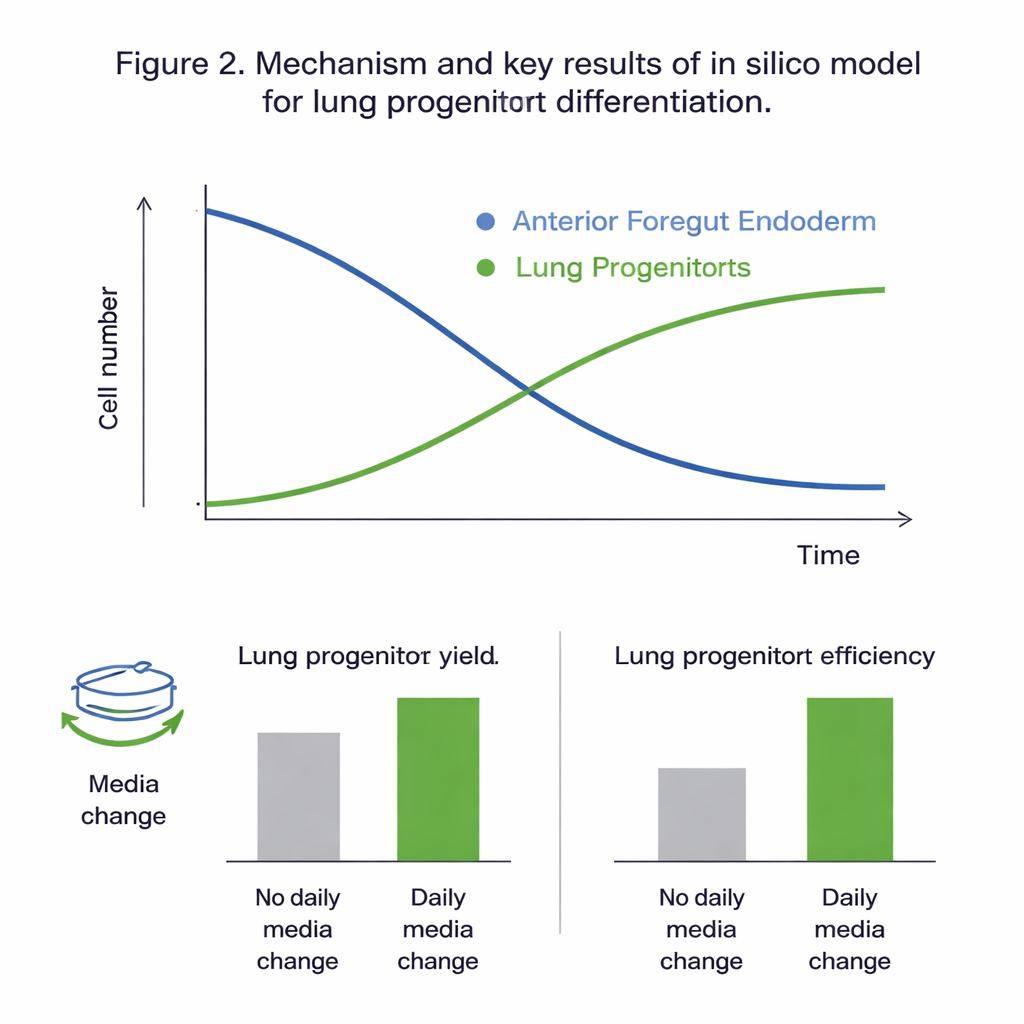
Quanto hanno rivelato gli esperimenti virtuali
Adattare tutte le versioni candidate del modello ai dati sperimentali ha mostrato che il modello a due popolazioni, che traccia separatamente le cellule dell’endoderma e i progenitori polmonari, poteva essere calibrato in modo affidabile e catturava al meglio il comportamento osservato. I controlli statistici hanno indicato che, nella finestra temporale studiata (giorni 11–15 del protocollo), la dinamica era guidata principalmente da proliferazione e differenziazione delle cellule dell’endoderma, mentre la proliferazione dei progenitori polmonari contribuiva poco. L’analisi di sensibilità globale ha rafforzato questo quadro, mettendo in evidenza i tassi di crescita, morte e differenziazione delle cellule dell’endoderma — e l’influenza del glucosio — come le leve principali che controllano l’esito. Il modello calibrato ha riprodotto dati non usati per la calibrazione con errori comparabili alla variabilità naturale degli esperimenti, suggerendo che fosse sufficientemente accurato per esplorare scenari «what‑if» in silico.
Ottimizzare i cambi di mezzo e le diluizioni cellulari
Con un sistema virtuale affidabile a disposizione, il team ha testato come due scelte pratiche del protocollo influenzino i risultati: quanto la coltura viene diluita (rapporto di split) al giorno 10 e se il mezzo di crescita viene sostituito ogni giorno. Le simulazioni hanno previsto che i cambi giornalieri del mezzo quasi raddoppiano il numero di progenitori polmonari e la resa per cellula iniziale, principalmente prevenendo l’esaurimento dei nutrienti e l’accumulo di rifiuti e di molecole di segnalazione instabili. Gli esperimenti hanno confermato da vicino queste previsioni. Il modello ha anche suggerito che l’utilizzo di rapporti di split più alti — distribuendo le cellule più sparse al giorno 10 — migliora la “resa per cellula in ingresso” di circa un quarto, anche se riduce il numero assoluto di cellule. In entrambi i casi, questi cambiamenti hanno avuto poco effetto sulla proporzione finale di progenitori polmonari nella coltura, spostando principalmente il numero di cellule che potevano essere prodotte in modo efficiente.
Cosa significa per le future terapie polmonari
Per un non specialista, il messaggio chiave è che gli autori hanno costruito una sorta di simulatore di volo per un passaggio critico nella coltivazione di cellule polmonari a partire da cellule staminali. Combinando esperimenti accuratamente progettati con una rigorosa modellazione matematica, mostrano come semplici scelte di protocollo — come la frequenza dei cambi di mezzo e la densità di semina delle cellule — possano influenzare drasticamente quante cellule «costruttrici del polmone» vengono prodotte, senza alterarne la qualità. Questo tipo di modellazione in silico può aiutare a snellire i protocolli futuri, ridurre il lavoro di tentativi sperimentali e, in ultima analisi, supportare una produzione più affidabile e scalabile di progenitori polmonari per la ricerca, la modellizzazione delle malattie e, infine, le terapie rigenerative.
Citazione: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
Parole chiave: cellule progenitrici polmonari, cellule staminali pluripotenti indotte, modellazione in silico, differenziazione cellulare, medicina rigenerativa