Clear Sky Science · it
Associazione tra alterazioni del numero di copie e il paesaggio trascrittomico immunitario nel cancro
Perché i nostri geni contano per l’immunoterapia del cancro
L’immunoterapia oncologica funziona aiutando il sistema immunitario a riconoscere e attaccare i tumori, ma solo una minoranza di pazienti ottiene benefici duraturi. Questo studio pone una domanda fondamentale con grandi conseguenze cliniche: come la confusione genetica all’interno delle cellule tumorali – in particolare grandi guadagni e perdite di DNA detti alterazioni del numero di copie – modella la reazione immunitaria contro il cancro, e possiamo rilevare questi effetti attraverso i modelli di attività genica?
Uno sguardo panoramico sui dati del cancro
Per affrontare la questione, i ricercatori hanno assemblato un’enorme collezione di 294.159 profili di attività genica provenienti da tumori e altri tessuti. Questi profili, tratti da diverse grandi banche dati pubbliche, catturano quali geni sono attivi o inattivi in migliaia di campioni che coprono molti tipi di cancro e condizioni sperimentali. Invece di esaminare i singoli geni uno per uno, il gruppo ha usato un metodo matematico per scomporre ogni profilo in “componenti” sottostanti ricorrenti – schemi di geni che tendono ad aumentare o diminuire insieme, ognuno riflettendo un processo biologico come una risposta immunitaria o l’effetto di una variazione del DNA.
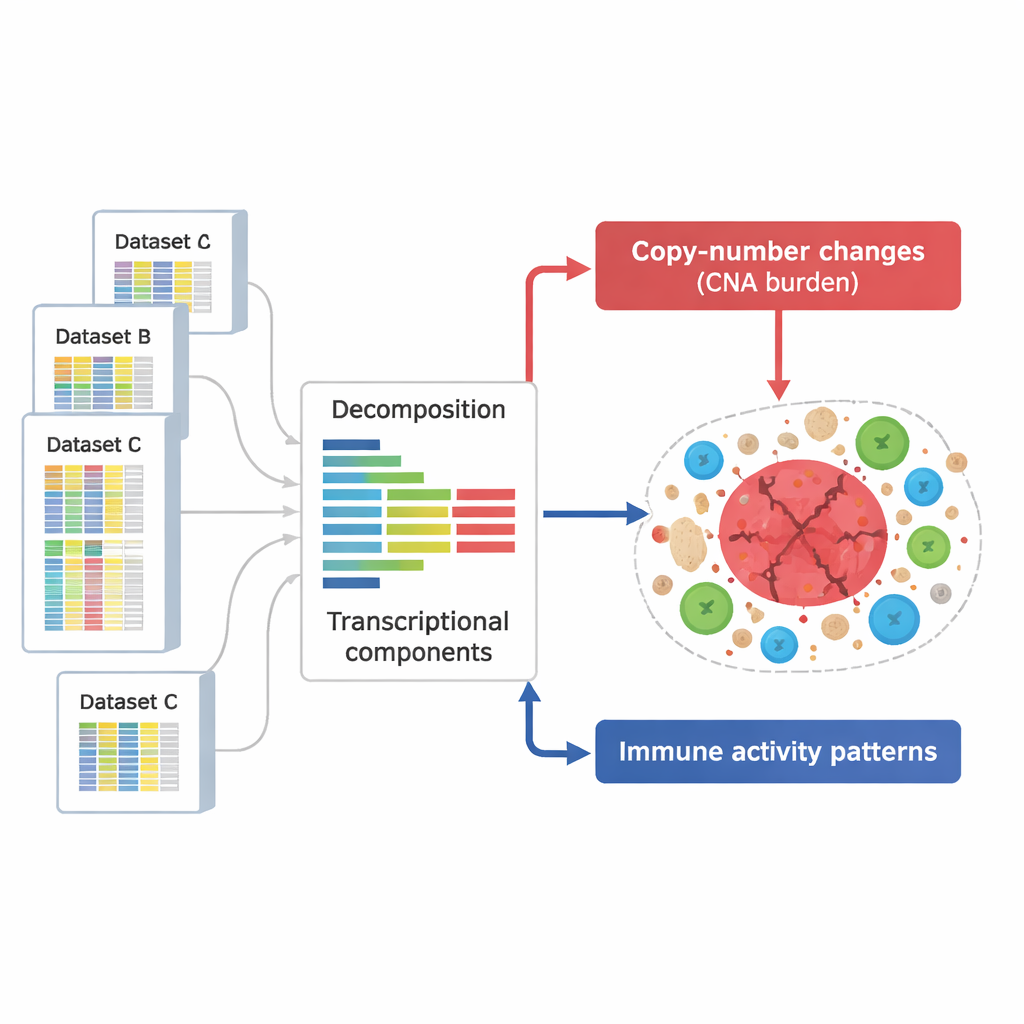
Separare i segnali del danno al DNA dai segnali immunitari
Dalle componenti così ottenute, gli scienziati hanno definito due gruppi chiave. Un gruppo catturava gli effetti delle alterazioni del numero di copie – tratti di cromosomi che vengono ripetutamente guadagnati o persi nelle cellule tumorali. Questi schemi coprivano quasi l’intero genoma, indicando che la maggior parte delle regioni coinvolte da tali alterazioni lasciava un’impronta rilevabile sull’attività genica. Un secondo gruppo di componenti risultava arricchito per geni coinvolti in funzioni immunitarie, come l’attivazione delle cellule T, l’attività delle natural killer e la presentazione degli antigeni. In totale, sono state identificate 657 componenti correlate al DNA e 283 correlate all’immunità, molte delle quali sono state riprodotte in dataset e tecnologie indipendenti, suggerendo che rappresentano caratteristiche robuste e generali della biologia tumorale.
Collegare i modelli alla risposta al trattamento
Il team ha poi chiesto se questi schemi immunitari potessero aiutare a prevedere chi risponde agli inibitori dei checkpoint immunitari, una classe importante di farmaci immunoterapici. Utilizzando dati di 13 studi clinici su 1.167 pazienti con sette tipi di cancro, hanno addestrato modelli computazionali per distinguere i responder dai non-responder basandosi esclusivamente sull’attività delle componenti immunitarie nei campioni tumorali pre-trattamento. Alcuni modelli hanno avuto prestazioni solide anche quando testati su gruppi di pazienti completamente indipendenti; per esempio, un modello addestrato su una coorte di carcinoma mammario ha predetto con precisione le risposte in una coorte diversa dello stesso tumore e ha mostrato prestazioni utili in vari altri tumori. Un piccolo insieme di schemi immunitari, incluse quelle legate alle risposte a interferoni, alle cellule natural killer e all’attivazione delle cellule T, ha contribuito maggiormente a queste predizioni.
Come il caos genetico rimodella l’immunità tumorale
Con questo quadro, i ricercatori hanno correlato in modo sistematico il carico complessivo di alterazioni del numero di copie – una misura dell’estensione con cui il DNA di un tumore è guadagnato o perso – con l’attività di ciascuno schema immunitario attraverso molti tipi di cancro. La maggior parte degli schemi immunitari mostrava una relazione inversa: i tumori con elevato carico di alterazioni del DNA tendevano ad avere minore attività delle componenti associate a funzioni immunitarie benefiche, come la presentazione degli antigeni e l’infiltrazione da parte di cellule immunitarie chiave. Tuttavia, una minoranza significativa di schemi si muoveva nella direzione opposta. I tumori con alto carico di alterazioni mostravano spesso segnali aumentati di tipi cellulari immunosoppressivi, incluse le cellule T regolatorie e alcuni macrofagi, oltre a cellule infiammatorie che possono promuovere la crescita tumorale anziché la sua distruzione. Analisi spaziali di sezioni tumorali hanno confermato che le regioni con ampie alterazioni del DNA coincidevano frequentemente con bassa attività di schemi immunitari utili e con zone “escluse” dall’immunità, dove le cellule immunitarie erano confinate ai margini del tumore.
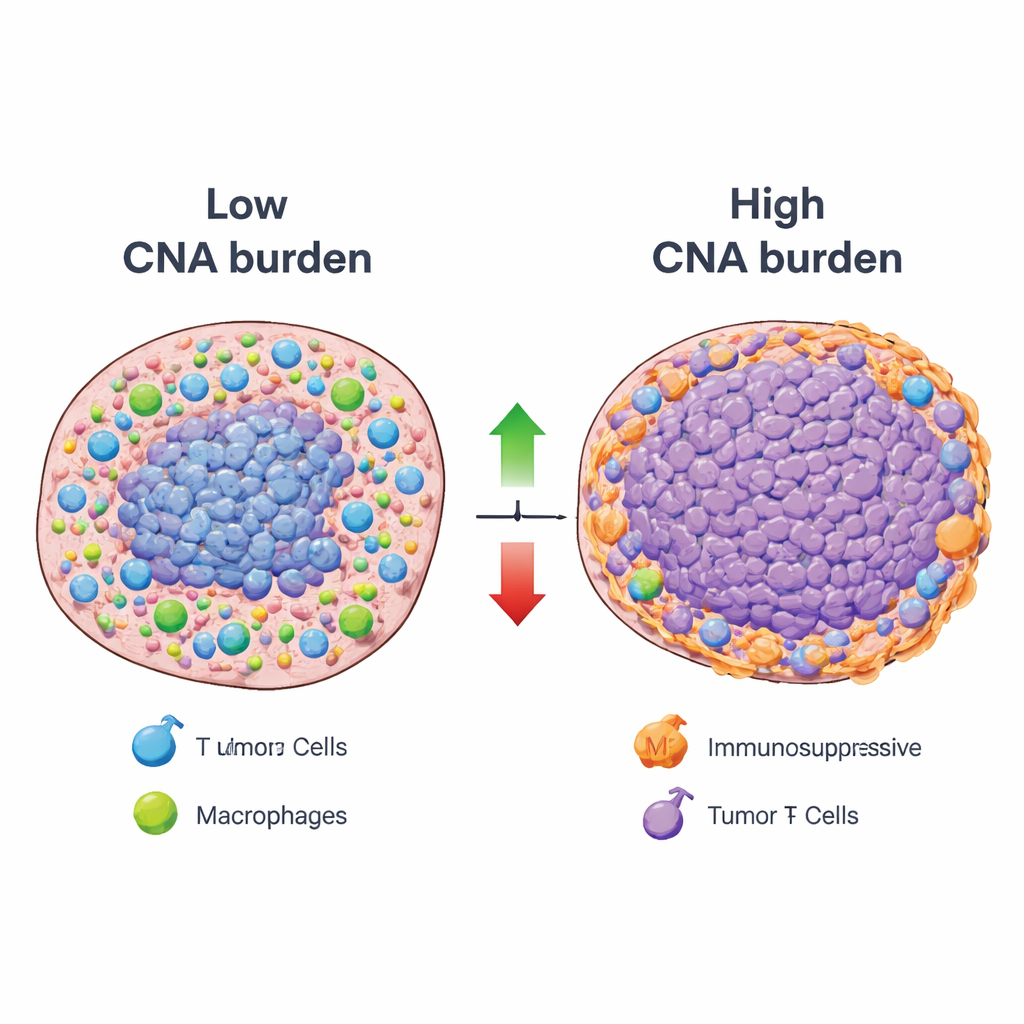
Che cosa significa per il futuro del trattamento del cancro
In termini semplici, lo studio mostra che i tumori gravati da guadagni e perdite di DNA su larga scala tendono sia ad attenuare risposte immunitarie utili sia a favorire ambienti immunitari soppressivi o protumorali. Tuttavia non sono immunologicamente silenti; al contrario, esibiscono stati immunitari specifici e ricorrenti che potrebbero essere vulnerabili a terapie mirate, come farmaci che bloccano la segnalazione di IL-17 o IL-23 o strategie per riprogrammare determinati macrofagi. Mappando queste relazioni DNA–immunità attraverso i tumori e rendendo la risorsa pubblicamente accessibile, il lavoro offre una guida dettagliata sul perché alcuni tumori geneticamente instabili resistono alle immunoterapie attuali e suggerisce nuove strategie di trattamento combinato per aiutare il sistema immunitario a superare quella resistenza.
Citazione: Loipfinger, S., Bhattacharya, A., Urzúa-Traslaviña, C.G. et al. Association of copy number alterations with the immune transcriptomic landscape in cancer. npj Syst Biol Appl 12, 28 (2026). https://doi.org/10.1038/s41540-026-00649-8
Parole chiave: immunoterapia del cancro, alterazioni del numero di copie, microambiente tumorale, inibitori dei checkpoint immunitari, trascrittomica