Clear Sky Science · it
La metabolomica assistita dall’apprendimento automatico decodifica il rimodellamento adattativo dei biofilm di Bacillus in risposta allo stress da pastorizzazione
Perché interessa a chi beve latte
Il latte pastorizzato è pensato per essere sicuro e duraturo, eppure alcuni batteri resistenti possono sopravvivere al trattamento termico e formare silenziosamente comunità viscide — chiamate biofilm — all’interno degli impianti di lavorazione. Questo studio pone una domanda inquietante con conseguenze pratiche: la pastorizzazione può a volte peggiorare questi biofilm e, in tal caso, quali cambiamenti chimici interni ai batteri ne sono responsabili?
Microbi tenaci negli impianti lattiero‑caseari moderni
Il latte è ricco di nutrienti e sostiene un’industria fiorente di prodotti lattiero‑caseari refrigerati a bassa temperatura. Ma offre anche un habitat per Bacillus, un gruppo di batteri che formano spore resistenti e si agganciano alle superfici metalliche. Questi microbi costruiscono biofilm — strati protettivi di cellule e sostanze adesive — che resistono alla pulizia, rallentano il trasferimento di calore e aumentano il rischio di alterazione o anche di malattie alimentari. Gli autori hanno isolato 14 ceppi di Bacillus da latte crudo in aziende agricole cinesi e hanno testato quanto bene formassero biofilm prima e dopo un passaggio di pastorizzazione simulata a 75 °C per 15 secondi. Sorprendentemente, mentre molti ceppi formarono biofilm più deboli dopo il riscaldamento, diversi ne divennero invece più forti e più adesivi.
Il calore che aiuta alcuni biofilm e ne danneggia altri
Per imitare le condizioni reali degli impianti, i ricercatori hanno cresciuto ceppi selezionati su campioni di acciaio inox 304 immersi in latte sterile. Hanno quindi colorato e misurato il materiale totale — batteri più residui di latte — rimasto sul metallo. Due ceppi, uno di Bacillus cereus (BC01) e uno di Bacillus subtilis (BS01), passarono da scarsa a forte adesione dopo la pastorizzazione, mentre cugini strettamente correlati (BC02 e BS02) mostrarono la tendenza opposta. Le immagini al microscopio elettronico rivelarono come cambiò l’architettura del biofilm: nei ceppi potenziati dal calore, la solita rete sottile e fibrosa di sostanze polimeriche extracellulari si fuse in aggregati spessi e compatti che intrappolarono più cellule e proteine del latte, formando un rivestimento più resistente e diffuso. Nei ceppi indeboliti dal calore, la matrice divenne rada e frammentaria.
Quando l’adesività superficiale non segue le regole
La saggezza convenzionale sostiene che più una spora è idrofoba (respinge l’acqua), meglio aderisce e più facilmente si forma un biofilm. Il team ha testato l’idrofobicità delle spore usando un sistema olio‑acqua e ha trovato il contrario di quanto prevedono i testi. Dopo la pastorizzazione, i ceppi che aumentarono la robustezza del biofilm mostrarono in realtà una minore idrofobicità delle spore, mentre quelli che persero capacità di biofilm divennero più idrofobi. Anche all’interno dei biofilm, le spore dei forti formatori risultavano meno idrofobe rispetto ai loro corrispondenti liberi in sospensione. Questa contraddizione indicava un meccanismo più profondo: cambiamenti indotti dal calore nel metabolismo e nell’espressione genica in grado di prevalere su semplici proprietà fisiche come l’adesività superficiale.
Riprogrammazione chimica sotto stress termico
Utilizzando la metabolomica non mirata — un’ampia indagine delle piccole molecole intracellulari — combinata con analisi di machine learning, gli autori hanno mappato come il calore rimodellasse la chimica del biofilm di ciascun ceppo. Tutti e quattro i ceppi presentarono grandi cambiamenti in centinaia di metaboliti, in particolare nei sistemi di trasporto e nelle vie degli amminoacidi, ma i dettagli variarono nettamente. In BC01, il riscaldamento sembrò attivare un enzima chiamato glutaminasi, prosciugando la riserva del nutriente del latte L‑glutamina e dell’amminoacido istidina. Questo spostamento fornì sia i mattoni per la matrice del biofilm sia rimosse freni naturali alla formazione del biofilm. Anche i livelli di xantosina, un composto che normalmente spinge i batteri lontano dai biofilm, diminuirono, favorendo probabilmente uno stile di vita stabile e adeso. In BS01, il calore ridusse arginina e diversi D‑amminoacidi, dopamina e acido arachidonico — molecole note da altri studi per destabilizzare i biofilm o bloccarne la formazione. Quantitativi inferiori di questi inibitori, insieme a un metabolismo energetico alterato, contribuirono a spostare l’equilibrio verso biofilm più robusti. Per contro, BC02 e BS02 soffrirono carenze di precursori polisaccaridici chiave e componenti del ciclo energetico, e in BS02 metaboliti anti‑biofilm come D‑triptofano e D‑arabinosa aumentarono, compromettendo collettivamente la crescita del biofilm.
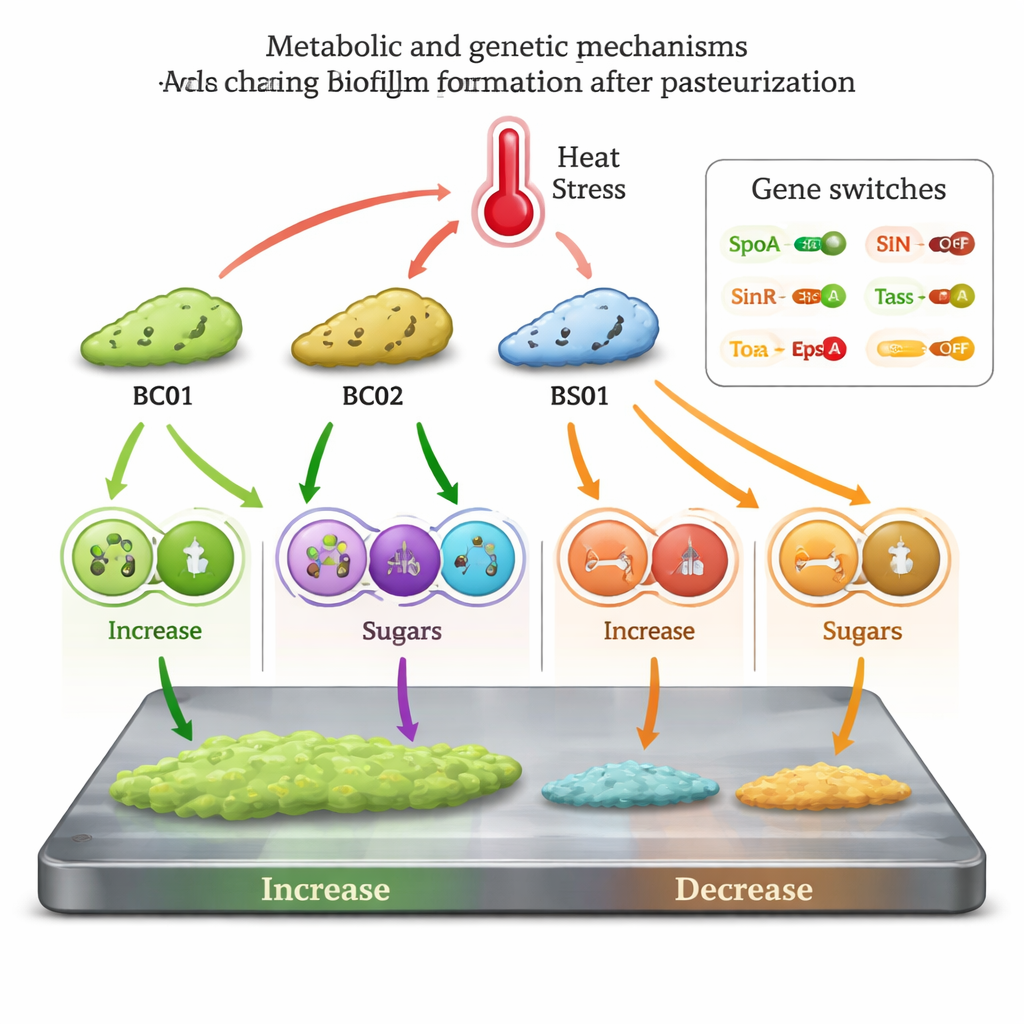
Geni che fanno scattare l’interruttore del biofilm
Per collegare la chimica al comportamento, il team ha misurato geni chiave legati al biofilm. Nei ceppi rinforzati dal calore BC01 e BS01, i regolatori principali che promuovono la formazione del biofilm (Spo0A, TasA ed EpsA) risultarono incrementati, mentre SinR, un gene che normalmente tiene sotto controllo i geni del biofilm, fu ridotto. Il modello opposto apparve in BC02 e BS02. Insieme, i dati metabolici e le letture geniche supportano un modello secondo cui la pastorizzazione funziona come un segnale di stress che alcune linee di Bacillus sfruttano: riprogrammano il loro metabolismo, riducono certe molecole naturali anti‑biofilm e azionano interruttori genetici per produrre più matrice e rivestimenti più spessi, anche se la loro attività complessiva rallenta.
Cosa significa per un latte più sicuro
Per i consumatori, il messaggio non è che il latte pastorizzato sia insicuro, ma che i microbi che sopravvivono al trattamento termico possono essere più adattabili del previsto. Piuttosto che limitarsi a rendere le spore più resistenti, la pastorizzazione può spingere alcuni ceppi di Bacillus in una modalità di «resistenza» in cui costruiscono biofilm più forti all’interno di tubazioni e serbatoi. Identificando metaboliti specifici e vie geniche che guidano questo cambiamento, lo studio suggerisce nuove strategie per contrastarlo: invece di fare affidamento solo su riscaldamenti più intensi o prolungati, i trasformatori potrebbero un giorno aggiungere bloccanti metabolici innocui o adattare i regimi di pulizia per interrompere il sistema chimico che sostiene questi biofilm. In sostanza, comprendere come il calore rimodella la chimica batterica apre la strada a strategie più intelligenti per mantenere i prodotti lattiero‑caseari sia nutrienti sia affidabilmente puliti.
Citazione: Liang, L., Wang, P., Zhao, X. et al. Metabolomics aided by machine learning decodes adaptive remodeling of Bacillus biofilms in response to pasteurization stress. npj Sci Food 10, 62 (2026). https://doi.org/10.1038/s41538-026-00712-y
Parole chiave: latte pastorizzato, biofilm di Bacillus, sicurezza alimentare, lavorazione dei latticini, metabolismo batterico