Clear Sky Science · it
Inibizione di CDK8 ristabilisce la guarigione compromessa delle fratture ischemiche
Perché il flusso sanguigno conta quando le ossa si rompono
La maggior parte delle ossa rotte alla fine si ricongiungono, ma per milioni di persone ogni anno questo processo si arresta. Un cattivo apporto di sangue attorno a una frattura — noto come ischemia — aumenta drasticamente il rischio che una rottura guarisca lentamente, male o per nulla. Questo studio esplora perché ciò avviene a livello cellulare e testa una pillola sperimentale che sembra spingere il corpo lontano da una riparazione simile a una cicatrice e di nuovo verso la vera rigenerazione ossea.
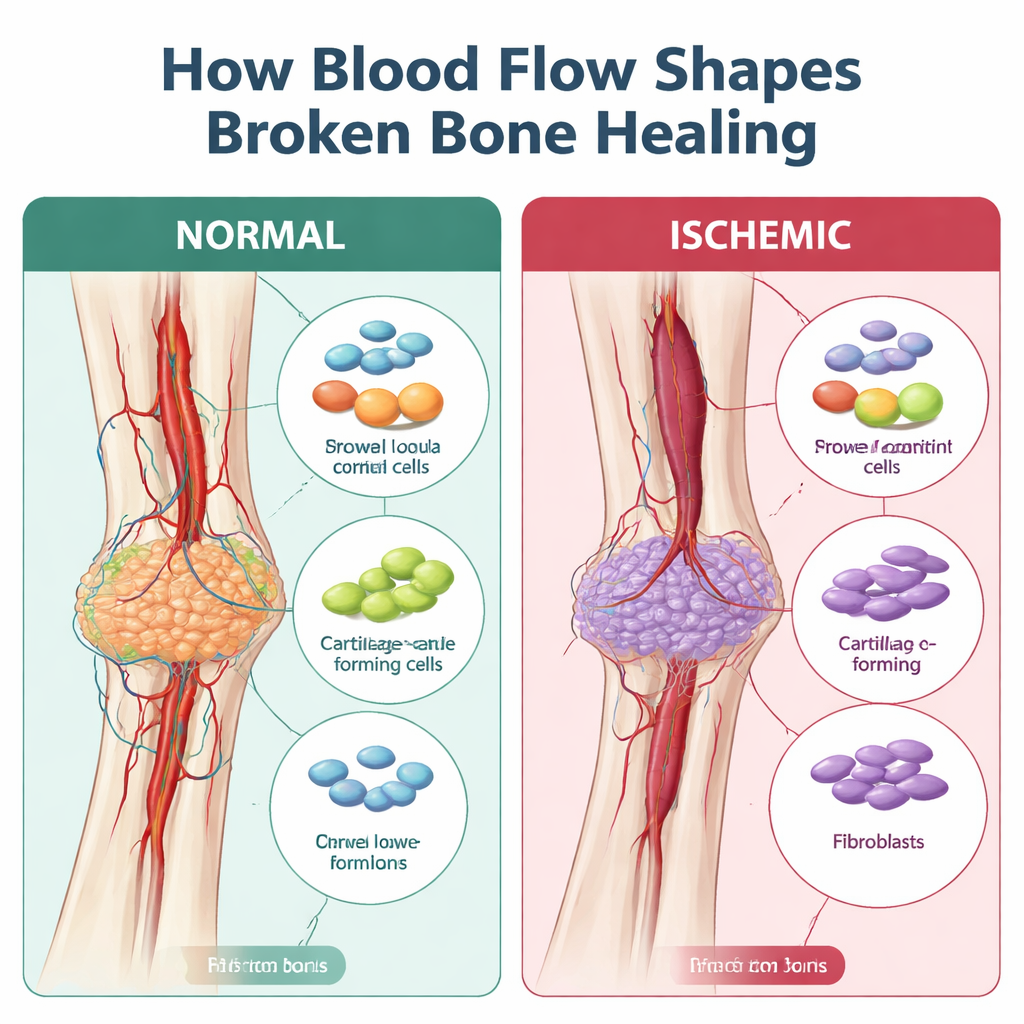
Quando la guarigione si trasforma in cicatrice invece che in ricostruzione
Normalmente l’osso guarisce costruendo un ponte morbido di cartilagine che viene gradualmente sostituito dall’osso duro. Questo ponte, chiamato callo, dipende da un apporto di cellule di supporto simili a cellule staminali, cellule immunitarie e vasi sanguigni che coordinano la riparazione. Nelle fratture ischemiche, lavori precedenti avevano mostrato che il callo tende a essere più piccolo, più debole e pieno di tessuto fibroso, più simile a una cicatrice che a una solida porzione di nuovo osso. Ciò che mancava era una mappa dettagliata di quali cellule deviano e quando, durante questo scostamento dalla corretta guarigione.
Cellule singole rivelano una deviazione verso la fibrosi
I ricercatori hanno usato un modello murino in cui un’arteria della gamba viene danneggiata chirurgicamente al momento della frattura, imitandone da vicino la perdita di flusso sanguigno osservata in lesioni gravi o in persone con malattie vascolari o fumatrici. Hanno quindi applicato il sequenziamento dell’RNA a singola cellula, una tecnica che legge i geni attivi in migliaia di cellule individuali, ai calli di frattura a quattro e sette giorni dall’infortunio. Nelle fratture ben perfuse, il callo iniziale era pieno di cellule immunitarie che presto lasciavano il posto a cellule stromali in espansione — le cellule di supporto che diventano cartilagine e osso. In condizioni ischemiche, invece, c’erano molto meno cellule che formano cartilagine e osso e molte più fibroblasti, le cellule che depositano tessuto fibroso. L’analisi computazionale delle “traiettorie” ha mostrato che, invece di maturare in modo regolare da progenitori precoci a cartilagine, le cellule stromali nell’osso ischemico spesso deviano attraverso uno stato simile ai fibroblasti, corrispondendo al callo più simile a una cicatrice osservato al microscopio.
Un freno molecolare sulle cellule che costruiscono l’osso
Approfondendo l’attività genica di queste cellule, il gruppo ha trovato un forte segnale di stress cellulare nei calli ischemici, inclusi alti livelli di proteine da shock termico. Tra i cambiamenti più sorprendenti vi era un’impennata nell’attività di un gene chiamato Cdk8, che codifica per un enzima regolatorio facente parte di un importante complesso di trascrizione e che può rallentare o reindirizzare come le cellule rispondono ai segnali. Cdk8 era noto per bloccare la differenziazione cellulare in altri contesti. Qui risultava particolarmente elevato nei progenitori stromali precoci nell’osso ischemico. Cellule stromali mesenchimali umane coltivate in condizioni di basso ossigeno in laboratorio — imitando il ridotto flusso sanguigno — aumentarono anch’esse l’espressione di CDK8, collegando direttamente la carenza di ossigeno a questo potenziale “freno” sulla formazione di cartilagine e osso.
Spegnere CDK8 per ripristinare la riparazione
I ricercatori hanno quindi chiesto se bloccare CDK8 potesse liberare le cellule stromali a riprendere la corretta guarigione. In coltura cellulare, trattare progenitori murini e umani con inibitori selettivi di CDK8 aumentò i geni chiave della cartilagine e la produzione di matrice cartilaginea, e migliorò anche la mineralizzazione quando le stesse cellule venivano indotte a diventare osso. Il team ha poi testato un inibitore orale di CDK8/19 chiamato SNX631-6 in topi con fratture ischemiche. Somministrato durante la finestra precoce di formazione della cartilagine, il farmaco aumentò la quantità di cartilagine nel callo. Quando il trattamento fu esteso nella successiva transizione da cartilagine a osso, i calli mostrarono più osso totale, contenuto minerale più elevato e dimensioni complessive maggiori alle scansioni micro–CT e alle sezioni tissutali, indicando una riparazione strutturale più robusta.
Dalla scoperta di laboratorio a possibili nuove terapie
Nel complesso, i risultati suggeriscono che l’ischemia indirizza le cellule della riparazione verso un destino stressato e fibrotico in parte aumentando CDK8, che limita la loro capacità di diventare cartilagine e osso. Bloccare questo enzima sembra rilasciare quel freno, permettendo di formare più cartilagine all’inizio e più osso successivamente, anche quando l’apporto di sangue è compromesso. Poiché gli inibitori di CDK8 sono già in fase di sperimentazione nei pazienti oncologici, potrebbero un giorno essere riproposti per aiutare persone ad alto rischio di scarsa guarigione delle fratture — come anziani, fumatori o chi ha malattie vascolari — a rigenerare osso forte invece di tessuto cicatriziale fragile.
Citazione: Capobianco, C.A., Song, M.J., Farrell, E.C. et al. Inhibition of CDK8 rescues impaired ischemic fracture healing. npj Regen Med 11, 12 (2026). https://doi.org/10.1038/s41536-026-00456-z
Parole chiave: guarigione delle fratture ossee, ischemia, inibitore di CDK8, cellule stromali mesenchimali, fibrosi