Clear Sky Science · it
La mappa sensoriale olfattiva è perturbata in un modello murino transgenico di malattia di Parkinson che sovraesprime α-sinucleina umana wild-type
Perché la perdita dell'olfatto è importante nel Parkinson
Molti associano la malattia di Parkinson a un disturbo del movimento, ma per la maggior parte dei pazienti la prima funzione a guastarsi è il senso dell'olfatto. Questa perdita può manifestarsi decenni prima del tremore o della rigidità, rendendola un potente segnale precoce. Lo studio descritto qui pone una domanda semplice ma ancora irrisolta: che cosa si guasta esattamente nel circuito cerebrale dell'olfatto quando iniziano i cambiamenti legati al Parkinson? Indagando questa questione in un modello murino progettato con cura, i ricercatori rivelano come una proteina chiave del Parkinson sconvolga la «mappa olfattiva» interna del cervello e indicano una nuova fonte facilmente accessibile di indizi precoci sulla malattia.
La mappa olfattiva del cervello
Nelle nostre narici ci sono milioni di cellule olfattive specializzate, ognuna delle quali risponde a particolari molecole d'odore. Queste cellule inviano lunghe fibre sottili alla parte anteriore del cervello, dove convergono in minuscoli nodi chiamati glomeruli all'interno del bulbo olfattivo. Ogni tipo di odore attiva uno schema specifico di glomeruli, formando una mappa sensoriale precisa che permette al cervello di distinguere, ad esempio, il caffè dalla cannella o il fumo dal profumo. Nei topi sani, le cellule che esprimono un recettore odoroso (chiamato M72) e un altro (chiamato P2) proiettano in modo affidabile a soli due glomeruli ben definiti per bulbo, creando una mappa altamente ordinata e riproducibile.
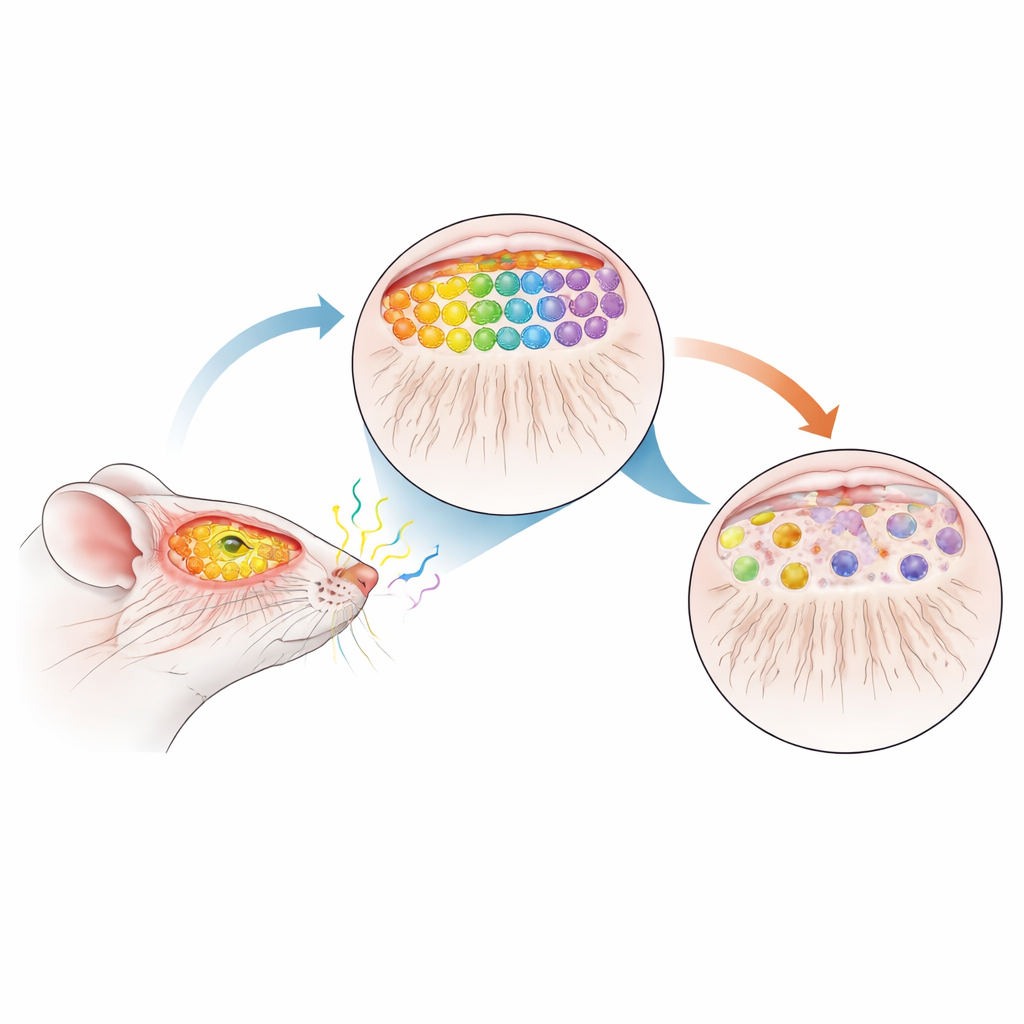
Un topo come sostituto del Parkinson precoce
Per capire come la malattia di Parkinson possa disturbare questa mappa, il gruppo ha usato topi che sovraproducono la α-sinucleina umana normale, la stessa proteina che forma aggregati nel cervello delle persone con Parkinson. Hanno poi incrociato questi animali con topi marcati per M72 e P2 in modo da poter seguire visivamente le cellule olfattive selezionate e le loro connessioni. È importante sottolineare che l'eccesso di α-sinucleina si attiva solo dopo la nascita e si accumula gradualmente con l'età, riproducendo il decorso lento e progressivo della malattia umana. A 12 mesi di età — all'incirca la mezza età per un topo e comparabile a una fase prodromica, o pre-diagnostica, negli esseri umani — i ricercatori hanno esaminato in dettaglio i sistemi olfattivi degli animali.
Quando la mappa olfattiva si disfa
Colorando i neuroni marcati e seguendone i percorsi, gli scienziati hanno osservato una marcata rottura della mappa olfattiva nei topi che sovraesprimono α-sinucleina. Il numero di neuroni M72 e P2 nel naso è crollato — circa tre quarti in meno per M72 e quasi la metà per P2 — mentre le loro fibre verso il bulbo risultavano fortemente ridotte. Invece di convergere ordinatamente su due glomeruli robusti, le fibre residue spesso formavano molteplici glomeruli più piccoli di dimensioni e posizioni variabili. Questi nodi «extra» non apparivano in posizioni coerenti da topo a topo, segnalando una perdita della precisione topografica normale. Un marcatore ampio delle terminazioni delle cellule olfattive, VGLUT2, risultava anch'esso ridotto di circa il 44% nel bulbo, indicando che questa degenerazione si estendeva ben oltre i due tipi di recettori marcati.
Collegare circuiti danneggiati alla perdita dell'olfatto
Il danno strutturale si traduceva in problemi olfattivi misurabili. I topi anziani con α-sinucleina impiegavano più tempo a trovare cibo nascosto, mostravano una peggiore capacità di discriminare un odore dall'altro e non preferivano aree marcate con il proprio odore — test comportamentali che insieme rivelano iposmia e compromissione della discriminazione odorosa. Avevano inoltre bisogno di concentrazioni di odore molto più elevate per rispondere, evidenziando una sensibilità ridotta. Questi deficit non si manifestavano nei topi giovani, nei quali i neuroni marcati e le loro mappe apparivano ancora per lo più normali, collegando la tempistica della perdita funzionale alla successiva rottura della mappa sensoriale piuttosto che a uno sviluppo alterato precoce. Degno di nota, sebbene la proteina problematica fosse abbondante nel bulbo olfattivo, non era rilevabile nell'epitelio sensoriale del naso, suggerendo che i cambiamenti all'interno del circuito del bulbo — in particolare nelle cellule mitrali che trasmettono l'informazione olfattiva in avanti — siano i probabili responsabili della perturbazione della mappa.
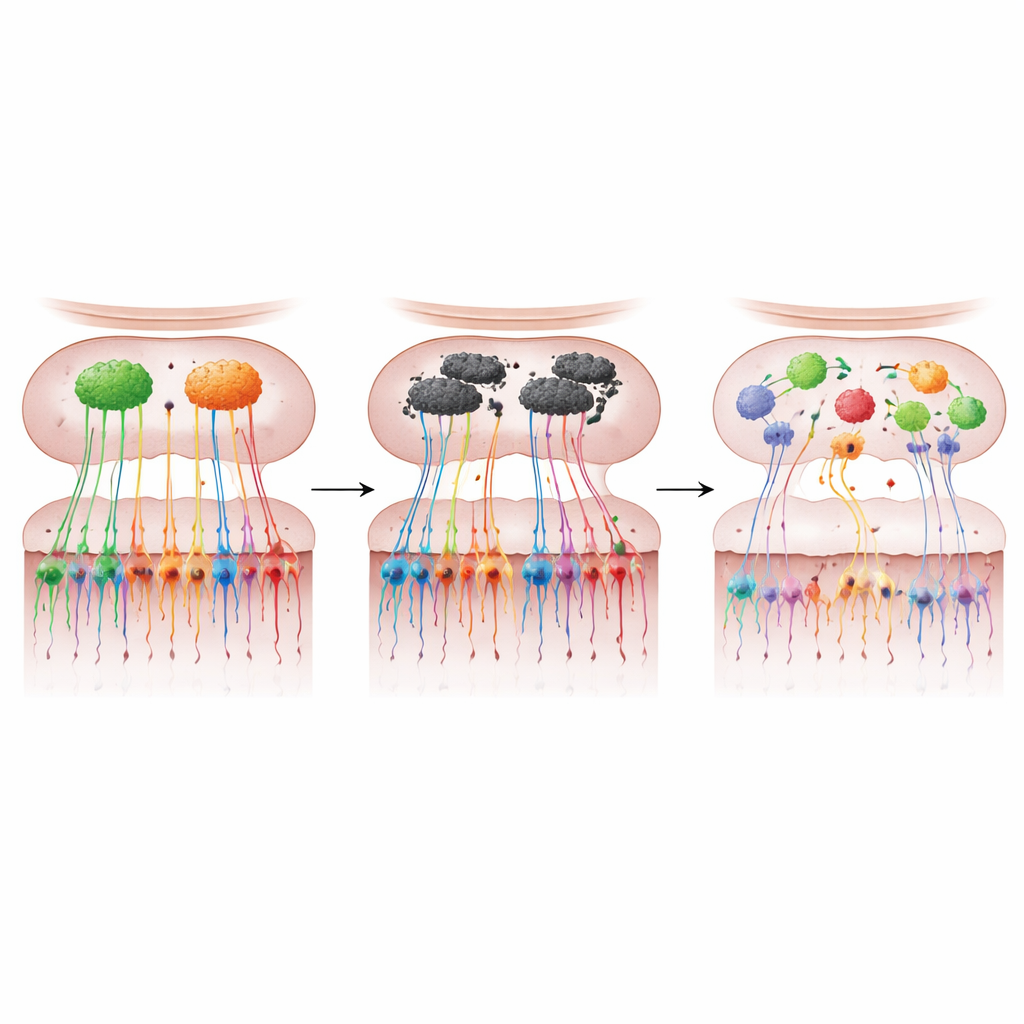
Le cellule olfattive come finestre sulla malattia precoce
Nel complesso, il lavoro sostiene un messaggio chiaro per i non specialisti: in questo modello murino simile al Parkinson, la sovrapproduzione di α-sinucleina nel bulbo olfattivo porta sia alla perdita sia al disordine delle connessioni delle cellule olfattive, deformando la mappa degli odori del cervello e causando problemi olfattivi precoci. Poiché le cellule sensoriali del naso sono legate allo sviluppo del cervello ma possono essere campionate con tamponi o biopsie minimamente invasive, gli autori sostengono che cambiamenti simili negli esseri umani potrebbero fornire un biomarcatore precoce potente della malattia di Parkinson. Mappare le impronte molecolari di queste cellule, suggeriscono, potrebbe non solo aiutare a individuare persone a rischio anni prima della comparsa dei sintomi motori, ma anche offrire nuovi spunti su come la malattia inizi e si diffonda — e su come potrebbe essere rallentata o prevenuta.
Citazione: Biju, K.C., Hernandez, E.T., Stallings, A.M. et al. Olfactory sensory map is perturbed in a human wild-type α-synuclein overexpressing transgenic mouse model of Parkinson’s disease. npj Parkinsons Dis. 12, 70 (2026). https://doi.org/10.1038/s41531-026-01288-w
Parole chiave: malattia di Parkinson, disfunzione olfattiva, alfa-sinucleina, mappa sensoriale, biomarcatori