Clear Sky Science · it
La mutazione LRRK2R1627P amplifica i fattori di rischio ambientali che inducono infiammazione cronica e aggregazione di α-sinucleina nell’intestino dei ratti
Perché l’intestino conta in una malattia del cervello
La malattia di Parkinson è più nota per i tremori e i problemi di movimento, ma crescenti evidenze suggeriscono che le sue radici possano iniziare lontano dal cervello, nel profondo dell’intestino. Questo studio esplora come una specifica modificazione genetica collegata al Parkinson nelle popolazioni asiatiche possa, insieme all’invecchiamento e all’esposizione a tossine, danneggiare gradualmente l’intestino nei ratti. Seguendo ciò che accade nell’intestino nel corso della vita degli animali, i ricercatori tracciano come le difese immunitarie quotidiane possano scivolare verso un’infiammazione cronica, predisponendo all’accumulo di proteine legate alla malattia che potrebbero infine minacciare il cervello.
Un gene a rischio nel tratto digestivo
Gli scienziati si sono concentrati su una variante di un gene chiamato LRRK2, da tempo associato alla malattia di Parkinson e ad alcune condizioni infiammatorie intestinali. Hanno creato ratti portatori della mutazione analoga, denominata LRRK2R1627P, e li hanno confrontati con ratti normali nel corso della vita. Pur non essendosi modificata la quantità di trascritti del gene LRRK2 nell’intestino, la proteina LRRK2 totale e uno dei suoi marcatori di attività sono risultati ridotti, indicando che la mutazione indebolisce la funzione normale di questa proteina nell’intestino. Questo cambiamento molecolare sottile non ha provocato danni precoci evidenti, ma ha alterato discretamente il modo in cui le cellule intestinali si rinnovano e si organizzano con l’età.
Un intestino invecchiato sotto stress lento e persistente
Con il passare dei mesi, i ratti portatori della mutazione hanno sviluppato chiari segni di alterazione della struttura intestinale. Il loro intestino tenue si è accorciato e i sottili villi e le cripte che assorbono i nutrienti sono risultati più piccoli. Alcune cellule specializzate della mucosa che producono muco protettivo e sostanze antimicrobiche—le cellule caliciformi e le cellule di Paneth—sono diminuite, mentre sono calate anche le proteine che consentono alle cellule adiacenti di formare giunzioni strette e resistenti alle perdite. Al microscopio, queste giunzioni sono apparse più corte o più larghe, suggerendo una barriera indebolita. È importante sottolineare che l’architettura complessiva non è collassata; piuttosto, l’intestino ha mostrato un modello più insidioso di ridotto rinnovamento e protezione, che lo rende più vulnerabile a irritazioni e infezioni. 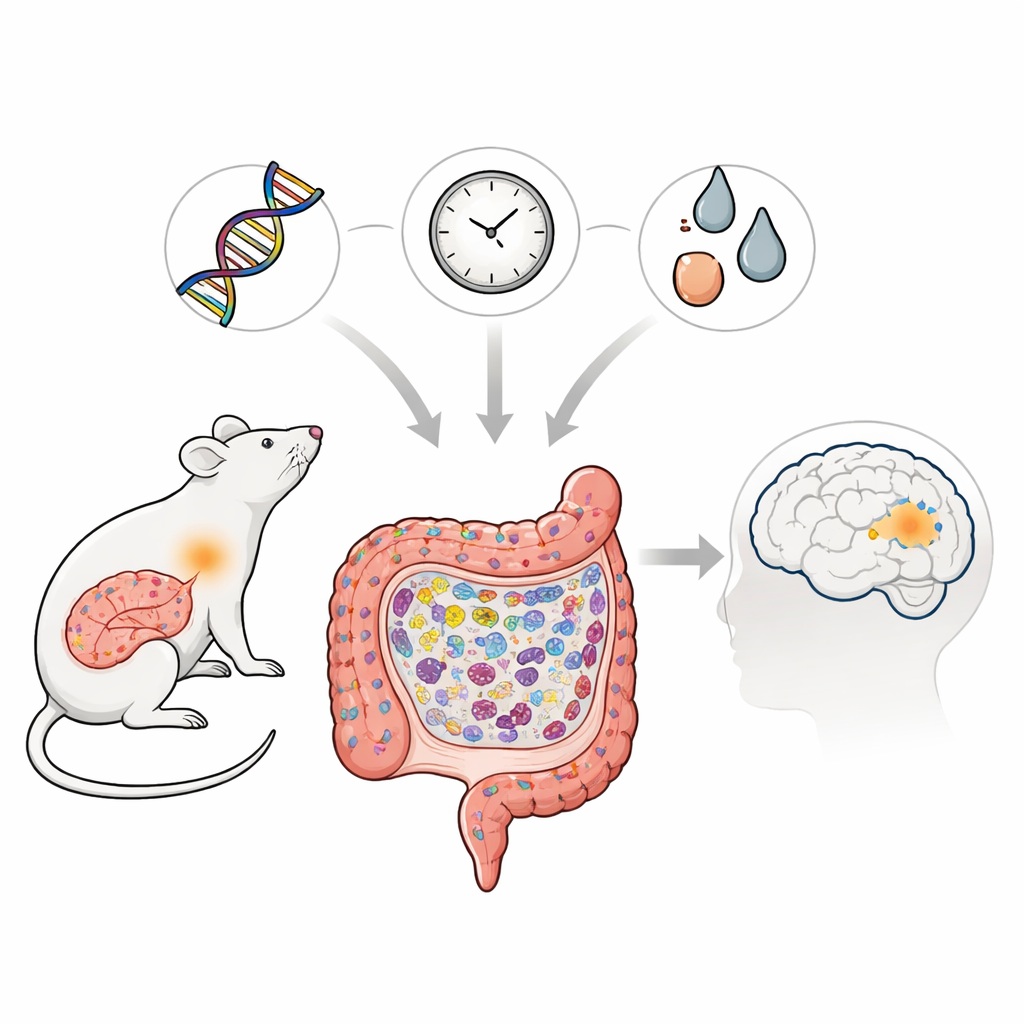
Sistema immunitario con il grilletto facile
Per capire perché l’intestino stesse perdendo l’equilibrio, il gruppo ha esaminato l’attività genica e le cellule immunitarie nella parete intestinale. Hanno riscontrato che le vie legate a un sensore chiamato TLR4 e al suo coadiuvante NF-κB erano iperattive nei ratti anziani mutanti. Questi sensori normalmente aiutano l’organismo a rilevare microrganismi dannosi, ma qui hanno guidato un accumulo di cellule immunitarie “da combattimento” note come macrofagi M1. Queste cellule secernono molecole infiammatorie, trasformando l’intestino in un ambiente cronicamente irritato. Colpisce il fatto che la proteina legata al Parkinson, α-sinucleina, nella sua forma fosforilata associata alla malattia, ha cominciato ad accumularsi non nei neuroni intestinali ma all’interno di questi macrofagi attivati nel piccolo intestino, soprattutto negli animali più anziani.
Più sensibili agli insulti ambientali
La mutazione genetica da sola non era tutta la storia. Quando ratti giovani sono stati brevemente esposti a tossine batteriche (LPS), che stimolano TLR4, gli animali con la mutazione LRRK2 hanno sviluppato un’infiammazione intestinale molto più grave rispetto ai controlli normali. Il loro rivestimento intestinale ha perso più cellule, le proteine di barriera sono scese ulteriormente e i macrofagi pro-infiammatori sono aumentati, accumulando ancora una volta α-sinucleina anomala. Questo suggerisce che persone portatrici di mutazioni simili potrebbero essere particolarmente sensibili a insulti ambientali che disturbano l’intestino, come alcune infezioni o tossine, amplificando il loro rischio a lungo termine.
Abbassare il segnale d’allarme
Poiché TLR4 stava al centro di questa tempesta infiammatoria, il gruppo ha testato un farmaco, TAK-242, che smorza specificamente la segnalazione di TLR4. Somministrato per diversi mesi a ratti di mezza età, l’inibitore ha in gran parte ristabilito la lunghezza del tenue, la dimensione di villi e cripte, le cellule produttrici di muco e le proteine di barriera. Ha ridotto i macrofagi iperattivi, abbassato le molecole infiammatorie e drasticamente ridotto l’accumulo di α-sinucleina anomala nell’intestino. Contemporaneamente ha corretto una comunità microbica alterata: la diversità è aumentata, un eccesso di Lactobacillus è diminuito e diversi gruppi batterici benefici sono ripartiti, mentre le funzioni microbiche previste si sono spostate lontano da schemi associati alla malattia. 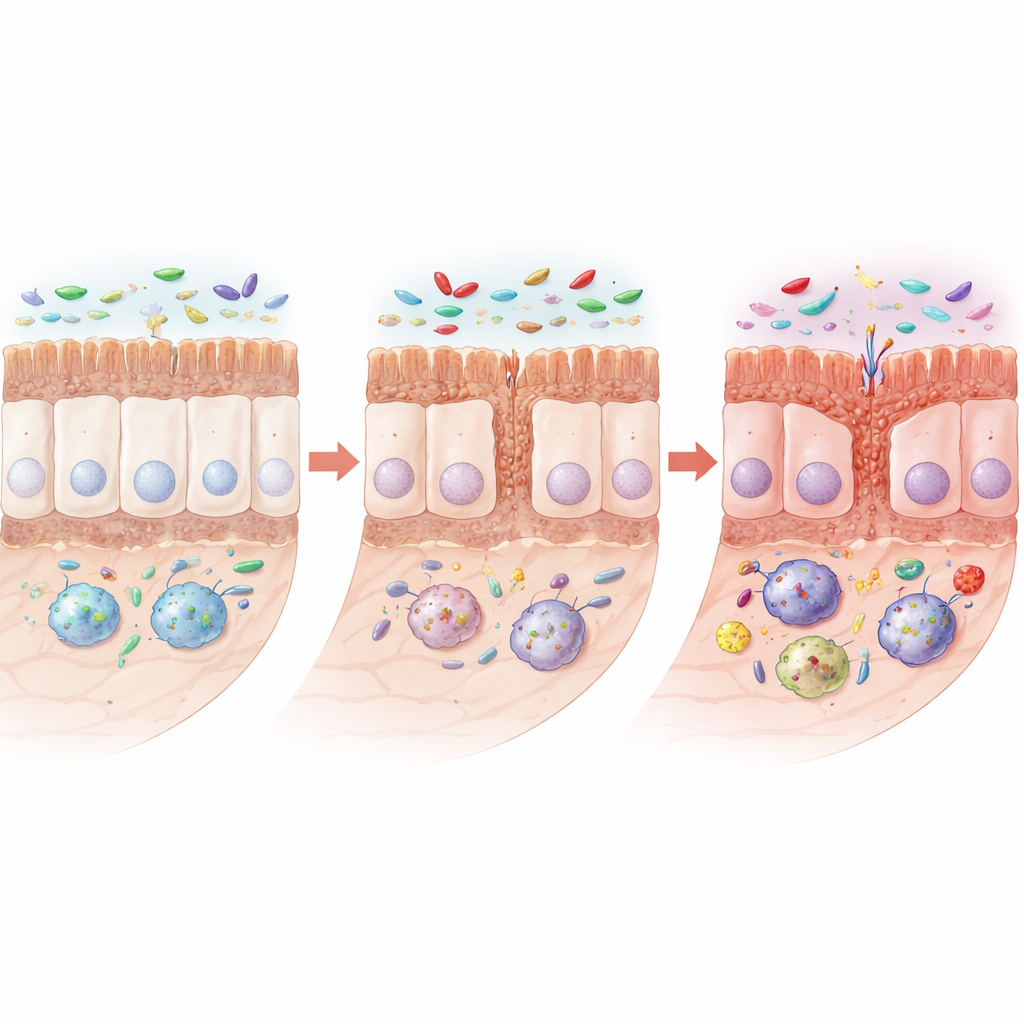
Cosa significa per il rischio di Parkinson
Per un non specialista, il messaggio è che un “gene del Parkinson” può rimodellare silenziosamente le difese immunitarie intestinali nel tempo, soprattutto in presenza di invecchiamento e stress ambientale. In questi ratti, il risultato è un’infiammazione cronica e di basso grado che indebolisce la barriera intestinale, altera i microbi residenti e causa l’accumulo di proteina legata al Parkinson nelle cellule immunitarie—non ancora un Parkinson conclamato, ma un contesto biologico che potrebbe favorire una successiva malattia cerebrale. Dimostrando che bloccare una singola via immunitaria intestinale può invertire molte di queste alterazioni, lo studio evidenzia l’intestino come un target precoce praticabile: proteggere la salute intestinale e controllare l’infiammazione potrebbe aiutare a ritardare o prevenire il Parkinson in persone con rischi genetici.
Citazione: Pang, S., Lu, J., Wang, Y. et al. LRRK2R1627P mutation amplifies environmental risk factors induced chronic inflammation and α-synuclein aggregation in the gut of rats. npj Parkinsons Dis. 12, 68 (2026). https://doi.org/10.1038/s41531-026-01281-3
Parole chiave: Malattia di Parkinson, infiammazione intestinale, mutazione LRRK2, microbioma, immunità innata