Clear Sky Science · it
Fenotipizzazione neurocomportamentale profonda svela impronte neurali dei deficit locomotori nella malattia di Parkinson
Perché i problemi di camminata nel Parkinson sono importanti
Per molte persone con la malattia di Parkinson, uno dei sintomi più spaventosi è quando i piedi sembrano improvvisamente incollati al suolo, o la camminata rallenta fino a quasi fermarsi. Questi cedimenti del movimento, dalla lieve lentezza al completo "freezing" della marcia, aumentano notevolmente il rischio di cadute e la perdita di autonomia, eppure i farmaci e la stimolazione cerebrale attuali spesso non riescono a prevenirli. Questo studio si è proposto di scoprire i pattern cerebrali nascosti che accompagnano tali problemi di camminata, con l’obiettivo a lungo termine di progettare terapie più intelligenti e on‑demand.
Osservare il movimento nei minimi dettagli
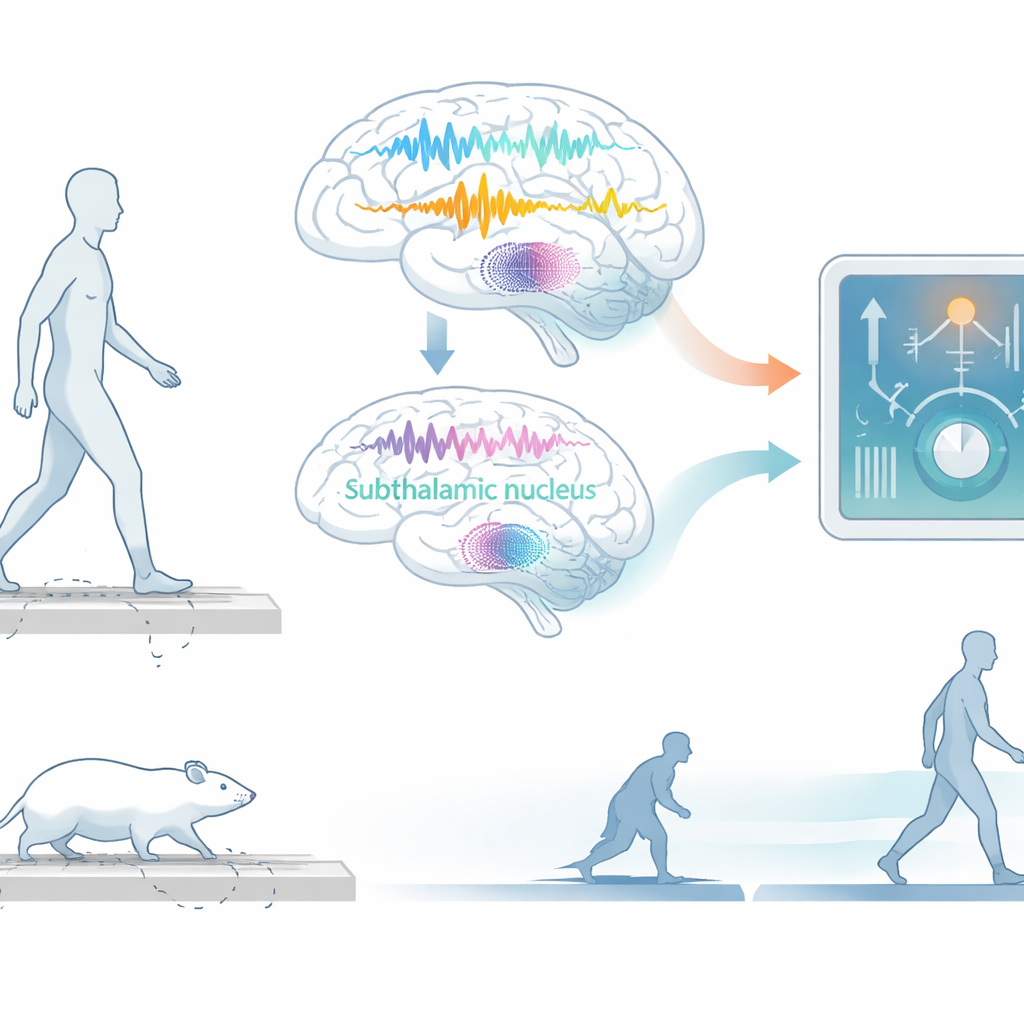
I ricercatori hanno iniziato con un modello ben consolidato di Parkinson nel ratto. Hanno addestrato i ratti a percorrere avanti e indietro una passerella monitorando ogni piccolo movimento delle zampe posteriori in tre dimensioni e registrando l’attività elettrica nelle aree cerebrali del movimento. Ogni istante di comportamento è stato etichettato come uno dei tre stati: camminata normale, piccoli movimenti intenzionali sul posto, o acinesia—un arresto quasi completo del movimento che somiglia agli episodi di freezing osservati nei pazienti. Questo ha creato un ricco dataset “neurocomportamentale” che ha allineato i ritmi cerebrali a ciò che il corpo faceva da un istante all’altro.
Trovare pattern nelle onde cerebrali
Per interpretare questi dati ad alta dimensionalità, il team ha applicato sia statistiche classiche sia strumenti moderni di deep learning. Hanno prima confermato firme note: i ratti con danno di tipo Parkinson trascorrevano più tempo in acinesia rispetto agli animali sani, e i loro segnali cerebrali mostravano maggiore attività in una banda di frequenza associata a ritmi beta anomali e low gamma. Ma quando gli scienziati hanno chiesto quali caratteristiche distinguessero meglio i tre stati di movimento, sono emersi nuovi indicatori. Misure chiamate complessità di Hjorth e mobilità di Hjorth—sintesi nel dominio del tempo di quanto irregolare e di quanto rapidamente cambia il segnale—si sono rivelate marcatori potenti. Nell’emisfero colpito, maggiore complessità e minore mobilità erano strettamente legate all’insorgenza dell’acinesia, mentre altre caratteristiche, come la potenza gamma ad alta frequenza, tracciavano il movimento attivo.
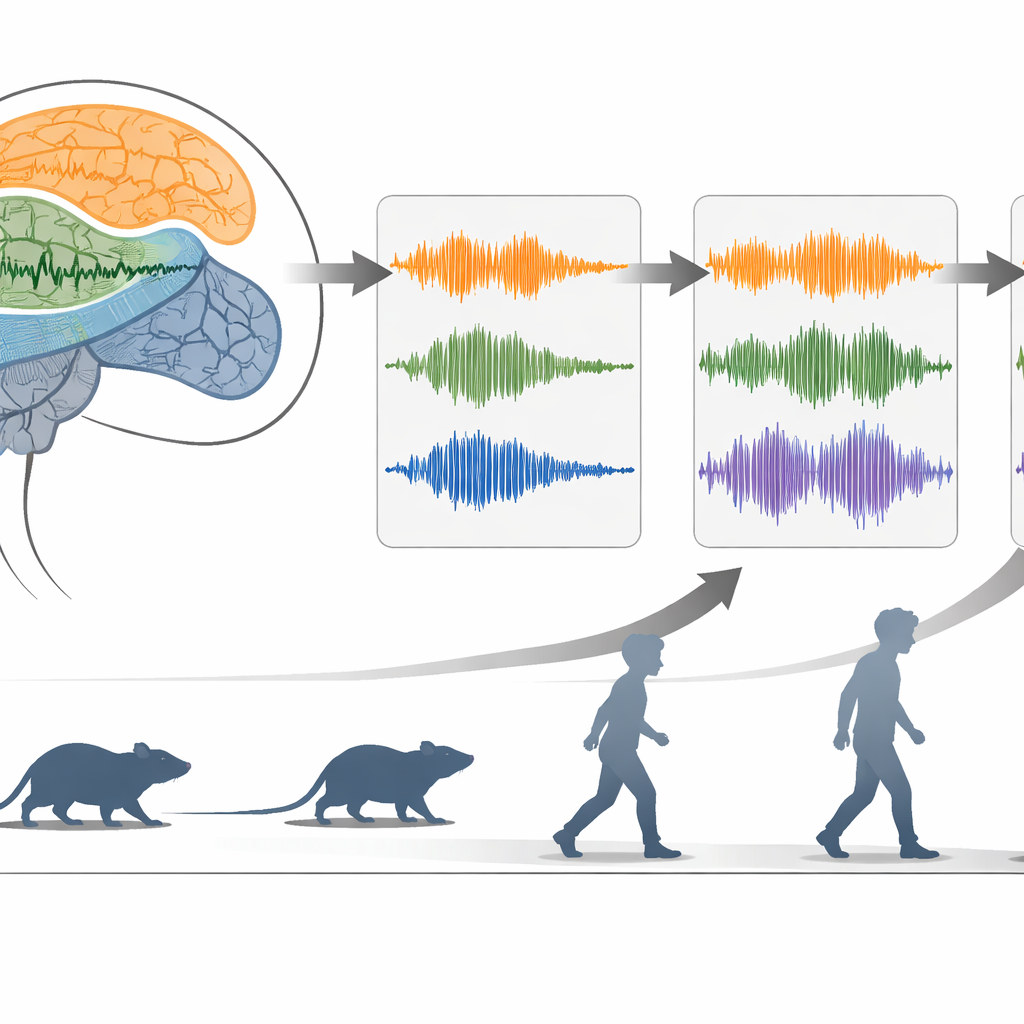
Zoom sul momento in cui il movimento si ferma
Utilizzando reti neurali che apprendono “mappe” compatte dei dati, i ricercatori sono stati in grado di collocare ogni breve finestra temporale in uno spazio a bassa dimensionalità dove camminata, movimento stazionario e acinesia occupavano regioni distinte. In questo spazio, le misure di Hjorth e la banda beta–low gamma anomala hanno fortemente determinato dove ricadevano gli episodi acinetici. Quando il team si è concentrato sui secondi attorno all’inizio di un episodio acinetico, ha osservato una sequenza coerente: complessità e potenza simile alla beta aumentavano poco prima e al momento dell’arresto, mentre mobilità e potenza gamma diminuivano. È cruciale che queste misure possano essere calcolate rapidamente senza un’analisi spettrale pesante, rendendole candidate attraenti per il monitoraggio in tempo reale.
Dai ratti alle persone con freezing della marcia
Il gruppo ha poi verificato se impronte neurali simili compaiono negli esseri umani. Hanno analizzato filmati di motion capture dettagliati e registrazioni da elettrodi impiantati in una struttura cerebrale profonda, il nucleo subtalamico, in due persone con Parkinson che sperimentavano freezing della marcia. In un partecipante è emerso lo stesso pattern osservato nei ratti durante gli episodi di freezing: aumento della complessità di Hjorth e della potenza beta, insieme a una diminuzione della mobilità di Hjorth. Sebbene la gamma si sia comportata in modo leggermente diverso tra le specie, il segnale centrale che indicava lo scivolamento del movimento verso uno stato patologico risultava sorprendentemente simile nella corteccia dei ratti e nel nucleo subtalamico di questo paziente, suggerendo un meccanismo sottostante condiviso attraverso la rete motoria.
Cosa potrebbe significare per le terapie future
Fusando il tracciamento del movimento dettagliato con l’analisi avanzata dei ritmi cerebrali, questo lavoro identifica “impronte” semplici e computazionalmente leggere che segnalano quando la camminata nel Parkinson sta per crollare. Per un pubblico non specialistico, ciò significa che medici e ingegneri potrebbero presto costruire stimolatori cerebrali in grado di riconoscere queste impronte in tempo reale e intervenire solo quando necessario, spingendo il sistema lontano da un episodio di freezing prima che si stabilizzi. Pur richiedendo studi umani più ampi, l’approccio apre una strada promettente verso trattamenti personalizzati e a circuito chiuso per i problemi di marcia invalidanti nella malattia di Parkinson.
Citazione: Garulli, E.L., Merk, T., El Hasbani, G. et al. Deep neurobehavioral phenotyping uncovers neural fingerprints of locomotor deficits in Parkinson’s disease. npj Parkinsons Dis. 12, 65 (2026). https://doi.org/10.1038/s41531-026-01280-4
Parole chiave: malattia di Parkinson, freezing della marcia, ritmi cerebrali, stimolazione cerebrale profonda, fenotipizzazione neurocomportamentale