Clear Sky Science · it
Utilità clinica dei potenziali evocati per la programmazione della stimolazione profonda del cervello nel nucleo subtalamico nella malattia di Parkinson
Perché questa storia del pacemaker cerebrale è importante
Per molte persone con malattia di Parkinson, i farmaci alla fine smettono di funzionare in modo stabile. Possono alternarsi tra rigidità e movimenti incontrollati, e mettere a punto il trattamento diventa un ciclo frustrante di visite cliniche. Questo articolo di revisione esamina come i medici possano usare gli echi elettrici del cervello—chiamati potenziali evocati—per programmare la stimolazione cerebrale profonda (DBS) in modo più rapido e oggettivo. In sostanza, si chiede se sia possibile trasformare la programmazione della DBS da una congettura attenta a un approccio più guidato dai dati e personalizzato, un vero e proprio pacemaker cerebrale su misura.
Dal metodo di tentativi all’ottimizzazione guidata
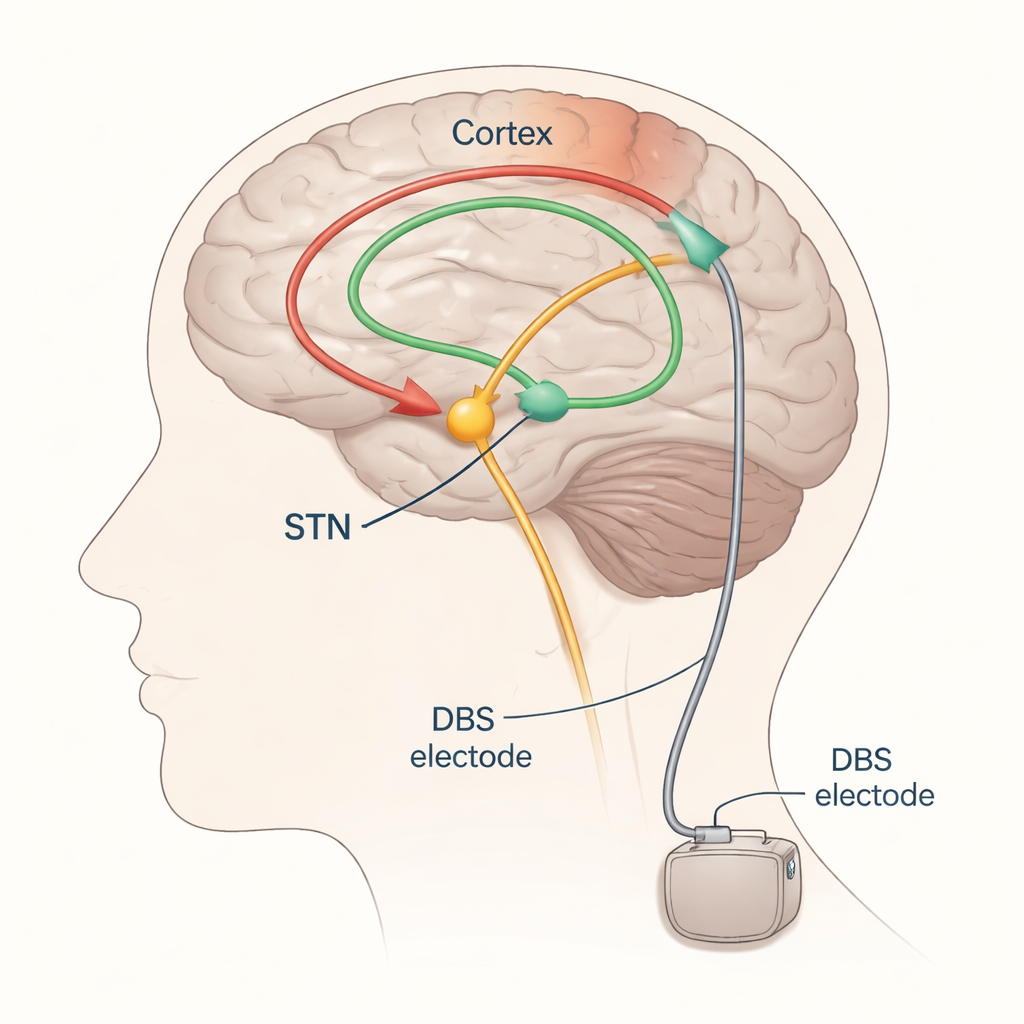
La DBS per il Parkinson mira più spesso a una piccola struttura profonda del cervello chiamata nucleo subtalamico (STN). In questo punto vengono impiantati gli elettrodi e collegati a un generatore di impulsi sotto la pelle nel torace. Quando è ben regolata, la DBS del STN può attenuare tremore, lentezza e rigidità, ma se il campo elettrico si estende troppo può stimolare involontariamente vie vicine che controllano muscoli o sensibilità, causando effetti collaterali come contrazioni muscolari o formicolio. Oggi i neurologi solitamente regolano la DBS modificando lentamente i parametri e osservando i movimenti e gli effetti collaterali del paziente—un approccio che richiede tempo, dipende da come il paziente si sente in quel giorno e spesso richiede diverse visite di controllo.
Ascoltare gli echi elettrici del cervello
Gli autori si concentrano sui potenziali evocati—risposte elettriche minime e temporizzate nel cervello o nei muscoli dopo uno stimolo—come possibili indicatori di impostazioni di DBS buone o dannose. Quando lo STN viene stimolato, onde di attività viaggiano lungo vie nervose e possono essere rilevate sul cuoio capelluto con EEG, nell’attività muscolare con EMG o talvolta con strisce di registrazione poste direttamente sulla superficie cerebrale. Stimolando ripetutamente a basse frequenze e mediando le risposte, i ricercatori possono vedere in modo affidabile onde distinte che compaiono a diversi ritardi (millisecondi) dopo ogni impulso. Onde precoci, che arrivano entro circa due millesimi di secondo, riflettono principalmente l’attivazione di vie motorie rapide vicine all’elettrodo. Onde leggermente più tardive, intorno ai tre millisecondi (spesso chiamate componente “P3”), si pensa derivino da un collegamento diretto tra la corteccia frontale e lo STN noto come via iperdiretta. Onde ancora più tardive probabilmente percorrono circuiti più lunghi e ricorsivi che includono il talamo e altri nuclei profondi.
Trovare il punto ottimale ed evitare problemi
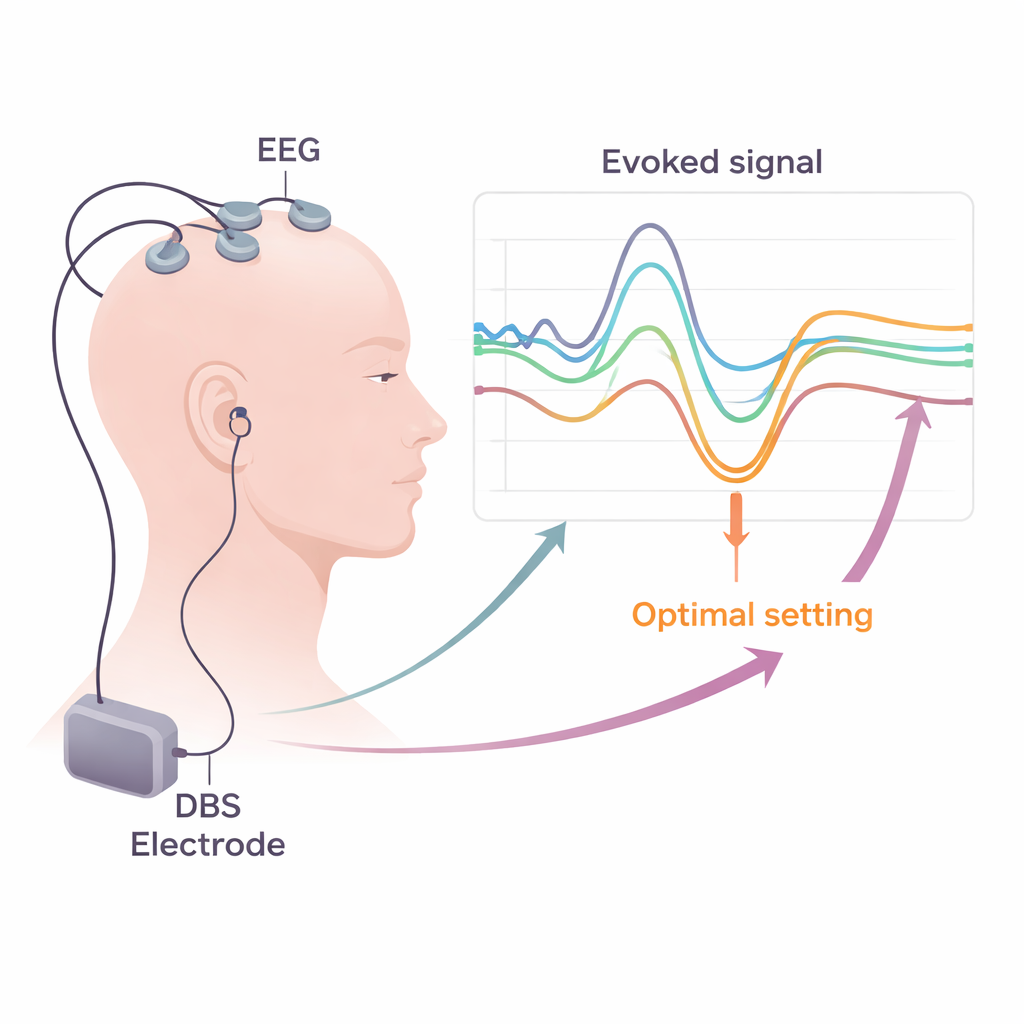
In molti studi emerge un quadro coerente: i contatti sul filo di DBS che producono una forte componente P3 a latenza breve tendono a trovarsi nella parte più utile dello STN e sono associati a un miglioramento maggiore dei sintomi motori parkinsoniani e a una “finestra terapeutica” più ampia prima della comparsa di effetti collaterali. Al contrario, onde molto precoci legate alle vie motorie e certe risposte intorno a 8–10 millisecondi spesso indicano che la stimolazione si sta estendendo in strutture limitrofe, aumentando il rischio di contrazioni muscolari o altri effetti indesiderati. Misurazioni separate dei potenziali motori evocati (risposte EMG nei muscoli del viso e degli arti) e dei potenziali evocati somatosensoriali (pattern EEG legati alle vie tattili) possono rivelare attivazione sottile della capsula interna o del lemnisco mediale—fasci di fibre che trasportano comandi motori e informazioni sensoriali. Rilevare questi cambiamenti precocemente consente ai clinici di deviare la corrente da aree a rischio scegliendo contatti diversi o regolando la forma e la polarità dell’impulso.
Rendere gli strumenti di laboratorio pratici in clinica
Trasformare queste intuizioni in pratica clinica richiede soluzioni pratiche. La revisione spiega come i sistemi EEG e EMG standard ospedalieri possano già registrare la maggior parte dei segnali necessari, a patto che impieghino frequenze di campionamento elevate e metodi accurati per rimuovere il “rumore” elettrico degli impulsi DBS. Gli autori discutono strategie per ridurre gli artefatti, come un ricollegamento intelligente dei riferimenti, la sottrazione di template e algoritmi informatici avanzati che separano la vera attività cerebrale dai residui di stimolazione. Sostengono che brevi sessioni di test strutturate—combinando periodi rapidi di DBS a bassa frequenza, registrazioni sul cuoio capelluto e monitoraggio muscolare durante il riposo e leggere contrazioni—potrebbero essere integrate nella consueta settimana di programmazione post-chirurgica. Mappe di potenziali evocati per ciascun contatto potrebbero quindi essere combinate con imaging e altri biomarcatori per guidare la scelta dei contatti e dei parametri da usare a lungo termine.
Cosa significa questo per le persone con Parkinson
L’articolo conclude che i potenziali evocati sono candidati promettenti per rendere la programmazione della DBS più precisa, efficiente e prevedibile. In particolare, l’onda P3 a latenza breve sembra essere un forte marcatore che la stimolazione sta colpendo il circuito giusto per alleviare i sintomi motori del Parkinson, mentre le risposte evocative motorie e sensoriali possono avvertire quando la corrente fuoriesce in vie che causano effetti collaterali. Sebbene siano necessari ulteriori studi per standardizzare le tecniche e dimostrare benefici nella pratica quotidiana, questo approccio punta a un futuro in cui i medici possono “ascoltare” il cervello durante la programmazione, individuare rapidamente il punto ottimale per ciascun paziente e ridurre il carico del metodo per tentativi per le persone che vivono con la malattia di Parkinson.
Citazione: Hale, B., Latorre, A., Rocchi, L. et al. Clinical utility of evoked potentials for programming subthalamic deep brain stimulation in Parkinsons disease. npj Parkinsons Dis. 12, 54 (2026). https://doi.org/10.1038/s41531-026-01274-2
Parole chiave: Malattia di Parkinson, stimolazione cerebrale profonda, potenziali evocati, mappatura cerebrale, neurofisiologia