Clear Sky Science · it
Decodificare l’impatto degli stati visivi sui segnali di feedback della stimolazione cerebrale profonda adattiva nei disturbi del movimento
Perché chiudere gli occhi conta per gli impianti cerebrali
Per le persone che vivono con il morbo di Parkinson o la distonia, la stimolazione cerebrale profonda (DBS) può funzionare come un pacemaker per circuiti cerebrali che funzionano male. I sistemi DBS “adattivi” più recenti promettono di regolare automaticamente la stimolazione in tempo reale ascoltando i segnali cerebrali. Questo studio mostra che qualcosa di semplice e normale come chiudere gli occhi può cambiare fortemente quei segnali, il che significa che i futuri impianti cerebrali devono prima comprendere lo stato della persona prima di decidere come stimolare.
Pacemaker cerebrali che imparano e si adattano
La DBS tradizionale eroga impulsi elettrici costanti nelle aree cerebrali profonde a tutte le ore. Sebbene questo possa alleviare sintomi come tremore e rigidità, può anche sprecare batteria e talvolta causare effetti collaterali, perché la stimolazione non cambia quando cambia la condizione del paziente. La DBS adattiva mira a risolvere questo problema aumentando o diminuendo la corrente in base ai «potenziali di campo locali», piccole tensioni ritmiche registrate dagli stessi elettrodi che forniscono la terapia. Questi ritmi sono più forti in strutture chiamate nucleo subtalamico (STN) e globo pallido interno (GPi), snodi chiave nella rete del movimento. 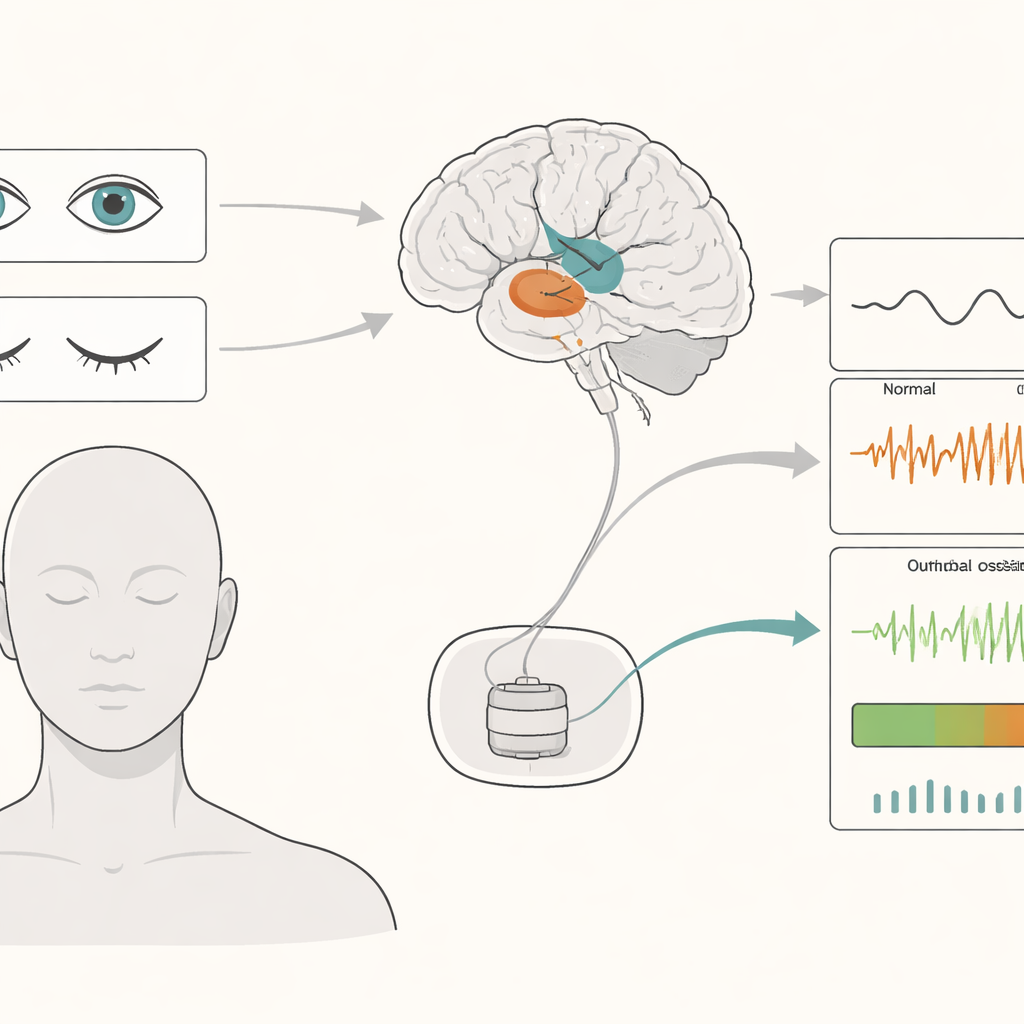
Quando la vista riposa, gli ritmi cerebrali profondi cambiano
I ricercatori hanno seguito 36 pazienti — 18 con morbo di Parkinson e 18 con distonia — nei giorni successivi all’intervento di DBS. Hanno registrato l’attività cerebrale dagli elettrodi nello STN o nel GPi e dal cuoio capelluto mentre i pazienti riposavano con gli occhi aperti, chiusi o addormentati. Chiudere gli occhi aumentava in modo coerente i ritmi lenti nel cervello profondo, soprattutto nelle bande theta e alfa, che sono proprio i segnali che molti sistemi DBS adattivi monitorano. Questo aumento era più pronunciato nello STN, che è strettamente connesso alla superficie corticale «pensante» del cervello, e meno marcato nel GPi. Il sonno mostrava invece un profilo differente, con onde molto lente particolarmente forti.
Disturbi diversi, impronte di segnale diverse
Il morbo di Parkinson e la distonia possiedono già «impronte» ritmiche distinte, e lo studio ha constatato che la chiusura degli occhi modificava queste impronte in modi leggermente differenti. In entrambi i disturbi, la potenza a bassa frequenza e nella banda alfa diminuiva quando i pazienti riaprivano gli occhi. Ma nel Parkinson compariva una diminuzione aggiuntiva della potenza theta che non si osservava nella distonia. Di conseguenza, una volta aperti gli occhi, le persone con distonia mantenevano più attività theta rispetto a quelle con Parkinson. Questo sottolinea che lo stesso segnale cerebrale profondo può riflettere sia la malattia sia cambiamenti ordinari nello stato di vigilanza, rendendo rischioso trattare qualsiasi singolo ritmo come un semplice marcatore on–off dei sintomi.
Le reti cerebrali comunicano di più quando gli occhi sono chiusi
Oltre alla forza dei ritmi stessi, il team ha esaminato anche quanto strettamente le strutture profonde e la corteccia si muovono in sincronia. Utilizzando un metodo che si concentra sulla comunicazione genuina piuttosto che sul semplice rumore condiviso, hanno trovato che chiudere gli occhi aumentava l’attività coordinata a bassa frequenza e alfa tra lo STN e le regioni centrali del cuoio capelluto sopra la corteccia sensomotoria. Anche il GPi mostrava un accoppiamento alfa più forte con la corteccia a occhi chiusi, seppure in modo più modesto e senza chiare differenze regionali. Questi risultati suggeriscono che riposare con gli occhi chiusi cambia non solo l’attività locale ma i modelli di comunicazione più ampi della rete del movimento.
Insegnare alle macchine a riconoscere gli stati interni
Poiché i futuri impianti probabilmente useranno algoritmi per leggere i segnali cerebrali, i ricercatori hanno testato se modelli di apprendimento automatico semplici potessero distinguere occhi aperti da occhi chiusi basandosi solo su questi ritmi. Alimentando i classificatori con più bande di frequenza, sono riusciti a identificare lo stato degli occhi con circa l’88 percento di accuratezza usando i segnali STN e il 77 percento usando i segnali GPi, sia nel Parkinson che nella distonia. I modelli non lineari, in grado di catturare schemi più complessi, hanno reso ancora meglio, e il miglior decoding proveniva dalle regioni sensomotorie più direttamente collegate al movimento. 
Verso una stimolazione cerebrale più intelligente e consapevole del contesto
In termini semplici, lo studio mostra che cambiamenti ordinari e sani nel livello di veglia o nel coinvolgimento visivo di una persona possono alterare fortemente le onde cerebrali su cui si basano i sistemi DBS adattivi. Se un impianto reagisse semplicemente ogni volta che un ritmo supera una soglia fissa, potrebbe interpretare erroneamente cambiamenti di stato normali come ricadute di malattia e stimolare troppo o troppo poco. Gli autori sostengono che la prossima generazione di DBS dovrebbe prima rilevare il contesto della persona — come occhi aperti vs chiusi, sonno vs veglia — e poi interpretare i segnali di malattia in modo differente a seconda di quello stato. Tali pacemaker cerebrali «consapevoli dello stato» potrebbero fornire un aiuto più preciso, evitare stimolazioni non necessarie e sostenere meglio le persone con disturbi del movimento nello svolgimento della vita quotidiana.
Citazione: Zhu, GY., Merk, T., Butenko, K. et al. Decoding the impact of visual states on adaptive deep brain stimulation feedback signals in movement disorders. npj Parkinsons Dis. 12, 61 (2026). https://doi.org/10.1038/s41531-026-01273-3
Parole chiave: stimolazione cerebrale profonda adattiva, morbo di Parkinson, distrofia, oscillazioni cerebrali, interfacce cervello–computer