Clear Sky Science · it
Disfunzione sinaptica retinica precoce e rimodellamento proteomico precedono la neurodegenerazione in un modello di malattia di Parkinson
Perché il tuo occhio potrebbe rivelare i primi segnali del Parkinson
La malattia di Parkinson è nota soprattutto per causare tremori e problemi motori, ma molto prima che questi sintomi si manifestino pienamente, potrebbero verificarsi cambiamenti sottili nell’occhio. Poiché la retina è, in sostanza, una propaggine del cervello osservabile in modo non invasivo, gli scienziati si chiedono se possa funzionare da finestra sulle fasi iniziali della malattia cerebrale. Questo studio in un modello murino del Parkinson mostra che il cablaggio retinico e il profilo proteico cominciano a mutare ben prima della perdita evidente dei neuroni, suggerendo che semplici test oculari potrebbero un giorno aiutare a rilevare il Parkinson in fase precoce e a monitorarne la progressione.
Guardare all’occhio per segnali di allarme precoci
I ricercatori hanno lavorato con topi ingegnerizzati per sovraprodurre una forma mutante di alfa-sinucleina, la proteina chiave che si aggrega nei cervelli delle persone con Parkinson. Hanno esaminato gli animali in una fase di giovane età adulta (sei mesi) e in una fase più avanzata (sedici mesi), combinando immagini oculari, test elettrici della funzione retinica e misurazioni proteomiche su larga scala. La domanda centrale era semplice: compaiono cambiamenti retinici misurabili prima che un gran numero di cellule nervose retiniche muoia, e se sì, quali cambiamenti molecolari li accompagnano?
Cambiamenti strutturali ed elettrici sottili nella retina
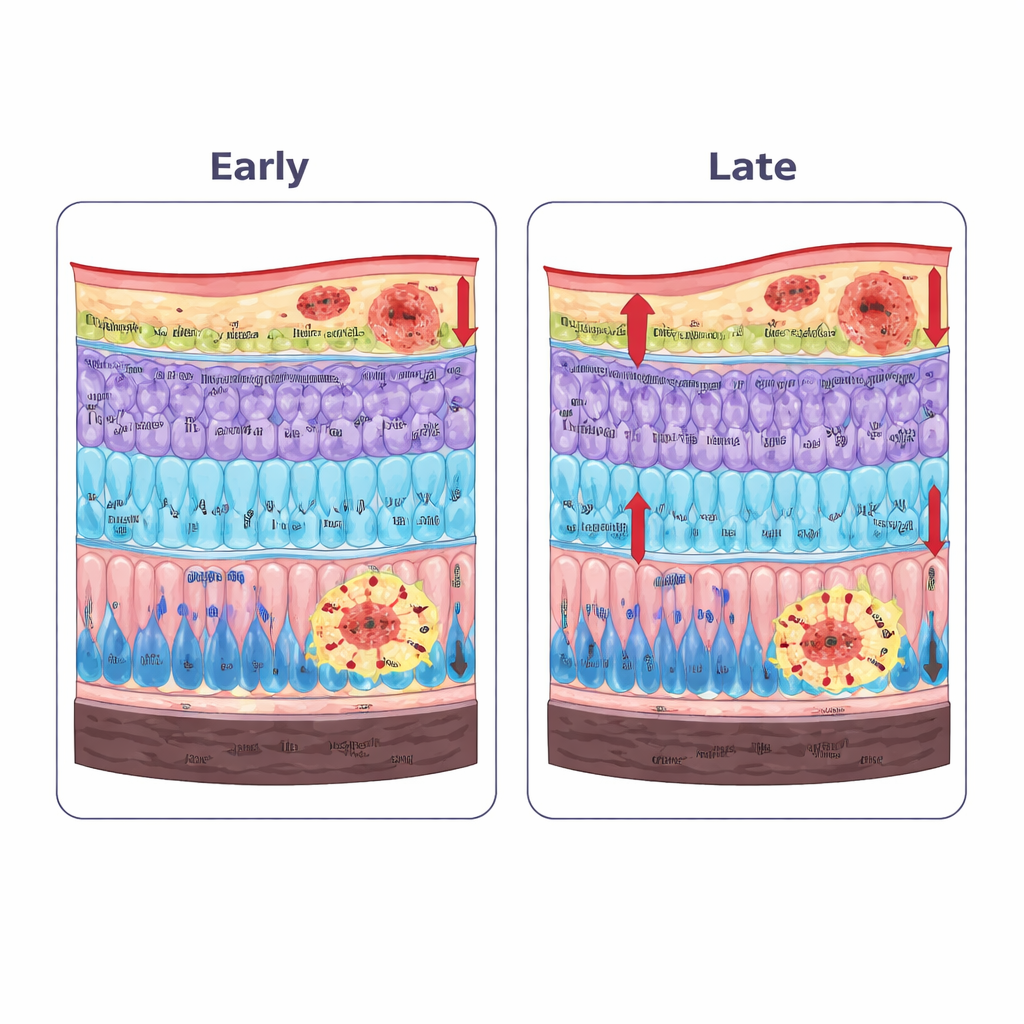
Scansioni oculari ad alta risoluzione, simili per principio a quelle già impiegate nelle cliniche oftalmologiche, hanno rivelato che specifici strati retinici modificavano lo spessore nei topi affetti dal Parkinson. Lo strato contenente le fibre nervose e le cellule gangliari (che inviano i segnali visivi al cervello) e lo strato dei fotorecettori sensibili alla luce erano già più sottili a sei mesi e si assottigliavano ulteriormente con l’età. Al contrario, lo strato plexiforme interno — dove molti neuroni retinici scambiano segnali — si è inspessito, un quadro coerente con edema e rimodellamento guidati dall’infiammazione piuttosto che con una semplice perdita cellulare. Le registrazioni elettriche dalla retina hanno mostrato che, nelle fasi iniziali, piccole oscillazioni legate ai circuiti locali di “interneuron” risultavano ridotte anche quando le onde principali apparivano quasi normali. A sedici mesi, sia le risposte mediate da bastoncelli che da coni erano chiaramente compromesse e l’attività correlata alle cellule gangliari di uscita era diminuita, rispecchiando i cambiamenti strutturali precedenti.
Accumulo proteico precoce e cellule di supporto sotto stress
La colorazione microscopica del tessuto retinico ha mostrato che l’alfa-sinucleina mutante non rimaneva confinata al cervello. La sua forma fosforilata, soggetta ad aggregazione, si accumulava nello strato plexiforme esterno, dove i fotorecettori si connettono alle cellule a valle. Allo stesso tempo, le cellule di supporto nella retina diventavano reattive. Un aumento precoce di una proteina strutturale chiamata GFAP è stato osservato principalmente negli astrociti vicino alla superficie interna della retina e, nella fase più avanzata, lunghi processi GFAP-positivi delle cellule di Müller attraversavano più strati — segni distintivi di stress cronico e infiammazione. Pur mantenendo in larga misura numeri e morfologia di base degli interneuroni chiave, le strutture specializzate a “nastro” nelle sinapsi dei fotorecettori, marcate dalla proteina CtBP2, erano già ridotte a sei mesi e diminuivano ulteriormente con l’età, indicando un deterioramento precoce dei punti di comunicazione tra le cellule.
Un paesaggio molecolare in evoluzione all’interno dell’occhio
Per comprendere questi cambiamenti a livello di sistema, il gruppo ha catalogato oltre 4.000 proteine retiniche e ha confrontato i topi con Parkinson e quelli normali a entrambe le età. I profili proteici complessivi si separavano nettamente in base allo stato di malattia, indicando che i processi legati al Parkinson plasmavano il proteoma retinico più fortemente dell’invecchiamento normale. L’alfa-sinucleina stessa era più abbondante in entrambe le fasi, confermando la colorazione tissutale. Proteine implicate nella gestione dello stress ossidativo, come alcune molecole leganti calcio e metalli, risultavano costantemente elevate, suggerendo una reazione persistente a specie reattive dannose. Altre proteine associate all’impalcatura cellulare e alle funzioni di chaperone protettive — in particolare membri della famiglia delle cristalline — mostravano spostamenti dipendenti dallo stadio: alcune aumentavano precocemente per poi calare, mentre altre salivano più tardi, implicando un tentativo iniziale di compensazione che cede il passo a un rimodellamento più ampio con l’avanzare della malattia. Le analisi di rete hanno evidenziato le cristalline e i componenti del citoscheletro come nodi centrali in questa mappa di interazioni proteiche in evoluzione.
Cosa significa per le persone che convivono con il Parkinson
Nel complesso, i risultati supportano un’idea semplice per i non specialisti: in questo modello di Parkinson, la retina comincia a malfunzionare e a rimodellarsi molto prima che un gran numero di neuroni venga perso. Aggregati proteici, infiammazione e risposte di stress alterano inizialmente le sinapsi — i minuscoli punti di contatto tra le cellule — soprattutto dove i fotorecettori trasmettono segnali. Questi cambiamenti precoci modificano il modo in cui la retina elabora le informazioni visive e alla fine portano a problemi visivi misurabili. Poiché imaging oculare e test elettrici simili sono già in uso clinico e la retina è relativamente accessibile per il campionamento, questo lavoro rafforza l’ipotesi di sviluppare misure retiniche come segnali d’allarme precoci e indicatori di progressione per la malattia di Parkinson, con l’obiettivo a lungo termine di permettere interventi prima che si verifichi un danno irreversibile.
Citazione: Moon, CE., Lee, S.J., Shin, H. et al. Early retinal synaptic dysfunction and proteomic remodeling precede neurodegeneration in a Parkinson’s disease model. npj Parkinsons Dis. 12, 47 (2026). https://doi.org/10.1038/s41531-026-01261-7
Parole chiave: Malattia di Parkinson, retina, alfa-sinucleina, neurodegenerazione, biomarcatori