Clear Sky Science · it
Inibizione della corrosione puntiforme dell'acciaio inossidabile da NaNO3: approfondimenti meccanicistici sulla dissoluzione dei solfuri, la depassivazione e la dissoluzione attiva
Perché contano le piccole macchie di ruggine
Dai ponti e grattacieli alle automobili e agli impianti chimici, l'acciaio inossidabile è scelto perché solitamente resiste alla ruggine. Tuttavia, nelle condizioni giuste, può improvvisamente sviluppare piccoli fori profondi chiamati cavità (pit) che possono evolvere in cricche pericolose. Questo studio pone una domanda pratica per l'industria: un composto comune e relativamente sicuro — il nitrato di sodio — può impedire l'avvio di questi pit e, se sì, in che modo? La risposta potrebbe contribuire a mantenere le infrastrutture critiche più sicure più a lungo, impiegando additivi accessibili ed ecologicamente meno dannosi. 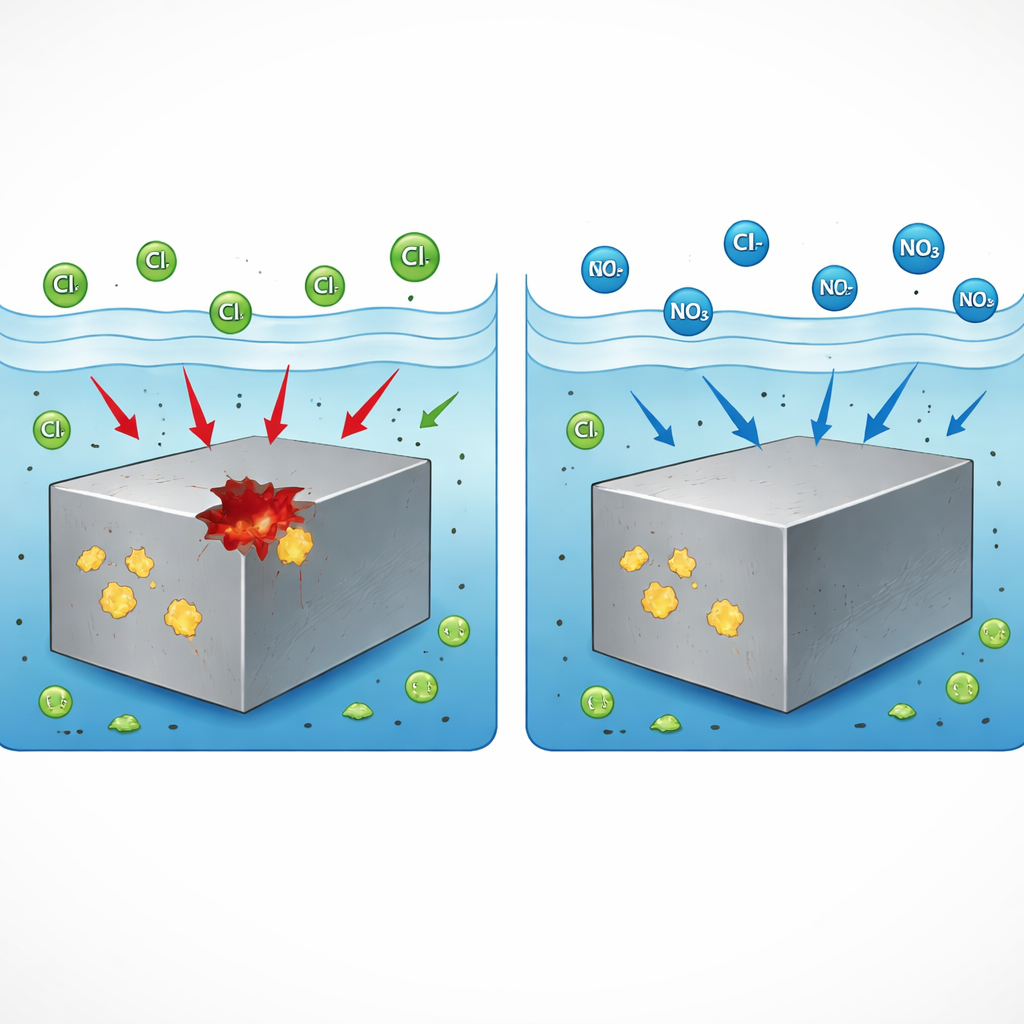
Punti deboli nascosti all'interno dell'acciaio inossidabile
Anche i migliori acciai inossidabili non sono perfettamente uniformi. Al loro interno sono distribuite particelle microscopiche ricche di zolfo, note come inclusioni solfidriche. Due tipi importanti si basano sul manganese (MnS) e sul calcio (CaS). Queste inclusioni si comportano come punti deboli incorporati dove i pit iniziano preferenzialmente quando acqua contenente cloruri, come spray salino o acqua di raffreddamento, entra in contatto con il metallo. Lavori precedenti hanno mostrato che la formazione di pit segue uno schema coerente: la particella solfidrica comincia a dissolversi, il film protettivo sull'acciaio vicino si rompe e poi il metallo circostante comincia a dissolversi rapidamente, scavando una cavità. Il presente studio confronta due acciai commerciali di tipo 304 — uno dominato da inclusioni MnS e uno da inclusioni basate su CaS — per capire se il nitrato può interrompere questo processo in uno o in entrambi i tipi di punto debole.
Testare additivi comuni in acqua salina
I ricercatori hanno immerso gli acciai in una semplice soluzione salina e hanno spinto gradualmente il metallo verso condizioni più corrosive osservando quando si formavano pit stabili. Hanno confrontato tre additivi a concentrazioni realistiche: ammonio, nitrito e nitrato, tutti come sali di sodio o ammonio. Solo il nitrato ha avuto un effetto sorprendente. Sia negli acciai ricchi di MnS sia in quelli ricchi di CaS, l'aggiunta di una modesta quantità di nitrato di sodio ha completamente impedito la formazione di pit stabili nell'intervallo testato, mentre gli altri due additivi non hanno offerto miglioramenti. La microscopia ha confermato che, senza nitrato, i pit iniziavano effettivamente alle inclusioni solfidriche, mentre con il nitrato tali inclusioni non provocavano più forature dannose. Ciò ha dimostrato che il nitrato è un efficace inibitore della puntinatura per diversi tipi di solfuri, non solo un caso particolare. 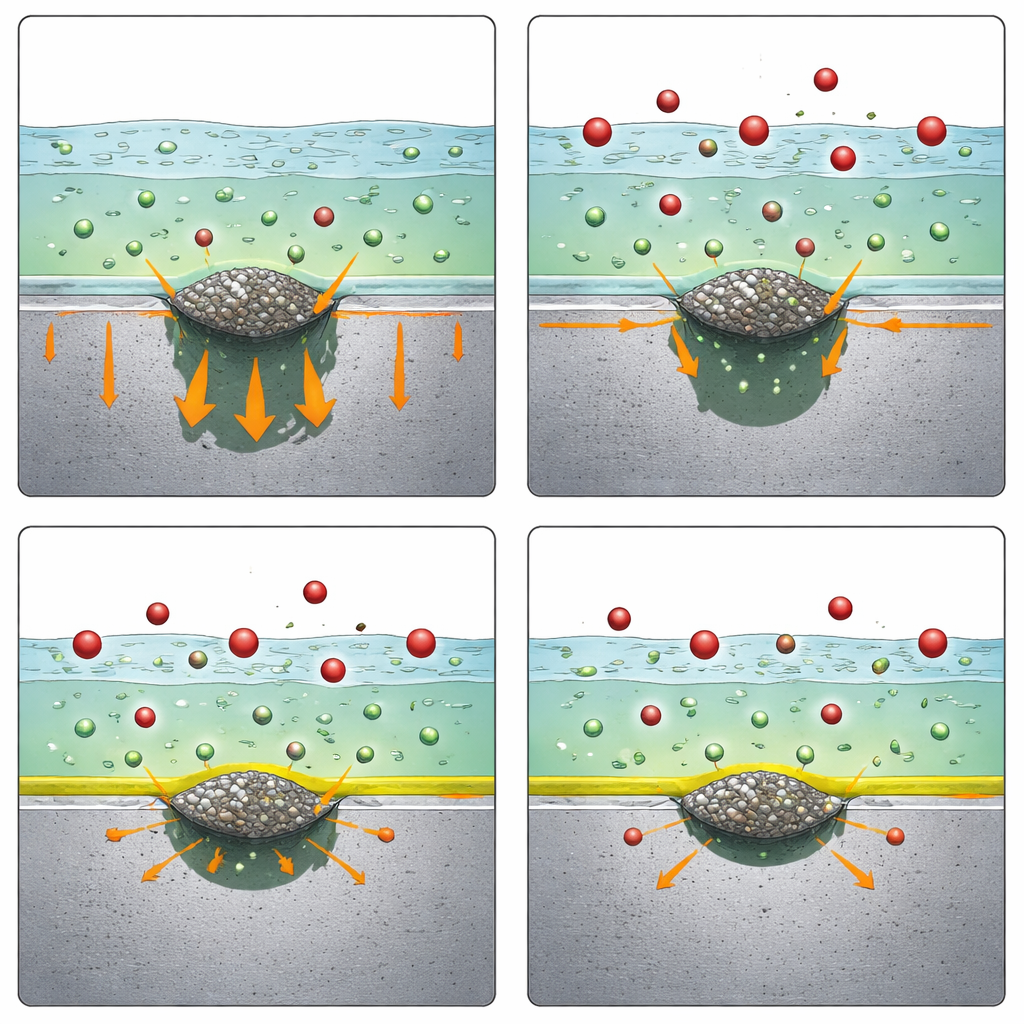
Osservare da vicino cosa il nitrato modifica — e cosa no
Per individuare il meccanismo d'azione del nitrato, il team si è concentrato sulle fasi iniziali dell'inizio dei pit attorno a singole particelle di MnS usando microelettrodi e imaging ad alta risoluzione. Hanno osservato che il nitrato non impediva la dissoluzione delle particelle di MnS né modificava le piccole trincee che si formano dove l'inclusione incontra l'acciaio circostante. Il nitrato non ha nemmeno spostato il livello di acidità a cui il film protettivo dell'acciaio fallisce in soluzione clorurata. Tutto ciò indica che i primi passi dell'iniziazione dei pit — l'indebolimento e la rottura attorno all'inclusione — procedono grosso modo allo stesso modo anche in presenza di nitrato.
Rallentare la fase finale di rapida perdita di metallo
La differenza cruciale è emersa quando i ricercatori hanno ricreato l'ambiente aggressivo all'interno di un pit già formato: condizioni molto acide e ricche di cloruri. Utilizzando soluzioni fortemente acide che imitano la chimica in profondità nelle cavità, hanno riscontrato che l'acciaio mostra normalmente due distinti picchi di rapida dissoluzione del metallo all'aumentare della tensione. L'aggiunta di nitrato ha ridotto in modo consistente il primo picco di dissoluzione, sia in acido semplice sia in acido contenente specie dello zolfo simili a quelle rilasciate dalla dissoluzione del MnS. Le osservazioni superficiali hanno mostrato un attacco uniforme ma a una velocità chiaramente più bassa. Test aggiuntivi, variando acidità e livelli di cloruro, hanno suggerito che l'effetto del nitrato non può essere spiegato semplicemente dalla diluizione dell'acidità, dallo spostamento dei cloruri o dalla stabilizzazione di croste salifiche. Piuttosto, i risultati indicano che il nitrato favorisce la formazione di uno strato superficiale stabilizzante a base di cromo nell'lega, il quale a sua volta rallenta la fase iniziale e più critica della perdita attiva di metallo.
Cosa significa per gli acciai nel mondo reale
In termini semplici, il nitrato non impedisce le prime punzecchiature chimiche alle piccole particelle solfidriche all'interno dell'acciaio inossidabile, ma rallenta la fase finale e incontrollata in cui un'imperfezione innocua si trasforma in un pit pericoloso. Smorzando quell'impennata di perdita di metallo in micro‑ambienti acidi e salini, il nitrato di sodio mantiene l'acciaio più vicino a uno stato passivo e auto‑protettivo, anche quando sono presenti inclusioni solfidriche e ioni cloruro. Poiché il nitrato è relativamente poco costoso, meno tossico di molte alternative e già impiegato nei sistemi idrici industriali, comprendere questo meccanismo rafforza l'argomento per il suo uso controllato come additivo per il controllo della corrosione al fine di estendere la vita utile di strutture e apparecchiature in acciaio inossidabile.
Citazione: Amatsuka, S., Nishimoto, M. & Muto, I. Pitting-corrosion inhibition in stainless steel by NaNO3: mechanistic insights on sulfide dissolution, depassivation, and active dissolution. npj Mater Degrad 10, 40 (2026). https://doi.org/10.1038/s41529-026-00753-4
Parole chiave: corrosione dell'acciaio inossidabile, inibizione della puntinatura, nitrato di sodio, inclusioni solfidriche, soluzioni clorurate