Clear Sky Science · it
Sistema a tetraedro 4A: un quadro sinergico per l’intervento panvascolare potenziato da elettronica flessibile
Riconsiderare la cura dei nostri vasi sanguigni
La malattia panvascolare — il danneggiamento dei vasi sanguigni in tutto il corpo — è oggi la principale causa di morte a livello mondiale. Può colpire cuore, cervello, reni e arti, spesso con pochi segnali premonitori. Questo articolo presenta un audace nuovo piano per affrontare questi disturbi usando elettronica ultra‑sottile e flessibile e intelligenza artificiale. Invece di considerare ogni procedura come un evento isolato, gli autori immaginano una partnership a vita, guidata dai dati, tra paziente e dispositivo, dalla diagnosi all’intervento fino al follow‑up a lungo termine.
Un’idea ampia basata su quattro pilastri
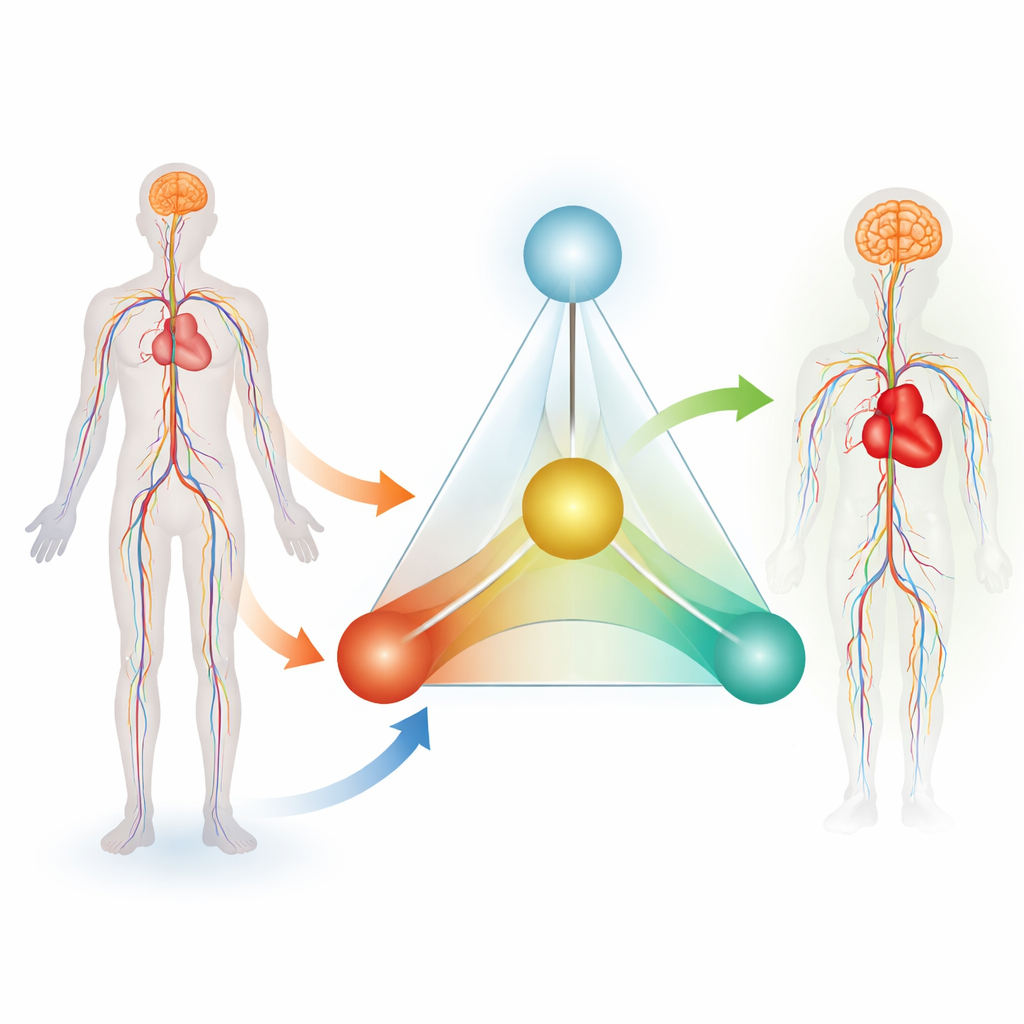
Gli autori propongono ciò che chiamano “Sistema a Tetraedro 4A”, un quadro in quattro parti per gestire la malattia dei vasi come un processo continuo. Le quattro A sono Assessment (valutazione), Assistance (assistenza), Aftercare (post‑cura) e AI‑retrofit (aggiornamento tramite IA). Assessment riguarda come i medici valutano sia il paziente sia gli strumenti prima di una procedura. Assistance si concentra sul guidare in sicurezza strumenti attraverso arterie e vene tortuose durante l’intervento. Aftercare si occupa di monitorare il paziente in seguito, idealmente in modo continuativo. A fare da legante è AI‑retrofit, in cui l’intelligenza artificiale apprende da tutti i dati generati lungo il percorso e reintegra le conoscenze per migliorare dispositivi e decisioni future. Insieme, questi quattro elementi sono rappresentati come una base a tre lati (Assessment, Assistance, Aftercare) che sostiene un apice (IA), formando un tetraedro che rappresenta un ciclo chiuso e auto‑migliorante di cura.
Test delicati e impianti più intelligenti
Nella fase di Assessment gli autori evidenziano cerotti a microaghi flessibili che penetrano minimamente la pelle per campionare il fluido chiaro tra le cellule. Questo fluido rispecchia da vicino la chimica del sangue e può essere prelevato in modo quasi indolore. Sensori integrati in questi minuscoli aghi possono monitorare marcatori di infiammazione, funzione renale, glicemia e altro, portando parti del laboratorio su un cerotto indossabile. Allo stesso tempo, la rassegna descrive come impianti tradizionali — come stent, valvole artificiali e plug per difetti cardiaci — potrebbero essere aggiornati con sensori ultra‑sottili di pressione, chimica e deformazione. Questi dispositivi “intelligenti” non si limiterebbero a riaprire vasi ostruiti; misurerebbero continuamente forze meccaniche, comportamento cellulare e ambiente chimico nel sito dell’impianto, rivelando se il vaso sta davvero guarendo o se sta silenziosamente evolvendo verso problemi.
Guidare gli strumenti dall’esterno verso l’interno
La fase di Assistance affronta un problema comune nelle moderne procedure interventistiche: navigare fili guida e cateteri attraverso reti vascolari complesse minimizzando esposizione ai raggi X e uso di mezzi di contrasto. Gli autori indicano cerotti a ultrasuoni flessibili emergenti e sonde fotoacustiche che possono fornire immagini in tempo reale dei vasi senza radiazioni. Descrivono anche fili guida morbidi e microcateteri controllabili magneticamente i cui punte possono essere deflesse da campi magnetici esterni e mossi da bracci robotici. Accoppiati a sensori flessibili e imaging intelligente, questi sistemi mirano a far avanzare dispositivi attraverso vasi sottilissimi o con curve acute con precisione sub‑millimetrica, riducendo il rischio di lacerazioni vascolari, ictus o procedure fallite.
Vivere con una rete di guardiani silenziosi
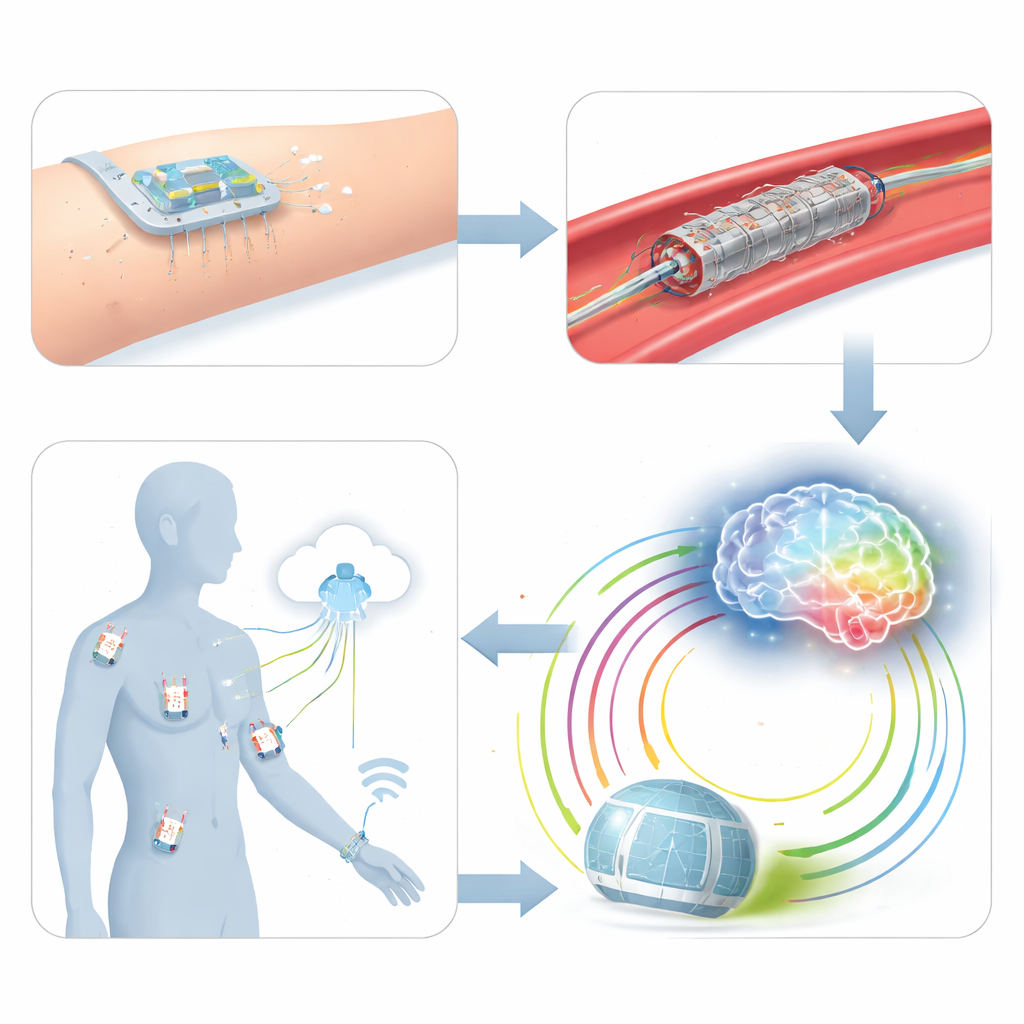
Dopo una procedura, molti pazienti oggi tornano a visite cliniche sporadiche e controlli brevi, che possono facilmente non rilevare restenosi silente o formazione di coaguli. Nella fase di Aftercare gli autori immaginano una “Internet delle cose mediche”: una rete di sensori flessibili indossabili, semi‑impiantabili e completamente impiantabili distribuiti su organi e profondità dei tessuti. Cerotti cutanei potrebbero monitorare ritmo cardiaco e respirazione, microaghi potrebbero sorvegliare glucosio e marcatori infiammatori, e sensori impiantati su stent o arterie seguirebbero pressione e flusso locali. Tutti questi invierebbero dati in modalità wireless a sistemi cloud, creando una “Rete Sanitaria Wireless di Sensori” che mantiene i medici virtualmente al letto del paziente e cattura come la malattia evolve in tutto il corpo, non solo in un singolo punto trattato.
Lasciare che gli algoritmi chiudano il ciclo
Sulla sommità del tetraedro si trova AI‑retrofit, dove gli algoritmi trasformano flussi grezzi di sensori in cura migliore. Modelli di machine learning possono aiutare a progettare microaghi più affidabili e stent più intelligenti, riconoscere schemi a rischio nei dati chimici e di pressione prima che compaiano i sintomi, e guidare robot chirurgici lungo percorsi più sicuri. L’apprendimento per rinforzo profondo — software che impara per tentativi ed errori su dati storici — potrebbe suggerire come aggiustare farmaci o quando reintervenire per ciascun paziente. Grandi modelli linguistici potrebbero un giorno intrecciare letture dei sensori, immagini e cartelle cliniche in riassunti chiari per i clinici e spiegazioni comprensibili per i pazienti. In questa visione, ogni procedura alimenta il sistema con informazioni, affinando le decisioni future.
Dal concetto alla cura quotidiana
Per un lettore non specialista, il messaggio centrale è che la cura delle malattie vascolari può passare da interventi isolati e reattivi a una partnership intelligente e continua tra corpo, elettronica flessibile e IA. I cerotti a microaghi rendono i test più delicati, gli impianti intelligenti sorvegliano i siti vulnerabili dall’interno, sensori indossabili e impiantati tengono sotto controllo l’intero organismo e algoritmi di apprendimento collegano i punti nel tempo su mesi e anni. Restano molte sfide — dalla sicurezza a lungo termine e all’alimentazione, fino alla sicurezza dei dati e alla regolamentazione — ma gli autori sostengono che nel prossimo decennio questo approccio a Tetraedro 4A potrebbe trasformare le procedure vascolari occasionali di oggi in un sistema di protezione personalizzato e in evoluzione contro il gruppo di malattie più letale al mondo.
Citazione: You, L., Qu, Y., Chen, Y. et al. 4A tetrahedron system: a synergistic framework for panvascular intervention empowered by flexible electronics. npj Flex Electron 10, 35 (2026). https://doi.org/10.1038/s41528-026-00537-5
Parole chiave: elettronica flessibile, malattie vascolari, impianti intelligenti, sensori indossabili, IA medica