Clear Sky Science · it
Screening genomico neonatale semi-automatizzato mette in luce complessità nel refertare
Perché le piccole gocce di sangue possono contenere grandi risposte
Nei giorni successivi alla nascita, la maggior parte dei neonati viene sottoposta a un silenzioso test salvavita: un prelievo dal tallone che deposita sangue su una scheda. Questo studio esplora cosa succede se facciamo un passo avanti e leggiamo molto di più del codice genetico del bambino da quella stessa macchia di sangue. I ricercatori dell’Australia Meridionale hanno cercato di capire se aggiungere un’analisi del DNA su larga scala ai controlli neonatali di routine potesse individuare in sicurezza più condizioni trattabili in fase precoce—senza sommergere famiglie e medici con informazioni confuse o non utili.
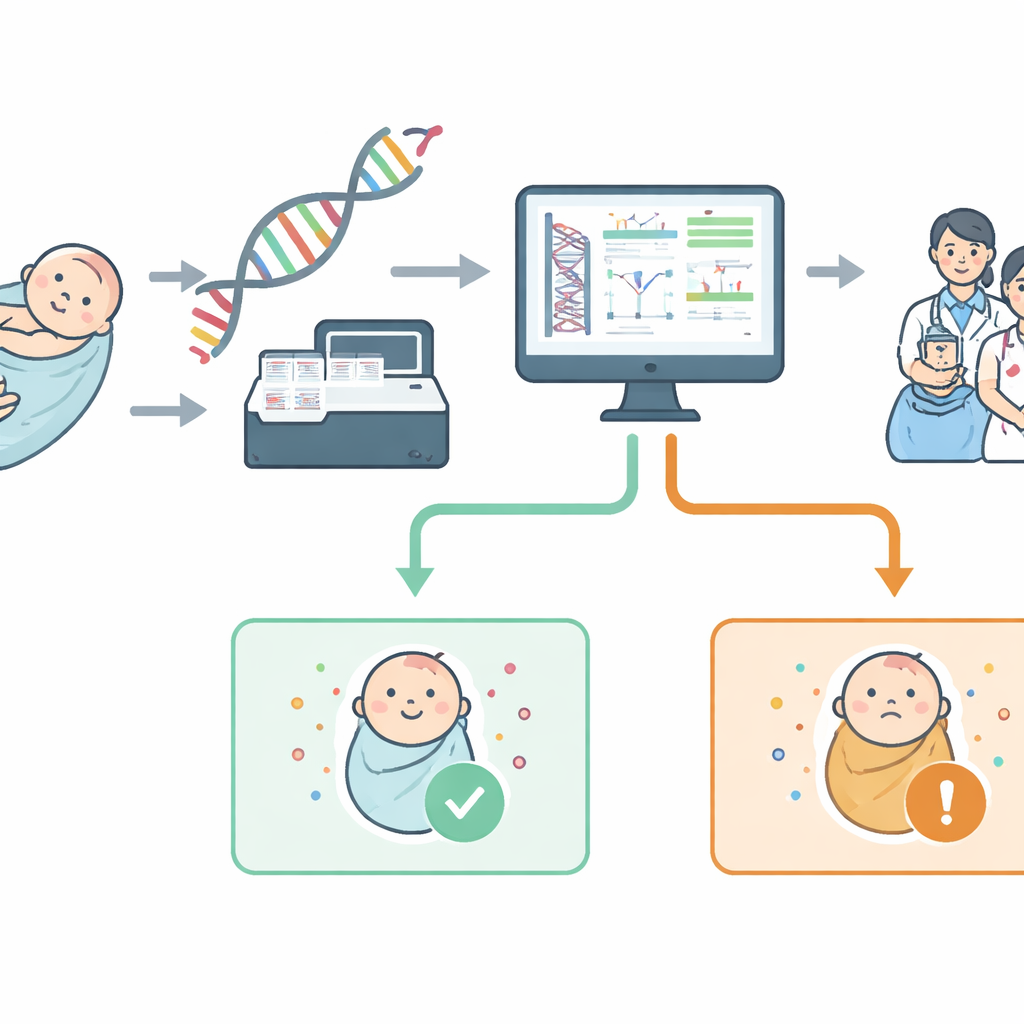
Dal prelievo al tallone alla scansione del genoma
Lo screening neonatale tradizionale ricerca alcune decine di condizioni misurando sostanze chimiche nel sangue. Al contrario, lo screening genomico neonatale legge porzioni di DNA per cercare direttamente cambiamenti che causano malattie in geni specifici. Il progetto NewbornsInSA ha sviluppato un test basato sul sequenziamento dell’intero genoma, ma ha deliberatamente limitato la ricerca a un pannello “virtuale” di 613 geni. Questi geni sono stati scelti insieme ai medici locali seguendo regole semplici: la condizione dovrebbe iniziare nell’infanzia, provocare problemi sanitari gravi, disporre di una strategia di trattamento o prevenzione significativa e essere rilevabile in modo affidabile in laboratorio. Gruppi di cittadini e pazienti hanno poi contribuito a raggruppare queste condizioni in categorie per apparati, in modo che i genitori potessero comprendere meglio ciò che il test copre.
Sottoporre il nuovo test alla prova
Prima di offrire questo controllo basato sul DNA alle nuove famiglie, il team doveva dimostrare che funzionasse. Hanno prelevato 46 schede di sangue conservate da bambini la cui diagnosi genetica era già nota ma nascosta agli analisti. Utilizzando il sequenziamento dell’intero genoma e due sistemi software separati, hanno verificato se la loro pipeline sarebbe stata in grado di segnalare correttamente i neonati che realmente avevano una delle condizioni target. Il risultato è stato incoraggiante: il processo ha identificato il 97% dei casi veri e non ha prodotto falsi allarmi dopo la revisione degli esperti. L’unico caso non rilevato ha messo in evidenza un limite chiave di qualsiasi screening basato sui geni—quando le prove scientifiche a supporto di una specifica variazione del DNA sono incomplete, i computer e perfino gli esperti possono essere costretti a etichettarla come “incerta” e considerarla un non-risultato.
Lasciare ai computer il lavoro pesante
Leggere un intero genoma genera migliaia di varianti per ogni neonato, troppe perché gli esseri umani le esaminino una per una. Per far fronte a questo, i ricercatori hanno costruito un flusso di lavoro semi-automatizzato. Script personalizzati, collegati a una piattaforma commerciale di analisi, esaminano l’elenco delle varianti annotate e mettono automaticamente da parte i neonati che chiaramente non presentano riscontri preoccupanti, etichettandoli come “bassa probabilità”. Solo i casi con modifiche che sembrano potenzialmente dannose—come varianti note causa di malattia o probabili interruzioni dannose di un gene—vengono passati agli analisti esperti per una revisione dettagliata. Nei primi 100 neonati reali testati, questa automazione ha immediatamente ridotto di oltre la metà il numero di bambini che richiedevano una revisione manuale, un passaggio cruciale se tale screening deve essere esteso all’intera popolazione.
Bambini reali, decisioni reali
Quando il team ha applicato il flusso di lavoro ai primi 100 neonati arruolati, cinque bambini hanno ricevuto risultati che suggerivano un’alta probabilità di una condizione specifica. Questi includevano disturbi del ritmo cardiaco che possono causare battiti pericolosamente irregolari, un problema metabolico già sospettato dallo screening standard, una variazione genica che rende certi antibiotici rischiosi per l’udito e una forma lieve di iperglicemia ereditaria. In ciascun caso, il risultato ha attivato un follow-up su misura: controlli cardiaci e monitoraggio continuativo, avvisi elettronici per evitare farmaci specifici o pianificazione della cura nelle gravidanze future. Allo stesso tempo, molti altri riscontri non sono stati deliberatamente comunicati perché legati a sintomi lievi, tumori ad insorgenza adulta, rischio incerto o schemi complessi che le conoscenze attuali non permettono di interpretare con sicurezza in un neonato sano. Queste decisioni complicate hanno richiesto ore di lettura della letteratura e discussioni tra genetisti e specialisti, sottolineando che il giudizio esperto è ancora fondamentale.
Bilanciare aiuto precoce e onere futuro
Questo lavoro mostra che è tecnicamente possibile utilizzare i dati dell’intero genoma ricavati da una piccola macchia di sangue per individuare più condizioni infantili trattabili rispetto ai test standard, con elevata accuratezza e supporto da software intelligenti. Ma mette anche a nudo la corda etica e pratica su cui camminare: ogni gene aggiuntivo controllato aumenta la possibilità di scoprire informazioni che potrebbero non aiutare il bambino ora, che potrebbero preoccupare i genitori o che potrebbero diventare rilevanti solo dopo decenni. L’approccio semi-automatizzato e attentamente curato del team NewbornsInSA—dove i computer scartano i negativi chiari e gli umani si concentrano sui casi sfumati—offre un modello di come lo screening genomico neonatale potrebbe essere implementato in modo responsabile, mentre studi di follow-up in corso monitorano i benefici e i rischi nel mondo reale per le famiglie.
Citazione: Chowdhury, A., Marri, S., Anastasi, L. et al. Semi-automated genomic newborn screening highlights complexities in reporting. npj Genom. Med. 11, 13 (2026). https://doi.org/10.1038/s41525-026-00553-4
Parole chiave: screening genomico neonatale, sequenziamento dell'intero genoma, gocce di sangue su carta, interpretazione di varianti genetiche, rilevazione precoce di malattie rare