Clear Sky Science · it
L'espressione dei geni bersaglio del recettore degli estrogeni β rivela nuove funzioni repressorie nel carcinoma mammario aggressivo
Perché questa ricerca è importante
Il carcinoma mammario infiammatorio è una delle forme più aggressive e letali di tumore al seno, spesso a rapida diffusione e con poche opzioni terapeutiche mirate per i pazienti. Questo studio indaga un sensore ormonale meno noto nelle cellule mammarie, chiamato recettore degli estrogeni beta, e mostra come possa agire come un freno naturale alla diffusione del tumore. Comprendere il funzionamento di questo freno intrinseco potrebbe aprire la strada a nuovi farmaci in grado di rallentare o prevenire le metastasi in pazienti che oggi hanno scelte molto limitate.
Un volto diverso del carcinoma mammario infiammatorio
A differenza di molti tumori mammari che dipendono dal classico recettore degli estrogeni alfa, il carcinoma mammario infiammatorio è di solito privo di questa molecola e quindi risponde poco alle terapie ormonali standard. Gli autori si concentrano invece su un secondo recettore degli estrogeni, il recettore degli estrogeni beta (ERβ), che avevano precedentemente associato a un numero minore di metastasi sia nei pazienti sia nei modelli murini. Studi precedenti suggerivano che ERβ rallenta il citoscheletro e i meccanismi di movimento cellulare. In questo lavoro, il gruppo ha voluto mappare, a livello dell’intero genoma, come ERβ modifica l’attività genica e quali molecole a valle possano spiegare il suo ruolo protettivo e anti-metastatico.
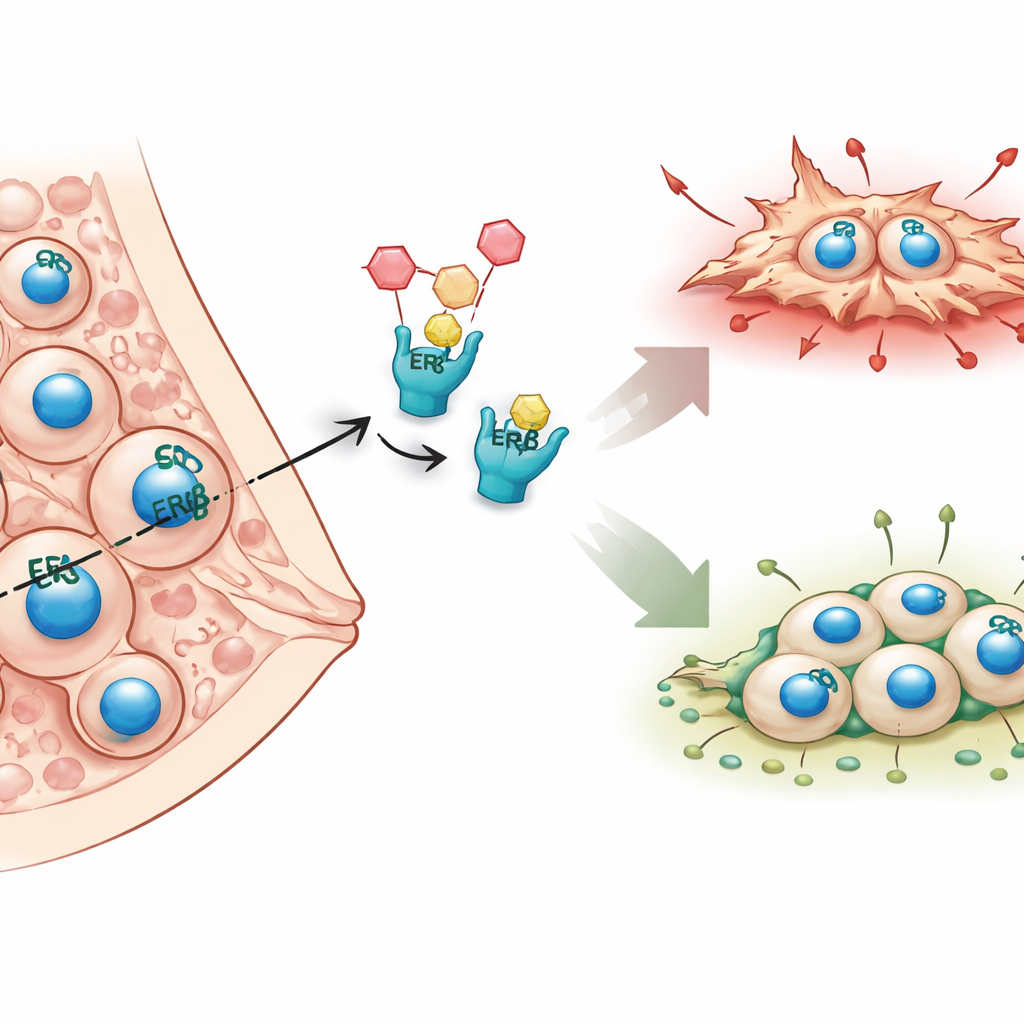
Leggere il manuale di istruzioni della cellula tumorale
Per mettere a fuoco l’influenza di ERβ, i ricercatori hanno usato due potenti approcci di sequenziamento su linee cellulari di carcinoma mammario infiammatorio. Un metodo, il ChIP-seq, individua esattamente dove ERβ si lega al DNA, come segnare pagine e righe specifiche nel manuale di istruzioni della cellula. L’altro, l’RNA-seq, misura quali geni vengono attivati o repressi quando ERβ è presente, assente o attivato da un farmaco selettivo. Confrontando questi dataset, hanno identificato migliaia di siti del DNA legati da ERβ, molti dei quali non solo negli interruttori di accensione/spegnimento dei geni ma anche all’interno o tra i geni, suggerendo un controllo di ampia portata. Hanno inoltre scoperto che ERβ spesso coopera con famiglie di altri fattori di trascrizione, formando complessi che decidono collettivamente quali geni vengano silenziati o attivati.
Rimodellare crescita, movimento e metabolismo
L’analisi integrata ha mostrato che ERβ tende ad attenuare i geni che promuovono il movimento cellulare, i cambiamenti di forma e l’invasione, in particolare quelli legati al citoscheletro di actina e alla segnalazione delle GTPasi Rho—vie note per guidare le metastasi. Contemporaneamente, ERβ sostiene programmi genici associati allo sviluppo dei tessuti e alla differenziazione cellulare, indirizzando le cellule tumorali verso uno stato più stabile e meno aggressivo. Lo studio ha anche rivelato un ruolo sorprendente di ERβ nell’aggiustare le vie metaboliche, in particolare quelle che coinvolgono acidi grassi e fosfolipidi, componenti chiave per il carburante e i mattoni dei tumori a rapida crescita. È importante sottolineare che questi effetti sono stati osservati non solo in cellule ingegnerizzate per sovraesprimere ERβ, ma anche in cellule con livelli naturali del recettore, a sottolineare la rilevanza nella pratica clinica.
Piccoli messaggeri di RNA e impatto clinico
Oltre ai geni che codificano proteine, il team ha esaminato i microRNA—piccole molecole di RNA che modulano finemente l’espressione genica. Hanno trovato dozzine di microRNA i cui livelli cambiavano quando ERβ veniva rimosso o ripristinato, molti dei quali sono stati collegati alla soppressione tumorale nel cancro al seno. Collegando questi microRNA ai loro geni bersaglio, gli autori hanno mostrato che ERβ controlla indirettamente alcuni driver tumorali attraverso una rete regolatoria a strati. Poi hanno analizzato dati clinici, esaminando tumori di pazienti con carcinoma mammario infiammatorio e non infiammatorio. Diversi geni regolati da ERβ sono risultati fortemente associati alla sopravvivenza dei pazienti: livelli elevati di alcuni (come SERPINA1 e HSPB8) prevedevano esiti migliori, mentre livelli alti di altri (come PITX1 e HOMER3) erano legati a una sopravvivenza peggiore. Questo posiziona queste molecole a valle come potenziali marcatori prognostici e possibili bersagli farmacologici futuri.
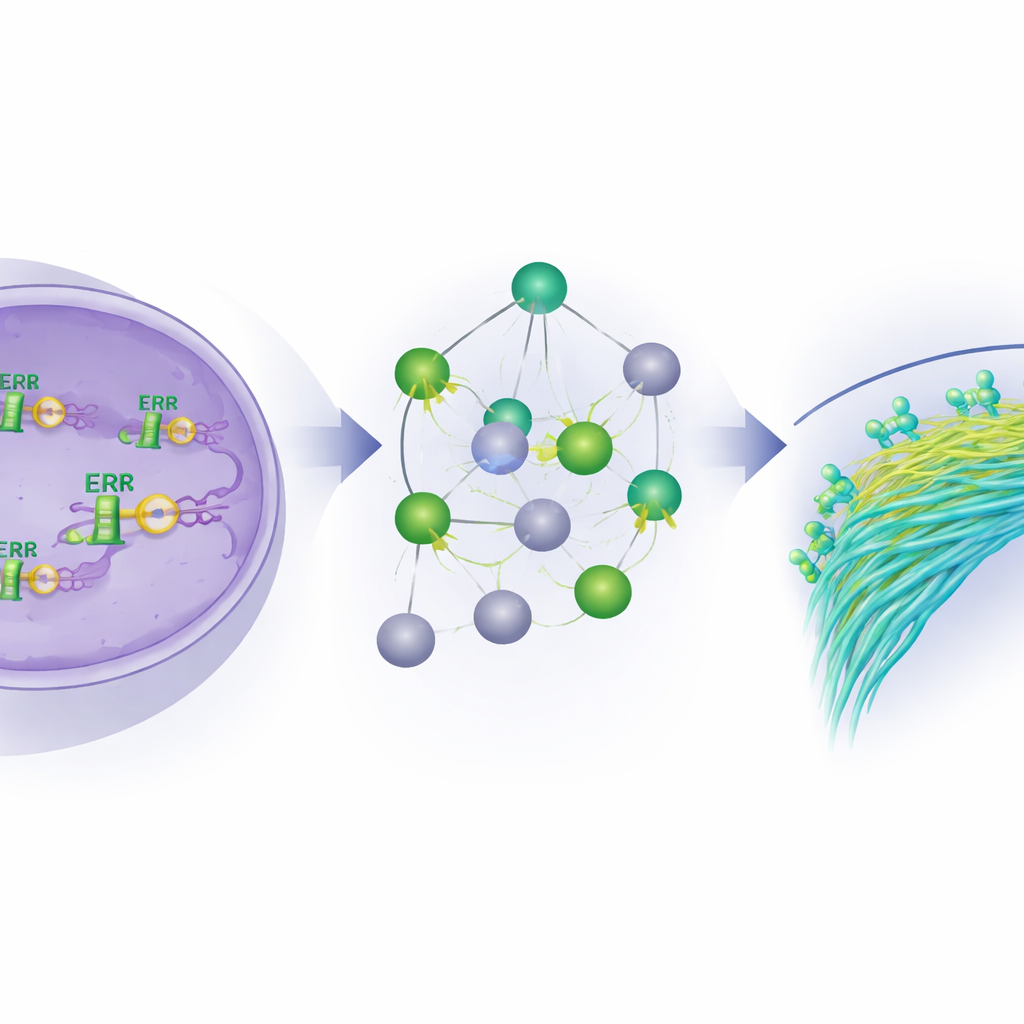
Dal freno molecolare alle terapie future
Nel complesso, lo studio ritrae ERβ come un freno centrale sul comportamento invasivo delle cellule del carcinoma mammario infiammatorio. Legandosi al DNA, associandosi ad altri regolatori e plasmando reti di geni e microRNA, ERβ attenua i programmi che favoriscono la migrazione cellulare e le metastasi, promuovendo stati più stabili e differenziati e riallineando il metabolismo tumorale. Per i pazienti, questo suggerisce che farmaci che attivano ERβ o inibiscono i suoi principali bersagli a valle—soprattutto quelli coinvolti nel movimento cellulare e nell’uso degli acidi grassi—potrebbero costituire la base di nuovi trattamenti più mirati per questa malattia difficile da trattare.
Citazione: Tastsoglou, S., Karagounis, I.V., Miliotis, M. et al. Estrogen receptor β target gene expression reveals novel repressive functions in aggressive breast cancer. npj Breast Cancer 12, 38 (2026). https://doi.org/10.1038/s41523-026-00905-4
Parole chiave: carcinoma mammario infiammatorio, recettore degli estrogeni beta, metastasi, regolazione genica, metabolismo del cancro