Clear Sky Science · it
L’asse CXCL10/CXCR3 è essenziale per sostenere la dormienza immunologica nel carcinoma mammario triplo negativo
Perché alcuni tumori rimangono dormienti invece di diffondersi
Il tumore al seno a volte si comporta come un agente dormiente. Dopo il trattamento iniziale, poche cellule tumorali possono nascondersi nell’organismo per anni, non crescendo a sufficienza per essere rilevate dalle immagini—ma rimanendo comunque capaci di risvegliarsi in seguito e provocare metastasi potenzialmente letali. Questo studio indaga perché quello stato di “sonno”, chiamato dormienza, si verifica in una forma particolarmente aggressiva della malattia, il carcinoma mammario triplo negativo, e individua un segnale chimico che aiuta il sistema immunitario a mantenere sotto controllo queste cellule.
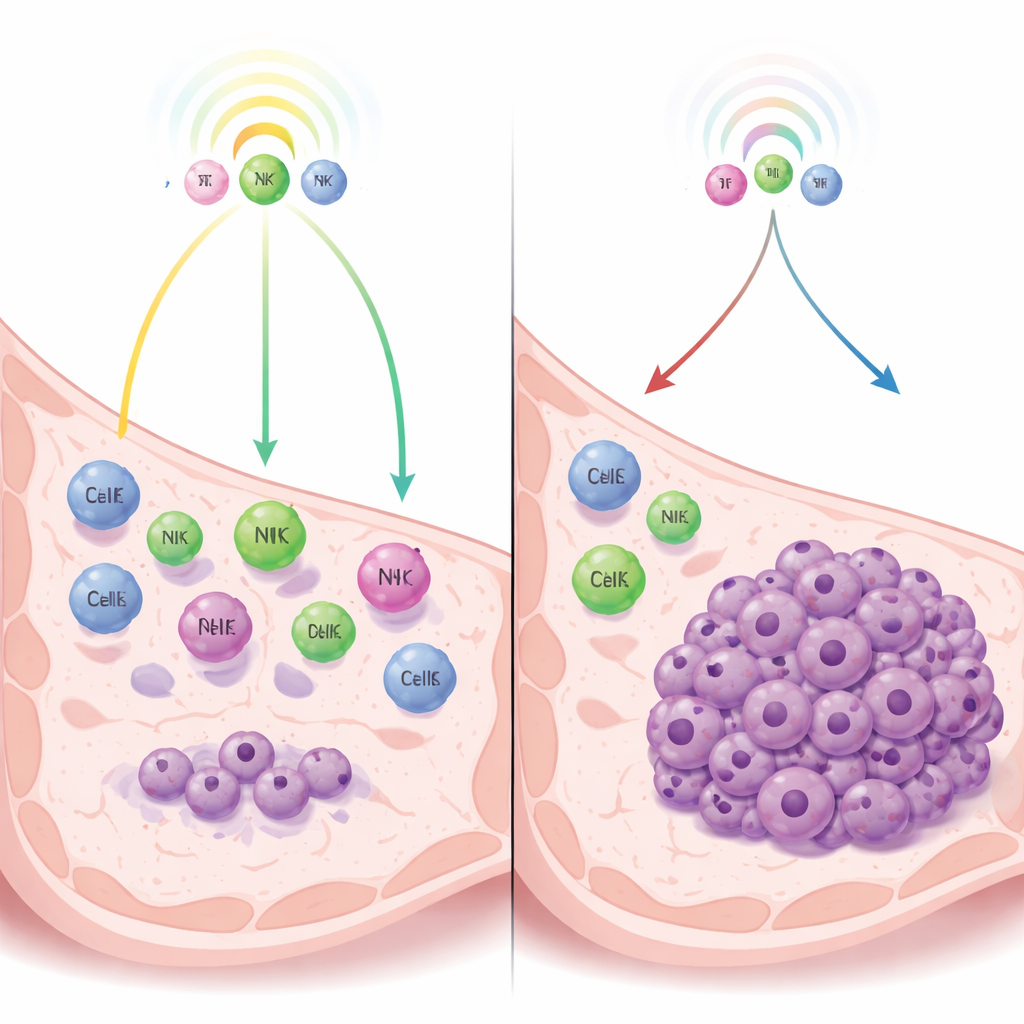
Una lotta di trazione tra tumore e sistema immunitario
Gli autori si concentrano su un tipo di dormienza controllata non dalla carenza di apporto ematico o da freni interni alle cellule, ma dalla sorveglianza immunitaria—la vigilanza costante delle cellule immunitarie che può tenere i tumori a bada senza eliminarli completamente. Utilizzando modelli murini di carcinoma mammario triplo negativo, confrontano cellule tumorali che rimangono naturalmente dormienti con cellule strettamente correlate che formano tumori a rapida crescita. Esaminando quali geni sono attivati, rilevano che le cellule dormienti attivano fortemente le vie dell’interferone—sistemi di allarme immunitari che stimolano il rilascio di messaggeri chimici che attraggono cellule immunitarie nell’area tumorale.
Un messaggero chimico chiave che mantiene i tumori silenziosi
Tra le molte molecole attivate nelle cellule dormienti, una spicca: CXCL10, una piccola proteina che agisce come un faro per le cellule immunitarie che esprimono il suo recettore partner, CXCR3. Le cellule tumorali dormienti producono molto più CXCL10 rispetto alle controparti aggressive. Quando i ricercatori disattivano deliberatamente CXCL10 nelle cellule dormienti e le impiantano in topi con sistema immunitario intatto, le cellule un tempo silenti formano rapidamente tumori. Bloccare il recettore CXCR3 con un anticorpo produce un effetto simile. In entrambi i casi, le cellule tumorali sfuggono allo stallo immunitario e cominciano a crescere, dimostrando che l’asse CXCL10/CXCR3 non è solo correlato alla dormienza—è necessario per mantenerla.
Come il cambiamento del microambiente locale altera l’equilibrio
Ridurre CXCL10 non altera solo una singola via; rimodella l’intero paesaggio immunitario locale. Nei tumori che hanno perso CXCL10, i benefici T CD4 e CD8 diminuiscono, mentre alcune cellule mieloidi con capacità soppressive diventano più abbondanti. Anche le cellule natural killer e le cellule dendritiche mostrano variazioni numeriche. Questo pattern appare sia nei tumori primari sia nei polmoni, dove le cellule tumorali possono migrare e rimanere nascoste. Anche quando le metastasi polmonari sono troppo piccole per essere viste al microscopio, i marker molecolari rivelano che più cellule tumorali riescono a colonizzare i polmoni in assenza di CXCL10, e meno cellule T infiltrano quei tessuti. Tuttavia, in topi privi di un sistema immunitario funzionante, rimuovere CXCL10 non fa differenza—le cellule dormienti crescono comunque—sottolineando che questo segnale agisce tramite il controllo immunitario piuttosto che come un freno diretto sulla proliferazione delle cellule tumorali.
Perché più segnale aiuta ma non è una soluzione magica
Il gruppo testa anche l’ipotesi opposta: aumentare CXCL10 può trasformare un tumore aggressivo in uno dormiente? Quando ingegnerizzano cellule tumorali a rapida crescita per produrre CXCL10 in eccesso, i tumori crescono più lentamente e compaiono con maggiore ritardo, e alcuni tipi di cellule immunitarie nel sangue aumentano. Tuttavia, la dormienza completa non si instaura; alla fine tutti i topi sviluppano tumori. Questo suggerisce che, sebbene CXCL10 sia essenziale per mantenere la dormienza quando il resto dell’apparato immunitario è presente, non può da solo costruire quello stato complesso da zero. Altre vie devono cooperare per creare un equilibrio duraturo tra attacco immunitario e sopravvivenza delle cellule tumorali.
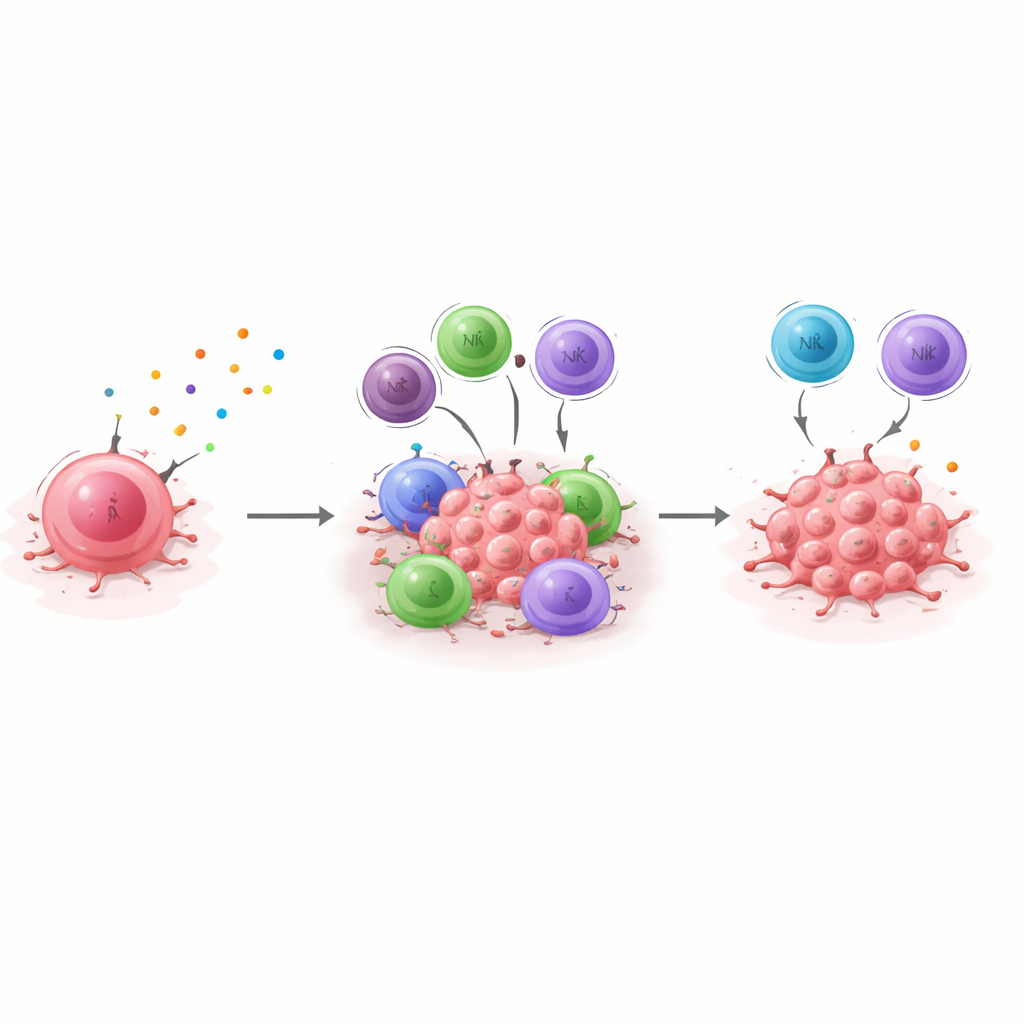
Dagli esperimenti sui topi alla prospettiva per i pazienti
Per collegare i loro risultati alla malattia umana, i ricercatori derivano una “firma di dormienza”—un insieme di geni costantemente più espressi nelle cellule dormienti e che diminuiscono quando CXCL10 viene silenziata. Esaminano quindi grandi dataset di pazienti con cancro al seno per valutare come questa firma sia correlata alla sopravvivenza. Nel carcinoma mammario triplo negativo, i pazienti i cui tumori esprimono a livelli più alti questa firma di dormienza vivono più a lungo in generale e tendono a rimanere liberi da recidiva per più anni, coerentemente con uno stato dormiente controllato dal sistema immunitario che ritarda le ricadute. L’effetto non si osserva allo stesso modo nei tumori ormono‑positivi, evidenziando differenze biologiche tra i sottotipi di cancro al seno. Nel complesso, i risultati suggeriscono che l’asse CXCL10/CXCR3 sia un pilastro centrale della dormienza mediata dal sistema immunitario nel carcinoma mammario triplo negativo, e che misurare questa firma di dormienza potrebbe aiutare a identificare i pazienti più propensi a beneficiare di terapie che rafforzano il controllo immunitario—o, al contrario, quelli che potrebbero richiedere un monitoraggio a lungo termine più stretto perché il loro tumore è meno ben controllato.
Citazione: Yilmaz, A., Haerri, L., Granda, M.E. et al. The CXCL10/CXCR3 axis is essential for sustaining immunological dormancy in triple-negative breast cancer. npj Breast Cancer 12, 36 (2026). https://doi.org/10.1038/s41523-026-00903-6
Parole chiave: carcinoma mammario triplo negativo, dormienza tumorale, sorveglianza immunitaria, segnalizzazione delle chemochine, asse CXCL10 CXCR3