Clear Sky Science · it
L'analisi spaziale dell'espressione genica rivela i fattori alla base della metastasi linfonodale estremamente precoce nel cancro al seno
Perché contano le cellule tumorali che viaggiano in piccole quantità
Quando il cancro al seno si diffonde al di fuori della mammella, spesso si arresta per primo nei linfonodi vicini—piccoli filtri che aiutano a combattere le infezioni. I medici sanno che trovare cellule tumorali in questi nodi in genere segnala un rischio maggiore di recidiva. Ma cosa accade nei primissimi istanti in cui solo poche cellule arrivano in un linfonodo è stato quasi impossibile da osservare nei pazienti reali. Questo studio ha impiegato un nuovo tipo di “mappa” microscopica dell’attività genica per osservare quegli stadi iniziali con un dettaglio senza precedenti, rivelando quali cellule riescono, quali falliscono e perché questo è importante per l’esito clinico.
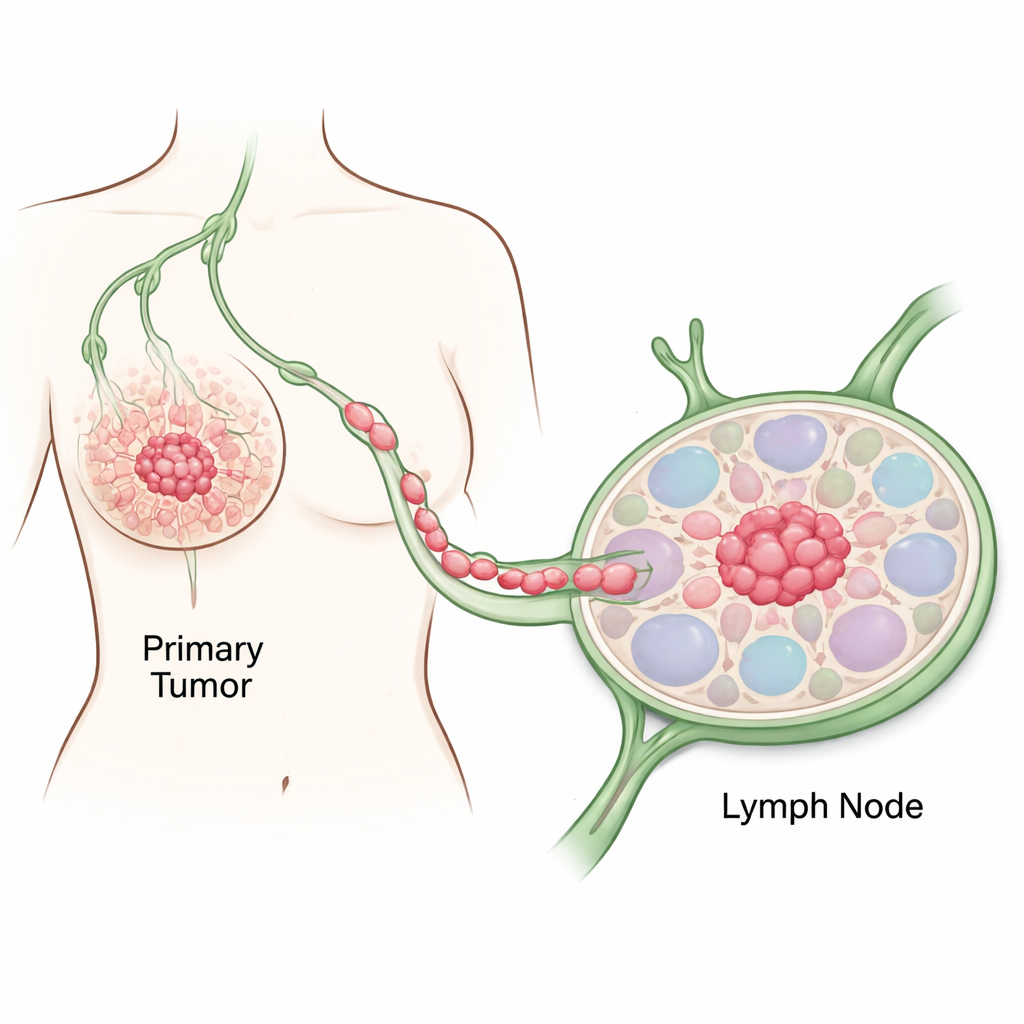
I primi passi del cancro
I ricercatori si sono concentrati su tessuto prelevato da una donna di 80 anni con un cancro al seno aggressivo, positivo per HER2. Hanno campionato sia aree della mammella dall’aspetto normale sia regioni tumorali vicine, quindi hanno usato diversi test su DNA e RNA per tracciare come le cellule ordinarie siano diventate tumorali. Rispetto al tessuto sano, le aree tumorali mostravano i classici segni del cancro: adesione cellulare compromessa, divisione cellulare iperattiva, ampi cambiamenti nella metilazione del DNA e mutazioni chiave in geni che controllano la crescita e la stabilità del genoma. Questi cambiamenti molecolari coincidevano con quanto osservato dai patologi al microscopio, confermando una progressione graduale da cellule mammarie normali a cellule pienamente maligne.
Cellule che cambiano forma in movimento
Per capire come le cellule tumorali inizino a migrare, il team ha usato una tecnica ad alta risoluzione che legge l’attività genica nelle singole cellule mantenendo la loro posizione esatta nel tessuto. Ciò ha permesso di ricostruire come le cellule tumorali cambiassero identità man mano che lasciavano le strutture mammarie normali e si dirigevano verso la metastasi. Hanno constatato che il tumore sembrava originare da un particolare tipo di cellula mammaria matura, che poi acquisiva progressivamente caratteristiche di un processo chiamato transizione epiteliale–mesenchimale—una specie di metamorfosi che aiuta le cellule a distaccarsi, muoversi e invadere i tessuti circostanti. Piuttosto che un interruttore acceso/spento, le cellule occupavano uno spettro di stati misti, mescolando tratti “epiteliali” (ordinati, aderenti) con tratti “mesenchimali” (mobili, invasivi). Alcune di queste cellule ibride si disperdevano nel tumore, mentre altre si raggruppavano in popolazioni più avanzate, pronte a diffondersi nei linfonodi.
La prima testa di ponte remota in un linfonodo
In un linfonodo che risultava privo di metastasi secondo i test clinici standard, gli scienziati hanno individuato qualcosa di notevole: appena 30 cellule tumorali isolate, occupanti una regione larga solo circa 200 micrometri—circa il doppio dello spessore di un capello umano. Queste cellule tumorali isolate provenivano da diversi stati ibridi distinti, ciascuno con il proprio profilo di espressione genica. Raggruppando le cellule correlate, il team ha definito sei sottotipi con ruoli diversi. Un sottotipo, fortemente “mesenchimale”, sembrava particolarmente abile a resistere alla morte cellulare e a sfuggire all’attacco immunitario. Un altro sottotipo, che riacquistava caratteristiche più epiteliali, mostrava un notevole cambiamento nel suo uso energetico, preferendo il metabolismo degli acidi grassi. Solo questo gruppo metabolicamente riorientato, più simile all’epitelio, è riuscito a formare piccole colonie nei linfonodi, suggerendo che la scelta del carburante—non solo l’invasività—contribuisce a determinare se gli arrivi precoci riescono a impiantarsi.
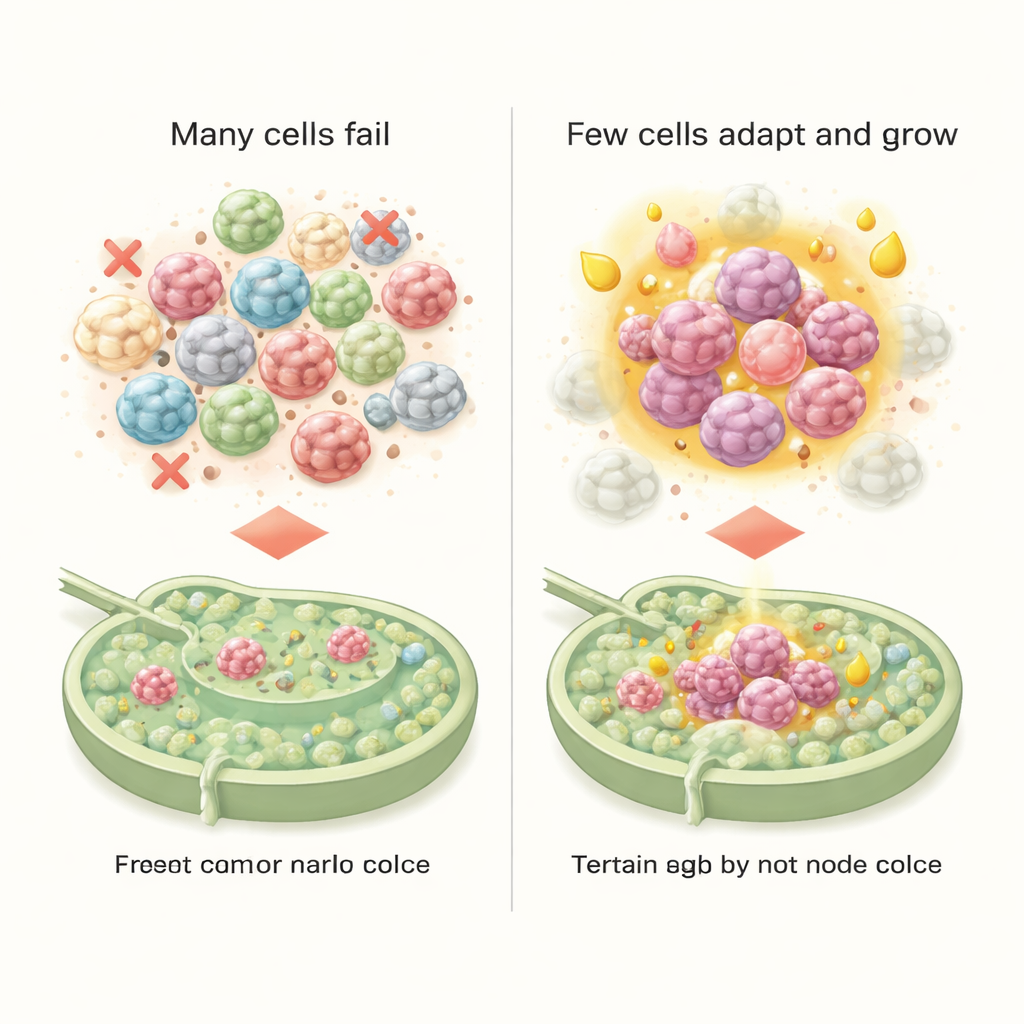
Un linfonodo che silenziosamente aiuta il cancro
Lo studio ha inoltre esaminato come l’ambiente del linfonodo rispondesse a questi intrusi. Anche prima che si formasse una metastasi visibile, cellule immunitarie, cellule dei vasi sanguigni e tessuto connettivo stavano già inviando segnali che attenuavano le reazioni immunitarie e sostenevano la sopravvivenza tumorale. Alcune coppie recettore–ligando tra le cellule immunitarie suggerivano una tolleranza immunitaria precoce, mentre altre promuovevano la crescita di nuovi vasi sanguigni e il rimodellamento degli impalcati tissutali. Insieme, questi cambiamenti hanno costruito una nicchia sorprendentemente accogliente per le cellule tumorali adattate metabolicamente, aiutandole a sopravvivere, crescere e potenzialmente seminare ulteriori diffusione.
Cosa significa per i pazienti
Confrontando i loro risultati con grandi dataset clinici esistenti, i ricercatori hanno fatto una scoperta controintuitiva. Le cellule più abili a formare colonie linfonodali precoci, e anche quelle con i tratti mesenchimali più pronunciati, non corrispondevano agli esiti clinici peggiori. Al contrario, i pazienti avevano gli esiti peggiori quando i loro tumori ospitavano certi tipi ibridi aggressivi caratterizzati da elevata attività del ciclo cellulare e programmi di consumo di zucchero (glicolisi) guidati da geni come MYC. In altre parole, diversi stati delle cellule trasformate sembrano specializzarsi: alcuni sono esperti nell’impadronirsi silenziosamente di nuovi siti, mentre altri guidano una rapida crescita e recidiva. Comprendere e mirare a questi distinti stati cellulari e alle loro preferenze metaboliche potrebbe portare a terapie più precise—capaci non solo di rilevare la diffusione più precoce in modo più affidabile, ma anche di eliminare i tipi cellulari tumorali più propensi a causare recidive letali.
Citazione: Nagasawa, S., Kajiya, K., Ishikawa, E. et al. Spatial gene expression analysis reveals drivers of extremely early lymph node metastasis in breast cancer. npj Breast Cancer 12, 28 (2026). https://doi.org/10.1038/s41523-026-00897-1
Parole chiave: metastasi del cancro al seno, linfonodo, transizione epiteliale-mesenchimale, transcrittomica spaziale, metabolismo tumorale