Clear Sky Science · it
La segnalazione CD52 tramite Siglec-G dei macrofagi rappresenta un bersaglio terapeutico per l’immunoterapia del cancro
Perché alcuni tumori al seno si nascondono dal sistema immunitario
Il carcinoma mammario triplo negativo è una delle forme più pericolose di cancro al seno perché si diffonde rapidamente e manca di molti dei bersagli terapeutici comuni. Questo studio esplora un meccanismo recentemente scoperto con cui questi tumori possono eludere le difese dell’organismo e mostra come bloccare quella via di fuga potrebbe rendere più efficaci le terapie basate sul sistema immunitario.
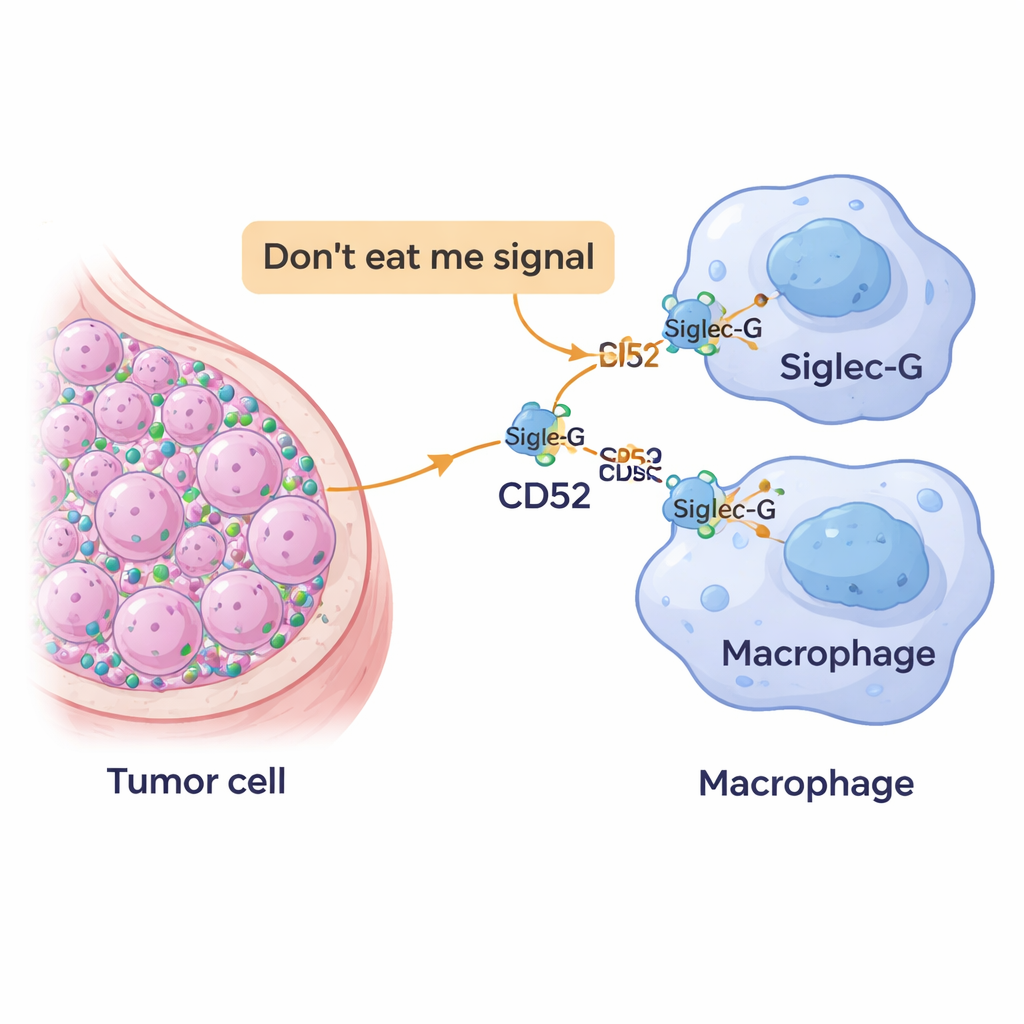
Una nuova “bandiera non mangiarmi” sulle cellule tumorali
Il nostro sistema immunitario si affida a cellule spazzine chiamate macrofagi per pattugliare i tessuti e inglobare cellule pericolose o anomale. Per evitare di essere distrutte per errore, le cellule sane mostrano marcatori di superficie che segnalano, in sostanza, “appartengo qui”. Le cellule tumorali spesso dirottano questo sistema sovrautilizzando tali segnali protettivi, trasformandoli in potenti flag “non mangiarmi”. I ricercatori si sono concentrati su una molecola chiamata CD52, già nota nei tumori del sangue e nelle malattie autoimmuni, e hanno indagato se anche le cellule dei tumori mammari la utilizzino per sfuggire all’attacco dei macrofagi.
Rilevare CD52 nei tumori mammari aggressivi
Il gruppo ha analizzato grandi banche dati pubbliche sul cancro e campioni di tessuto di pazienti. Ha rilevato che i tumori al seno, specialmente quelli triplo negativi, producevano più CD52 rispetto al tessuto mammario normale. Inoltre, i tumori con livelli più elevati di CD52 tendevano a essere meno differenziati, una caratteristica spesso associata a una malattia più aggressiva. Allo stesso tempo, le cellule immunitarie dentro e attorno ai tumori esprimevano alti livelli di una molecola partner chiamata Siglec‑10 (e il suo corrispettivo nei topi Siglec‑G), che si trova sui macrofagi e può inviare segnali calmanti all’interno di queste cellule. Nel complesso, questi schemi suggerivano che CD52 sulle cellule tumorali potesse interagire direttamente con Siglec‑G sui macrofagi per impedire loro di svolgere il proprio compito.
Spegnere CD52 per liberare i macrofagi
Per verificare questa ipotesi, gli scienziati hanno usato strumenti di editing genetico per rimuovere CD52 da cellule di carcinoma mammario triplo negativo murine. Quando queste cellule modificate sono state mescolate con macrofagi in laboratorio, i macrofagi hanno fagocitato in modo significativo più cellule tumorali rispetto a quanto avveniva con cellule tumorali non modificate. È importante che le cellule tumorali stesse non mostravano differenze nella crescita o nella morte dopo la perdita di CD52, indicando che l’effetto chiave riguardava il riconoscimento immunitario più che la biologia intrinseca delle cellule tumorali. Quando le stesse cellule tumorali sono state impiantate in topi, quelle prive di CD52 hanno formato tumori più piccoli ed erano circondate da macrofagi che mostravano maggiori evidenze di aver ingerito cellule tumorali. Se i macrofagi venivano depleti nei topi, questo vantaggio in termini di crescita scompariva, confermando che il ruolo principale di CD52 era proteggere i tumori dall’essere fagocitati.
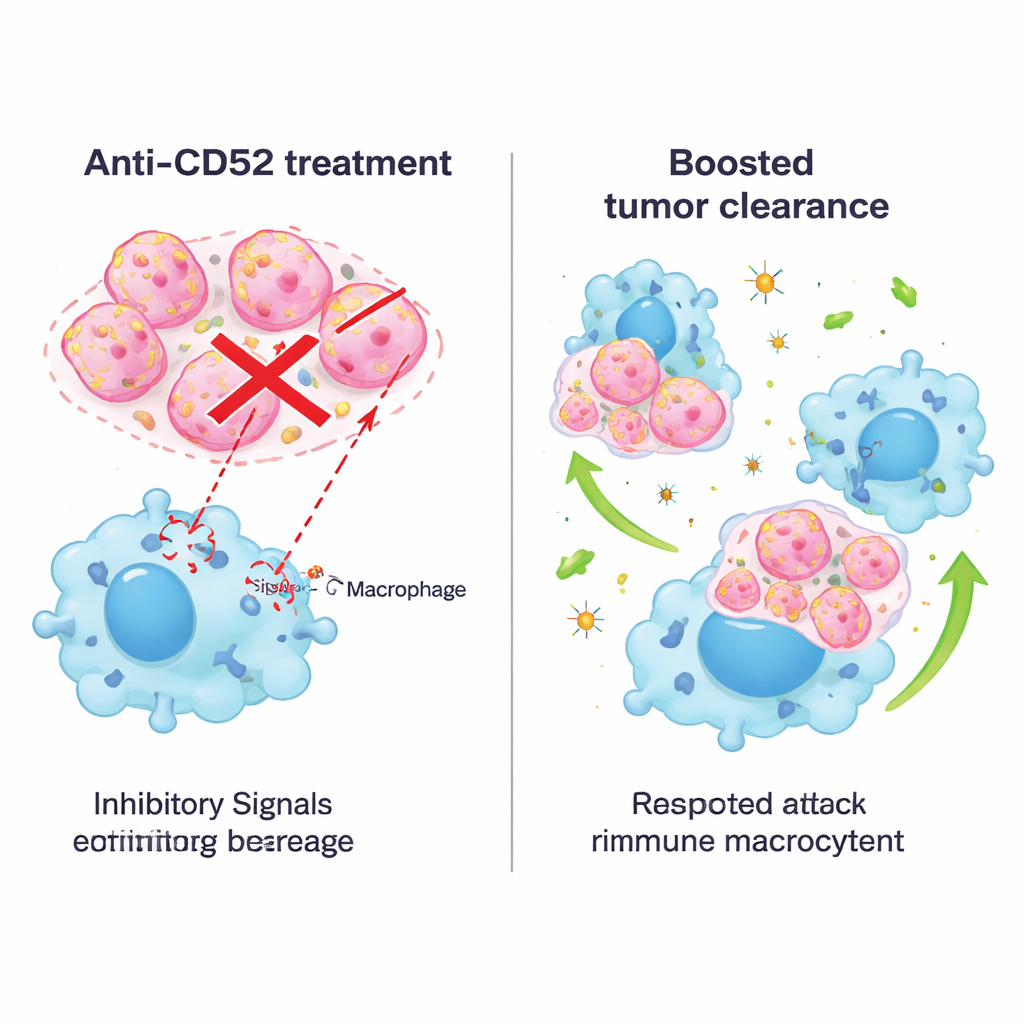
Bloccare il segnale con anticorpi e combinare i trattamenti
Poiché farmaci che prendono di mira CD52 sono già usati in altre malattie, i ricercatori hanno provato un anticorpo bloccante in modelli murini. Il trattamento di topi portatori di tumore con un anticorpo anti‑CD52 ha ridotto la crescita tumorale, prolungato la sopravvivenza e non ha causato danni evidenti agli organi né perdita di peso. In colture, anticorpi simili hanno aumentato la capacità sia dei macrofagi murini sia di quelli umani di inglobare cellule di carcinoma mammario di diversi sottotipi, non solo del triplo negativo. Il gruppo ha poi combinato il blocco di CD52 con la terapia anti‑PD‑1, un farmaco di checkpoint ampiamente usato che agisce sui linfociti T. In un modello spontaneo murino di carcinoma mammario triplo negativo, la combinazione ha funzionato meglio di ciascun trattamento da solo: i tumori si sono ridotti di più, i macrofagi sono diventati più infiammatori e attivi, e più linfociti T con elevata attività citotossica sono entrati nel tumore mentre sono diminuiti i linfociti T esauriti.
Cosa significa per la futura cura del cancro al seno
Questo lavoro identifica CD52 come un segnale “non mangiarmi” precedentemente non riconosciuto che le cellule del carcinoma mammario triplo negativo usano per difendersi dai macrofagi. Interrompendo la comunicazione tra CD52 sulle cellule tumorali e Siglec‑G sui macrofagi, i ricercatori sono riusciti a riattivare sia le cellule immunitarie innate sia, indirettamente, i linfociti T, soprattutto se abbinati al blocco di PD‑1. Pur essendo necessari ulteriori studi di sicurezza e clinici — perché CD52 è presente anche in molte cellule immunitarie normali — i risultati indicano una promettente strategia a doppio checkpoint che potrebbe aiutare a trasformare tumori mammari difficili da trattare e resistenti all’immunità in neoplasie più sensibili all’immunoterapia.
Citazione: Qin, X., Chang, Y., Qiu, Y. et al. CD52 signaling via macrophage Siglec-G represents a therapeutic target for cancer immunotherapy. npj Breast Cancer 12, 29 (2026). https://doi.org/10.1038/s41523-026-00895-3
Parole chiave: carcinoma mammario triplo negativo, macrofagi, immunoterapia, CD52, blocco dei checkpoint