Clear Sky Science · it
Co-consegna della chemochina CXCL9 e del ligando costimolatorio TNFSF9 da parte di cellule staminali mesenchimali riprogramma il microambiente immunitario per il carcinoma mammario triple-negativo
Perché questo nuovo approccio al cancro al seno è importante
Il carcinoma mammario triple-negativo è una delle forme più pericolose di cancro al seno perché cresce rapidamente, si diffonde precocemente e manca dei bersagli ormonali comuni su cui si basano molti farmaci. L’immunoterapia ha alimentato speranze, ma in molti pazienti le cellule difensive dell’organismo semplicemente non penetrano nel tumore in numero sufficiente per fare la differenza. Questo studio esplora una strategia ingegnosa: utilizzare cellule vive come “camion di consegna” guidati che portano segnali che potenziano il sistema immunitario direttamente nei tumori difficili da trattare, potenzialmente rendendo più pazienti eleggibili a trattamenti immunoterapici potenti.
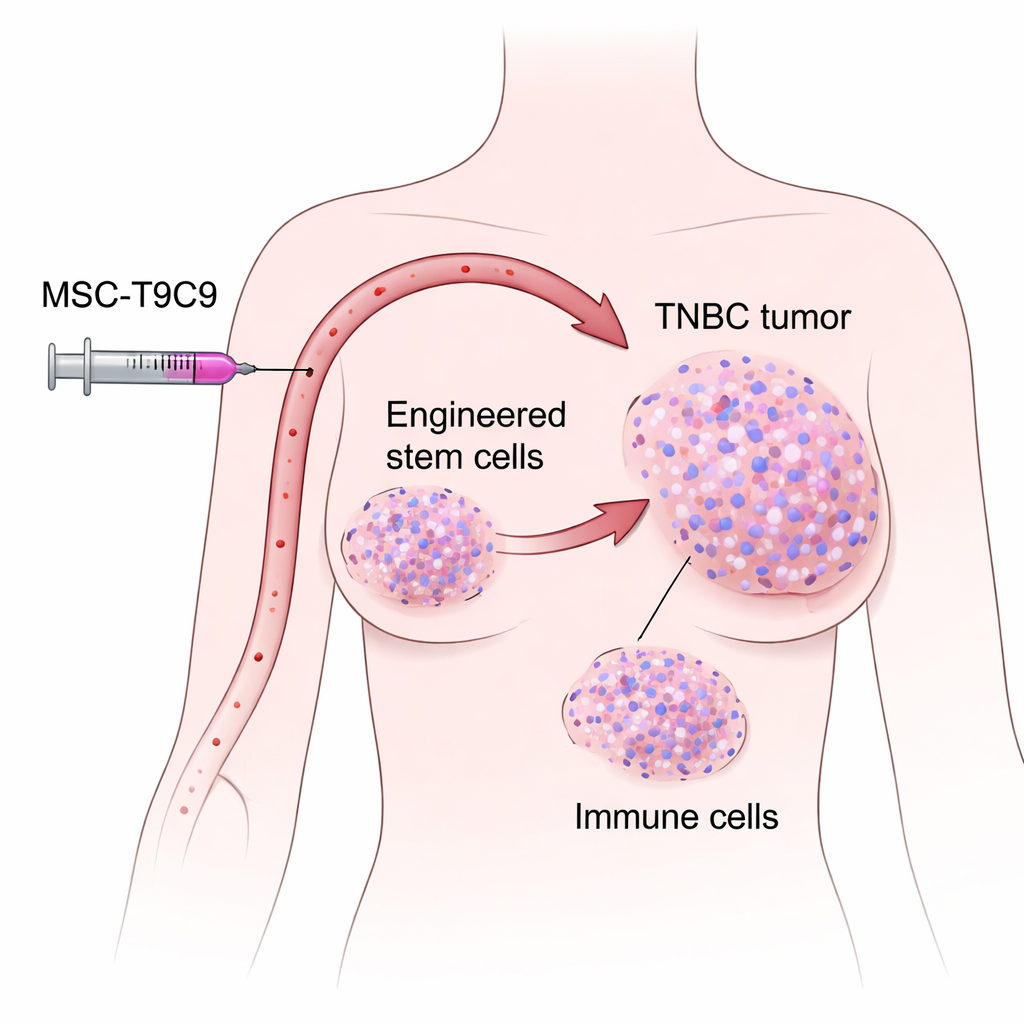
Un cancro difficile con troppo poco aiuto immune
I trattamenti standard per il carcinoma mammario triple-negativo—intervento chirurgico, chemioterapia e radioterapia—spesso non prevengono le recidive, e la sopravvivenza media nelle malattie avanzate resta sotto i due anni. Una ragione chiave è che molti di questi tumori sono “freddi”, cioè contengono poche cellule immunitarie che combattono il cancro. Grandi database di pazienti hanno mostrato che le persone i cui tumori producono naturalmente quantità più elevate di due molecole correlate all’immunità, CXCL9 e TNFSF9, tendono a vivere più a lungo e ad avere più cellule T e cellule natural killer (NK) all’interno dei tumori. CXCL9 è un segnale chimico che richiama le cellule immunitarie nei tessuti, mentre TNFSF9 funziona come un interruttore supplementare che aiuta quelle cellule ad attaccare con maggior forza. Il quadro suggeriva che aumentare entrambi i segnali direttamente all’interno dei tumori potesse inclinare la bilancia a favore del sistema immunitario.
Trasformare le staminali in camion di consegna intelligenti
I ricercatori si sono concentrati su cellule staminali mesenchimali prelevate da cordoni ombelicali umani donati. Queste cellule hanno una proprietà utile: quando iniettate nel flusso sanguigno di topi portatori di tumori mammari, tendono naturalmente a localizzarsi nei siti tumorali e a permanere lì per giorni, evitando in gran parte gli organi normali. Il gruppo ha ingegnerizzato geneticamente queste cellule staminali per rilasciare CXCL9 e mostrare TNFSF9 sulla loro superficie, creando una terapia cellulare a doppio scopo che chiamano MSC‑T9C9. Test di laboratorio hanno dimostrato che le cellule modificate hanno secreto alti livelli di CXCL9 e hanno fortemente attivato le cellule T e le cellule NK murine, senza modificare il loro comportamento di crescita né causare tumori. Ciò le ha rese candidate promettenti come potenziatori immunitari mirati.
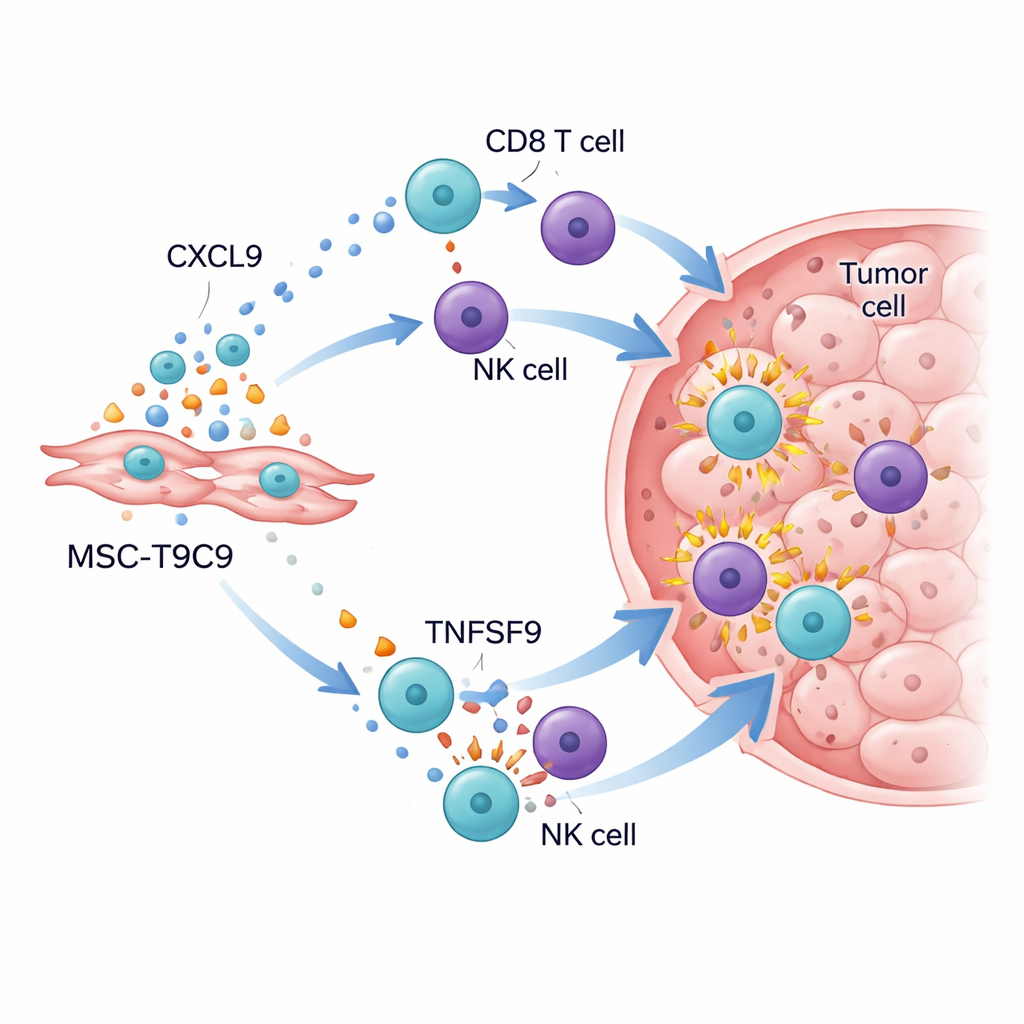
Risvegliare il campo di battaglia immunitario del tumore
Quando le cellule ingegnerizzate sono state somministrate a topi portatori di tumori mammari triple-negativi, i risultati sono stati sorprendenti. Nei topi con un sistema immunitario funzionante, iniezioni ripetute di MSC‑T9C9 hanno notevolmente rallentato la crescita tumorale e aumentato la morte delle cellule cancerose, mentre le cellule staminali di controllo hanno avuto scarso effetto. L’analisi dettagliata dei tumori ha mostrato un aumento drastico del numero di cellule T CD8 “assassine” e di cellule NK, insieme a livelli più elevati di potenti molecole d’attacco come granzima B, interferone‑γ, fattore di necrosi tumorale‑α e interleuchina‑2. Allo stesso tempo, il microambiente tumorale si è spostato da uno stato soppressivo: i macrofagi infiammatori utili sono aumentati e, sebbene le cellule T regolatorie fossero ancora presenti, sono state superate numericamente dalla nuova ondata di combattenti. In topi immunodeficienti, dove mancano T e NK, MSC‑T9C9 non ha rallentato la crescita tumorale, confermando che il suo beneficio dipende dalla mobilitazione delle difese dell’organismo.
Preparare i tumori alla terapia con checkpoint
I farmaci immunoterapici moderni come gli anticorpi anti‑PD‑1 rimuovono i “freni” molecolari dalle cellule T, ma funzionano meglio quando ci sono già abbastanza cellule T all’interno del tumore. Lo studio ha rilevato che MSC‑T9C9 non solo ha attratto più cellule T CD8 nei tumori, ma le ha anche spinte in uno stato altamente attivo, pur sensibile al freno, caratterizzato dal recettore PD‑1. In un modello murino, la combinazione di MSC‑T9C9 con un farmaco anti‑PD‑1 ha prodotto la più marcata riduzione tumorale e la sopravvivenza più lunga rispetto a ciascun trattamento da solo. Le analisi di dataset umani sul cancro hanno supportato questa idea: i pazienti con livelli combinati più alti di TNFSF9 e CXCL9 avevano maggiori probabilità di beneficiare delle terapie di blocco dei checkpoint, suggerendo che la stessa biologia potrebbe applicarsi anche negli esseri umani.
Sicurezza e prospettive future
Qualsiasi trattamento che potenzi l’immunità solleva preoccupazioni riguardo a effetti collaterali pericolosi come infiammazione diffusa o danno agli organi. In modo incoraggiante, i topi che hanno ricevuto MSC‑T9C9 hanno mantenuto peso e comportamento normali, non hanno mostrato lesioni evidenti nei principali organi e hanno avuto esami del sangue e test di fegato‑rene nella norma. È importante che l’impennata di attività immunitaria sia stata in gran parte confinata al tumore stesso e che i segnali infiammatori nel circolo sanguigno non siano aumentati. Sebbene siano necessari ulteriori studi prima di trial umani—inclusi test in modelli più realistici e un accurato studio delle dosi—questo lavoro suggerisce che guidare cellule staminali ingegnerizzate ai tumori per richiamare e attivare le cellule immunitarie potrebbe offrire un modo mirato e più sicuro per trasformare i tumori triple-negativi “freddi” in tumori “caldi” che rispondono meglio all’immunoterapia.
Citazione: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
Parole chiave: carcinoma mammario triple-negativo, immunoterapia, cellule staminali mesenchimali, microambiente tumorale, blocco dei checkpoint