Clear Sky Science · it
Interleuchina-1α derivata dall’ospite guida l’immunosoppressione tumorale riprogrammando le cellule mieloidi tumorali
Perché questa ricerca conta per i pazienti oncologici
L’immunoterapia ha trasformato il trattamento di alcuni tumori, ma molti tumori mammari riescono ancora a eludere il sistema immunitario. Questo articolo esplora un colpevole meno noto: una molecola di segnalazione chiamata interleuchina‑1 alfa (IL‑1α) prodotta non dalle cellule tumorali stesse, ma da cellule normali dell’organismo. Gli autori mostrano che l’IL‑1α di origine ospite può silenziosamente trasformare le cellule immunitarie in alleate del tumore e che bloccare questo segnale nei topi può indurre la riduzione o la scomparsa dei tumori mammari. Comprendere questo interruttore potrebbe aiutare i medici a progettare terapie che rendano l’immunoterapia più efficace per il cancro al seno.
Un influenzatore nascosto nel quartiere tumorale
I tumori non crescono isolati; vivono in un «quartiere» affollato di cellule immunitarie, vasi sanguigni e tessuto connettivo noto come microambiente tumorale. Tra i residenti più importanti vi sono le cellule mieloidi, in particolare i macrofagi, che possono attaccare i tumori o proteggerli. I manuali classici dividono i macrofagi in M1 (antitumorali) e M2 (protettivi per il tumore), ma nei tumori reali esistono molte sfumature intermedie. Gli autori si sono concentrati su IL‑1α, una molecola normalmente prodotta dai tessuti non cancerosi, per chiedersi se questo segnale dell’ospite orienti le cellule mieloidi in ingresso verso ruoli utili o dannosi all’interno dei tumori mammari.
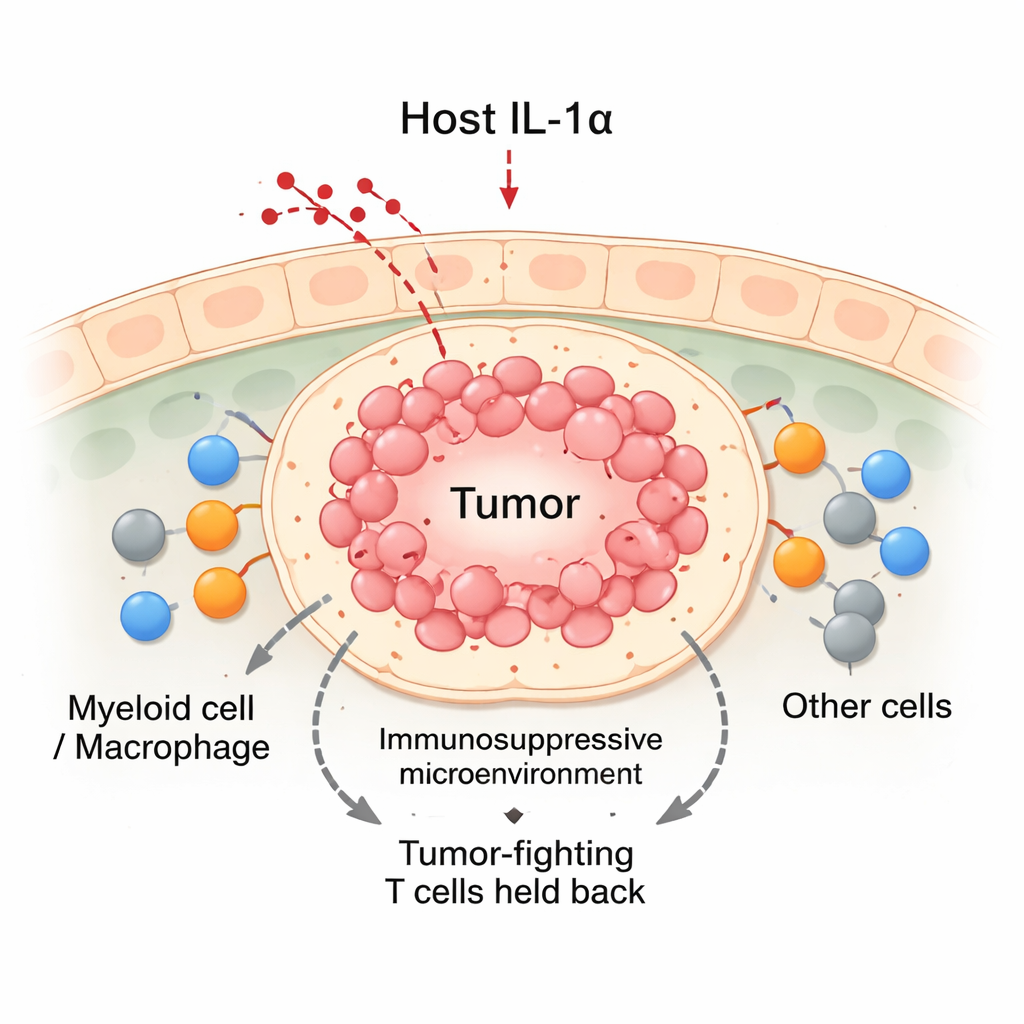
Spegnere l’IL‑1α inclina la bilancia contro i tumori
Usando modelli murini di cancro al seno, il gruppo ha confrontato animali normali con altri ingegnerizzati geneticamente per non esprimere IL‑1α. Quando le cellule tumorali mammarie sono state trapiantate nelle ghiandole mammarie, i tumori nei topi normali crescevano in modo costante. Al contrario, nei topi privi di IL‑1α i tumori crescevano inizialmente per circa due settimane e poi spesso regredivano. Questi tumori in regressione contenevano complessivamente più cellule immunitarie, inclusa un’impennata di cellule T CD8 «killer» e di cellule mieloidi. Sebbene i topi privi di IL‑1α avessero meno leucociti nel sangue circolante, concentravano molte più cellule immunitarie nel sito tumorale. Analisi dettagliate hanno mostrato che le cellule T CD8 infiltranti nei tumori senza IL‑1α erano più attive, producevano livelli più elevati di molecole che uccidono il tumore e mostravano meno segni di esaurimento.
Come l’IL‑1α rimodella le cellule mieloidi associate al tumore
Per capire cosa facesse l’IL‑1α a livello cellulare, i ricercatori hanno utilizzato il sequenziamento dell’RNA a singola cellula per esaminare migliaia di singole cellule provenienti dai tumori. Hanno scoperto che solo un piccolo sottogruppo di macrofagi associati al tumore — quelli caratterizzati da un recettore chiamato CX3CR1 — produceva IL‑1α. Nei topi normali, molti monociti in ingresso maturavano in questi macrofagi CX3CR1‑positivi, collegati a comportamenti immunosoppressivi. Nei topi privi di IL‑1α, questa via di maturazione risultava interrotta. Al contrario, le cellule mieloidi tendevano a diventare macrofagi infiammatori iNOS‑positivi, un profilo associato ad attività antitumorale. Funzionalmente, le cellule mieloidi provenienti da tumori senza IL‑1α erano meno in grado di indurre freni come PD‑1 e CTLA‑4 sulle cellule T e mostravano una capacità più debole di attenuare la proliferazione dei linfociti T.
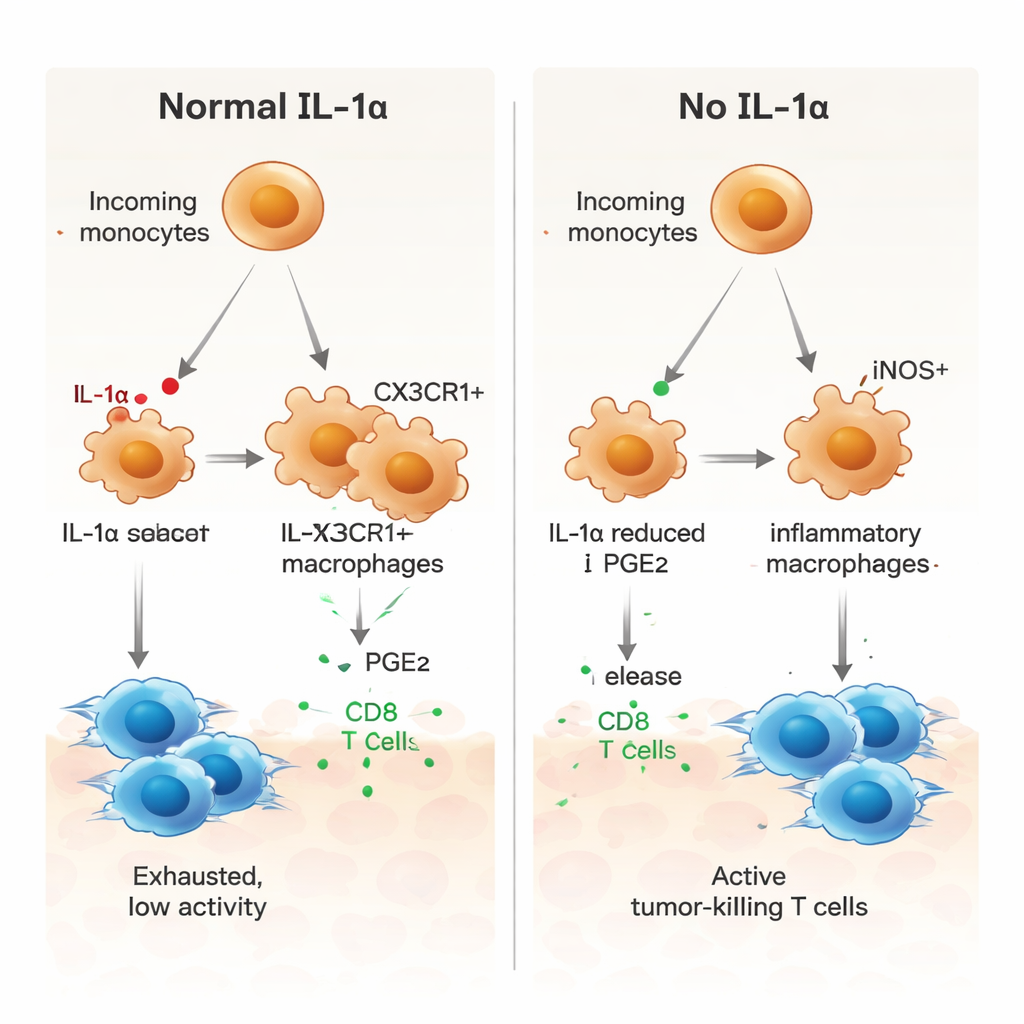
Un ruolo chiave per un messaggero lipidico, la PGE2
Gli autori hanno quindi cercato di capire come l’IL‑1α spinga le cellule mieloidi verso uno stato di supporto al tumore. L’analisi della comunicazione nei dati a singola cellula ha indicato diverse vie di segnalazione, inclusa quella che coinvolge la prostaglandina E2 (PGE2), un mediatore lipidico noto per promuovere l’immunosoppressione. Nei tumori privi di IL‑1α, i macrofagi esprimevano livelli più bassi di recettori per il fattore di crescita dei macrofagi (M‑CSF), dei recettori per TGF‑β e di un recettore per la PGE2, e le cellule stromali vicine producevano meno degli enzimi che sintetizzano la PGE2. In colture di laboratorio, i macrofagi derivati dal midollo osseo di topi privi di IL‑1α mostravano un profilo più infiammatorio, con iNOS più elevato e CX3CR1 più basso. L’aggiunta di PGE2 invertiva questo cambiamento e ristabiliva un modello più soppressivo, mentre il blocco della PGE2 nei macrofagi normali li spingeva verso uno stato pro‑infiammatorio. I macrofagi privi di IL‑1α stimolavano anche in modo più forte la proliferazione delle cellule T CD8 specifiche per il tumore, un effetto attenuato quando la PGE2 veniva reintegrata.
Collegare i risultati nei topi all’immunità umana
Per verificare se i dati murini rispecchiassero la biologia umana, il gruppo ha confrontato le firme geniche dei diversi sottogruppi di macrofagi murini con un ampio pannello di cellule mieloidi umane indotte in vari stati in laboratorio. I cluster di macrofagi provenienti dai tumori nei topi normali somigliavano a cellule umane spinte verso stati di tipo M2, immunosoppressivi, da molecole come IL‑10, IL‑4 e glucocorticoidi. Al contrario, gli stessi cluster dai tumori privi di IL‑1α corrispondevano a cellule umane in condizioni più infiammatorie e meno soppressive. In particolare, i pattern genici legati alla segnalazione di PGE2 erano arricchiti nei macrofagi dipendenti da IL‑1α ma assenti quando l’IL‑1α mancava, rafforzando l’idea che IL‑1α e PGE2 collaborino per costruire una nicchia immunosoppressiva.
Cosa potrebbe significare per le future terapie del cancro al seno
In termini semplici, questo studio suggerisce che una molecola di origine ospite, l’IL‑1α, può silenziosamente dire ad alcuni macrofagi di proteggere il tumore e tenere sotto controllo le cellule T killer, in parte attraverso la segnalazione PGE2. Quando l’IL‑1α viene rimossa nei topi, i macrofagi si spostano verso uno stato più infiammatorio e anticancro, le cellule T CD8 diventano più attive e i tumori mammari trapiantati sono spesso respinti. Poiché le immunoterapie attuali mirano già a rivitalizzare le cellule T esauste, combinarle con approcci che bloccano l’IL‑1α o la sua via PGE2 a valle potrebbe ulteriormente orientare il microambiente tumorale a favore del sistema immunitario del paziente. Pur richiedendo ulteriori studi per testare sicurezza ed efficacia negli esseri umani, questi risultati evidenziano l’IL‑1α come un nuovo e promettente bersaglio per rendere il cancro al seno più vulnerabile all’attacco immunitario.
Citazione: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
Parole chiave: immunoterapia del cancro al seno, microambiente tumorale, macrofagi, interleuchina-1 alfa, prostaglandina E2