Clear Sky Science · it
Regolazione microbica delle molecole segnalanti associate allo stress e il suo ruolo nella salute e nella malattia
Come i minuscoli inquilini intestinali plasmano il nostro stress
La maggior parte di noi pensa allo stress come a qualcosa che accade nella testa, ma questo articolo mostra che alcuni dei protagonisti più importanti della nostra risposta allo stress vivono nell’intestino. I microbi che abitano il nostro intestino fanno molto più che aiutare la digestione: possono sintetizzare, degradare e rimodellare gli stessi ormoni che controllano come il corpo reagisce a pressione, paura e dolore. Comprendere questa partnership nascosta può aprire nuove vie per alleviare condizioni come la malattia infiammatoria intestinale, la depressione e altre malattie collegate allo stress.
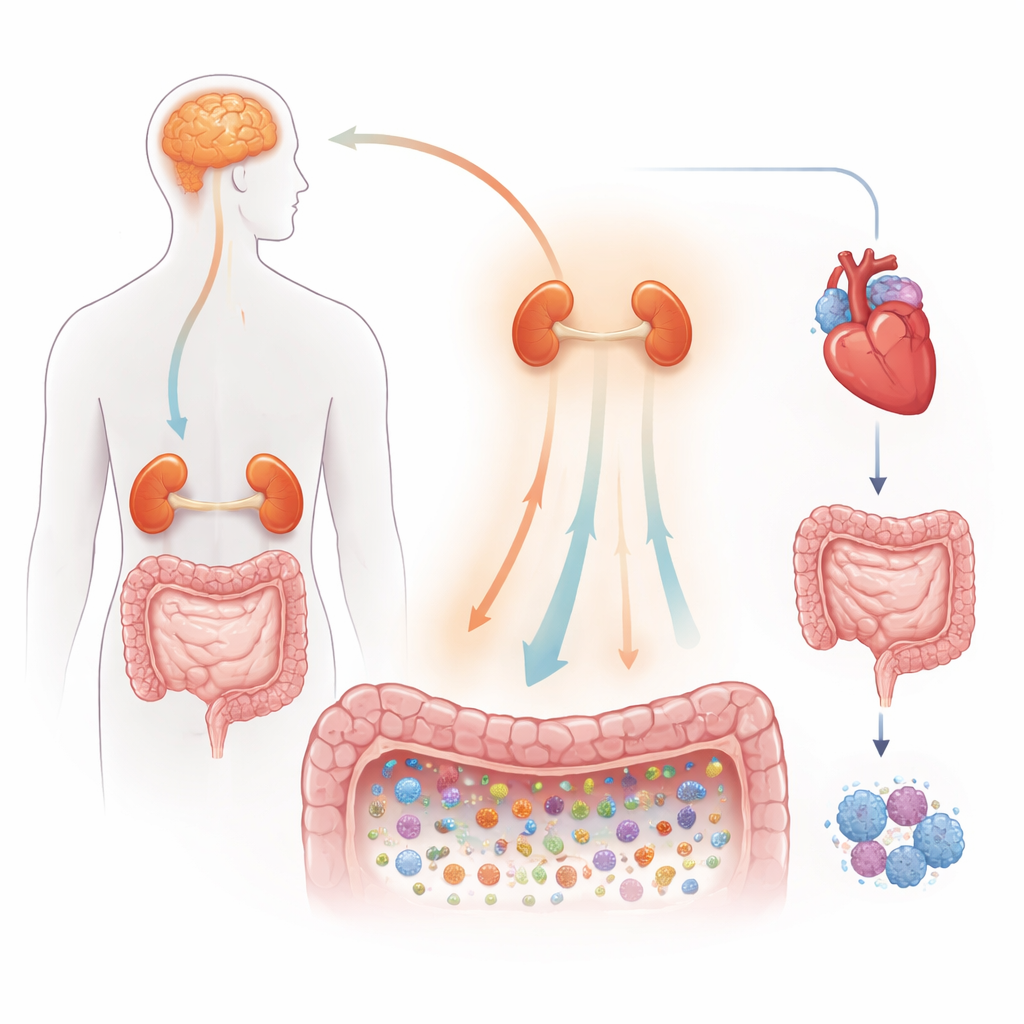
Il sistema d’allarme integrato del corpo
Gli autori iniziano delineando come funziona normalmente la risposta allo stress. Quando affrontiamo una sfida, il cervello attiva una catena di comando che coinvolge ipofisi e ghiandole surrenali, inondando il corpo di messaggeri chimici come le catecolamine simili all’adrenalina e gli ormoni steroidei chiamati glucocorticoidi. Questi segnali aumentano la frequenza cardiaca, ridistribuiscono il flusso sanguigno, modificano la motilità intestinale e regolano il sistema immunitario per la “lotta o fuga”. I nervi che innervano direttamente il tratto digestivo forniscono una via veloce per portare segnali all’intestino, stringendo o rilassando la barriera intestinale e alterando l’ambiente locale in cui vivono i microbi. Questo rende l’intestino un crocevia chiave dove biologia dello stress e microbioma si incontrano continuamente.
I microbi che ascoltano e parlano i segnali dello stress
La ricerca condotta in diversi decenni rivela che molti batteri possono percepire e usare i nostri composti legati allo stress. Esperimenti precoci mostrarono che alcuni batteri intestinali e patogeni crescono più velocemente e diventano più aggressivi se esposti a catecolamine come norepinefrina ed epinefrina. Altri studi dimostrarono che i batteri possono assorbire queste molecole, convertirle in nuove forme o persino produrre composti simili a partire da aminoacidi come la tirosina. Allo stesso tempo, gli enzimi dell’ospite spesso “spengono” le catecolamine legando piccoli gruppi chimici ad esse; i batteri intestinali dotati degli strumenti adatti possono staccare di nuovo questi gruppi, ripristinando la forma attiva. Nei topi privi di microbi, molti mediatori dello stress nell’intestino rimangono nella forma inattiva, ma l’introduzione di batteri specifici ripristina il pool attivo, mostrando che i microbi controllano direttamente quanto questi segnali siano disponibili.
Rimodellare gli steroidi dello stress dall’interno
La rassegna si concentra poi sui glucocorticoidi, gli ormoni steroidei noti per attenuare l’infiammazione e aiutare l’organismo a fronteggiare lo stress prolungato. Piccole quantità di questi ormoni entrano nell’intestino dal flusso sanguigno o vengono prodotte localmente nell’epitelio intestinale, dove incontrano comunità batteriche dense. Molti microbi intestinali possiedono enzimi specializzati che possono tagliare, riorganizzare o ridurre queste molecole steroidee. Alcuni rimuovono catene laterali trasformandole in androgeni, che agiscono più come ormoni sessuali e possono influenzare la pressione sanguigna e persino tumori sensibili agli ormoni. Altri eliminano gruppi chimici particolari, indebolendo la capacità dell’ormone di legare il suo recettore, o riducono ulteriormente la struttura impedendone il riciclo in forme potenti. Altri ancora invertiscono i passaggi di “inattivazione” dell’organismo rimuovendo gruppi solfato o zuccherini attaccati, riportando gli steroidi in circolazione nella forma attiva. Insieme, queste azioni fanno del microbioma una manopola di controllo dinamica sulla potenza e sull’equilibrio degli steroidi.
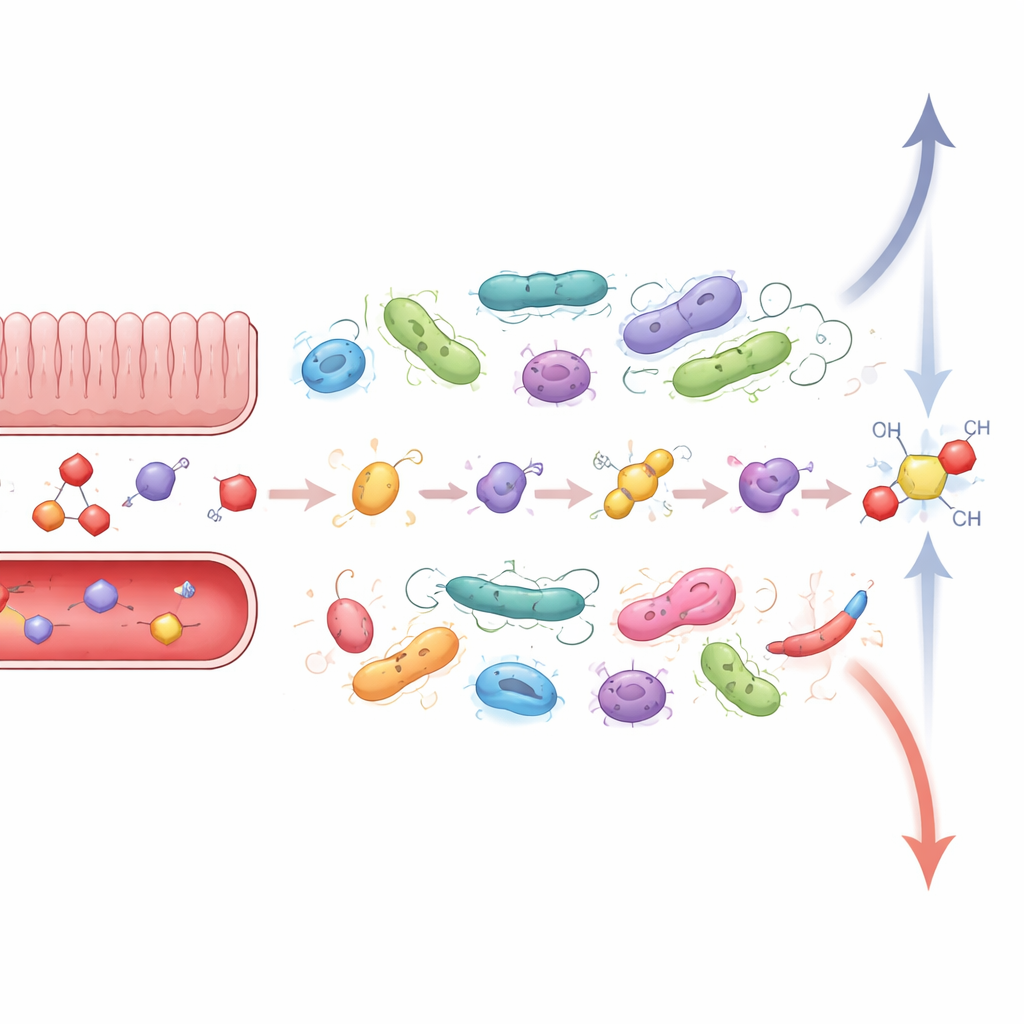
Quando stress, infiammazione e microbi si alimentano a vicenda
Questi scambi chimici intimi sono più rilevanti nelle malattie in cui sia lo stress sia i microbi intestinali sono già alterati. La malattia infiammatoria intestinale (MII) è un esempio tipico: i pazienti mostrano infiammazione intestinale cronica, comunità microbiche alterate e una maggiore sensibilità allo stress della vita. Gli ormoni dello stress possono allentare la barriera intestinale, permettendo a più microbi e ai loro prodotti di attraversarla e stimolare il sistema immunitario. Allo stesso tempo, la MII è associata a proliferazioni di specie che possono rimodellare il cortisolo e steroidi correlati, così come a perdite di batteri che producono acidi grassi a catena corta, piccoli prodotti della fermentazione che normalmente aiutano a sigillare la barriera e calmare l’infiammazione. Studi su animali suggeriscono che questi spostamenti microbici possono amplificare gli squilibri ormonali e l’attività immunitaria, intrappolando i pazienti in un circolo vizioso in cui lo stress aggrava la malattia intestinale e la malattia intestinale aumenta lo stress.
Nuove vie per calmare il circuito intestino–stress
Poiché i microbi si trovano all’incrocio tra segnali di stress e infiammazione, rappresentano bersagli attraenti per nuove terapie. L’articolo evidenzia lavori che mostrano come diete ricche di fibre come l’inulina possano aumentare i prodotti della fermentazione benefici, ridurre l’infiammazione intestinale e attenuare alcuni danni legati allo stress nei modelli di MII. Ceppi probiotici di Lactobacillus sono stati trovati in grado di rinforzare la barriera intestinale, ridurre i picchi ormonali indotti dallo stress e abbassare la sensibilità al dolore negli animali. La somministrazione diretta di acidi grassi a catena corta al colon può ridurre comportamenti simili all’ansia nei topi e attenuare le risposte del cortisolo allo stress sociale negli esseri umani. Questi successi iniziali suggeriscono che probiotici, prebiotici e metaboliti microbici progettati con cura potrebbero aiutare a ripristinare la risposta allo stress rimodellando la gestione degli ormoni nell’intestino.
Cosa significa questo per la salute quotidiana
In conclusione, gli autori sostengono che i microbi intestinali dovrebbero essere considerati partner attivi nella nostra biologia dello stress, non spettatori passivi. Facendo, modificando e riciclando le molecole segnalanti legate allo stress, il microbioma può influenzare quanto intensamente reagiamo alle sfide, quanto rapidamente ci riprendiamo e quanto è probabile che lo stress ci spinga verso malattie croniche. Questo non significa che un singolo “microbo magico” curerà lo stress, ma suggerisce che proteggere e coltivare un ecosistema intestinale sano può essere uno degli strumenti più potenti che abbiamo per costruire resilienza. Man mano che i ricercatori mappano in maggiore dettaglio queste interazioni microbo–ormone e le testano negli esseri umani, strategie quotidiane che supportano la salute intestinale potrebbero diventare una parte centrale della gestione dello stress, dell’umore e delle condizioni infiammatorie.
Citazione: Sie, C., Tropini, C. Microbial regulation of stress-associated signaling molecules and its role in health and disease. npj Biofilms Microbiomes 12, 65 (2026). https://doi.org/10.1038/s41522-026-00932-w
Parole chiave: microbioma intestinale, ormoni dello stress, asse microbiota-intestino-cervello, malattia infiammatoria intestinale, endocrinologia microbica