Clear Sky Science · it
Eliminazione mirata delle infezioni da mastite da Staphylococcus aureus con sistemi di consegna CRISPR-Cas basati su fagi sintetici
Combattere un’infezione costosa per il settore lattiero-caseario
Il latte di vacche e altri animali da allevamento può essere compromesso da un doloroso processo infiammatorio della mammella chiamato mastite, spesso causato dal batterio Staphylococcus aureus. Il trattamento di queste infezioni richiede tipicamente cicli prolungati di antibiotici, che sono costosi, stressanti per gli animali e contribuiscono al crescente problema della resistenza agli antibiotici. Questo studio esplora un approccio radicalmente diverso: trasformare un parassita naturale simile a un virus dei batteri in un’arma di precisione in grado di tagliare selettivamente il DNA batterico e risanare le infezioni senza diffondere geni di resistenza.
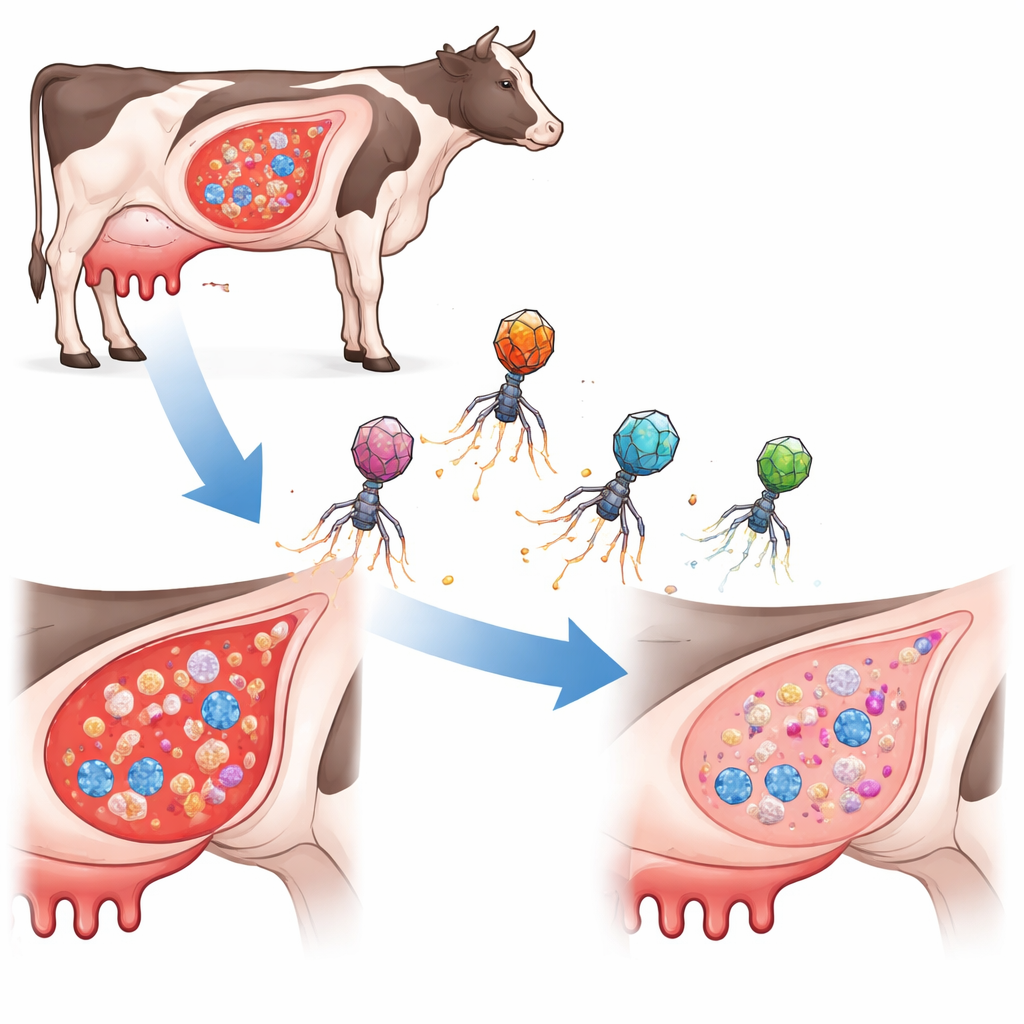
Un nuovo tipo di cacciatore batterico mirato
Invece di usare antibiotici tradizionali o batteriofagi ordinari (virus che infettano i batteri), i ricercatori hanno ingegnerizzato piccoli elementi portatori di DNA noti come isole cromosomiche indotte dai fagi. In natura, queste isole viaggiano all’interno di involucri fagici per saltare tra le cellule batteriche. Qui, il team le ha ricostruite come “ePICI” che trasportano lo strumento di editing genico CRISPR‑Cas9 più brevi sequenze guida rivolte a tre piccoli ma importanti RNA regolatori di S. aureus. Quando un ePICI entra in una cellula target, viene prodotto Cas9 che taglia il cromosoma batterico nel sito scelto, uccidendo la cellula dall’interno. È fondamentale che queste particelle ingegnerizzate non si replicano da sole, il che limita la loro diffusione e riduce il rischio di trasferire accidentalmente geni dannosi.
Come lo scudo batterico cambia la battaglia
S. aureus spesso sopravvive ai trattamenti formando biofilm—comunità appiccicose in cui le cellule sono immerse in una matrice auto‑prodotta. Il team ha confrontato due tipi comuni di matrice: una costruita principalmente da una proteina chiamata Bap e un’altra composta da un polimero zuccherino noto come PIA/PNAG. Nei test di laboratorio, i biofilm ricchi di Bap proteggevano fortemente i batteri dagli ePICI e da un fago helper standard, comportandosi come un’armatura densa che bloccava l’infezione. Al contrario, i biofilm basati sul polimero zuccherino rendevano i batteri più facilmente eliminabili, probabilmente perché gli enzimi presenti sulle proteine della capsula virale possono degradare questi zuccheri e aiutare le particelle a raggiungere i loro bersagli.
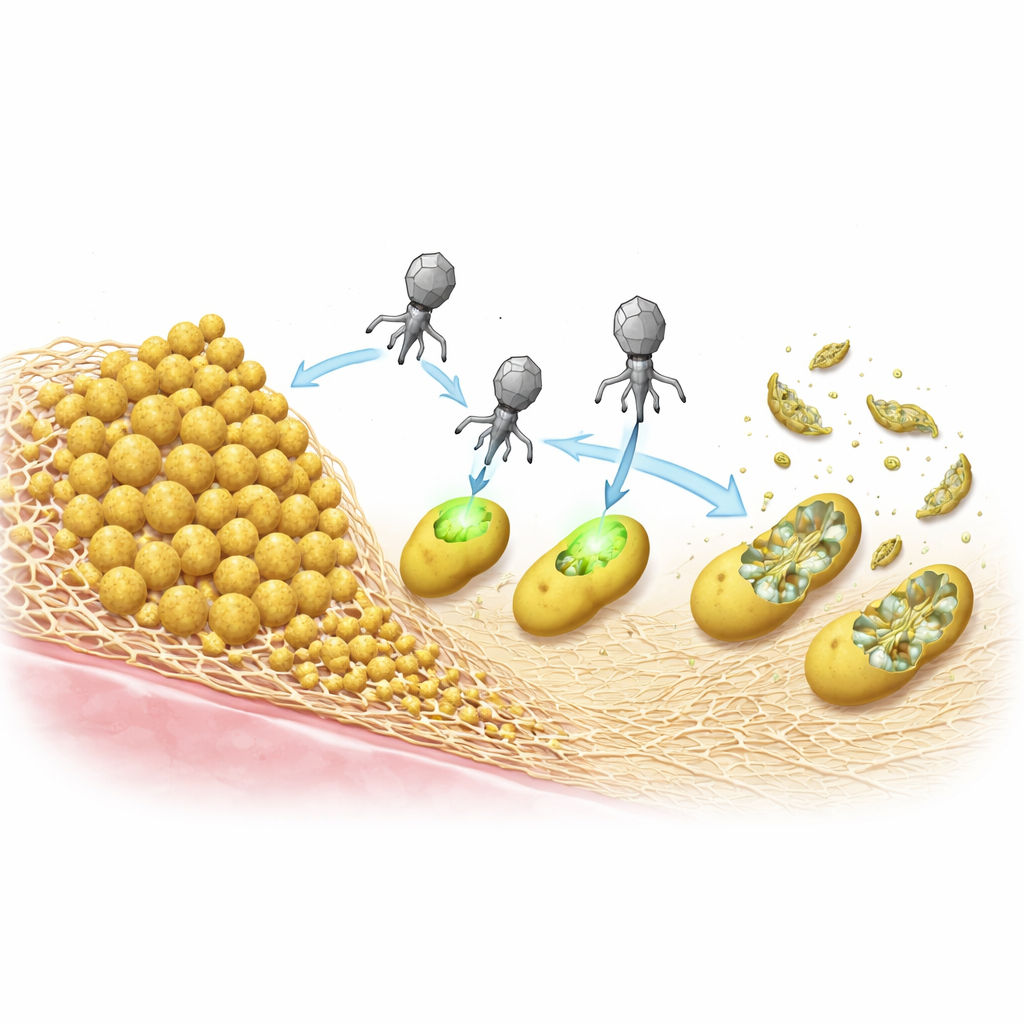
Uccidere i batteri senza incorporare il loro DNA
Una volta all’interno della cellula, gli ePICI possono integrarsi nel cromosoma batterico, ma i ricercatori si sono chiesti se quel passaggio sia effettivamente necessario per uccidere. Hanno creato una versione incapace di integrarsi e hanno dimostrato che, purché la particella fosse prodotta correttamente nel ceppo sorgente, era altrettanto letale per S. aureus quanto l’originale. Ciò significa che il sistema CRISPR può essere espresso direttamente dal DNA circolare in arrivo, svolgere la sua funzione e poi andare perso con la morte della cellula. Questa azione priva di integrazione riduce ulteriormente le possibilità di trasferimento genico non intenzionale e distingue queste particelle dalla terapia con fagi classica, che si basa sulla replicazione virale e sulla lisi cellulare per diffondersi.
Dalla piastra di Petri alle ghiandole mammarie infette
Poiché i ceppi produttori di Bap sono comuni nella mastite lattiera, il team ha testato il loro costrutto con le migliori prestazioni, chiamato ePICIrsaE, in un modello murino che imita l’infezione della mammella. Nel latte e nelle colture di laboratorio, i biofilm ricchi di Bap riducevano chiaramente l’attività dell’ePICI. Eppure all’interno della ghiandola mammaria, dosi ripetute di ePICIrsaE hanno ridotto drasticamente il numero di batteri per tutti i ceppi testati, inclusi quelli che producevano Bap. Le sue prestazioni sono state comparabili a quelle della vancomicina, un potente antibiotico di ultima risorsa. I risultati suggeriscono che le condizioni nei tessuti viventi—come una minore produzione di Bap, la presenza di batteri liberi in sospensione o componenti del latte favorevoli—permettono alle particelle ingegnerizzate di funzionare molto meglio rispetto ai biofilm statici in laboratorio.
Cosa potrebbe significare per le aziende agricole e oltre
Lo studio dimostra che sistemi CRISPR incapsulati in fagi e non replicanti possono eliminare selettivamente S. aureus in un’infezione difficile associata a biofilm senza auto‑diffondersi o provocare la lisi massiva di cellule. Sebbene siano necessarie dosi elevate di particelle e il passaggio da modelli murini a bovini presenti sfide, queste particelle offrono un’alternativa promettente e controllabile agli antibiotici per infezioni localizzate come la mastite. Più in generale, il lavoro sottolinea che trattamenti che sembrano deludenti in semplici test di laboratorio possono comunque avere successo nell’ambiente complesso di un organismo animale e apre la strada a librerie di ePICI personalizzate tarate su diversi batteri, involucri virali e sequenze guida.
Citazione: Garmendia-Antoñana, N., Dorado-Morales, P., Gil, C. et al. Targeted elimination of Staphylococcus aureus mastitis infections with synthetic phage-based CRISPR-Cas delivery systems. npj Biofilms Microbiomes 12, 67 (2026). https://doi.org/10.1038/s41522-026-00931-x
Parole chiave: mastite bovina, Staphylococcus aureus, terapia CRISPR, trattamento basato su fagi, infezioni da biofilm