Clear Sky Science · it
La via regolatoria ppGpp-HpaR1-gum modula la produzione di esopolisaccaridi in Xanthomonas campestris pv. campestris
Perché batteri «appiccicosi» sono importanti per le colture
Molti batteri patogeni sopravvivono e si diffondono avvolgendosi in involucri vischiosi di zuccheri noti come biofilm. Nelle colture orticole come cavoli e broccoli, questi rivestimenti possono ostruire i condotti d’acqua delle piante, causando la nota malattia della «ruggine nera» e gravi perdite di produzione. Questo studio esplora un batterio di questo tipo, Xanthomonas campestris, per rivelare come un sistema di allarme chimico interno controlli la produzione del suo scudo zuccherino. Comprendere questo circuito di controllo nascosto potrebbe aiutare gli scienziati a progettare modi migliori per proteggere le colture o persino a sfruttare questi zuccheri per materiali utili.
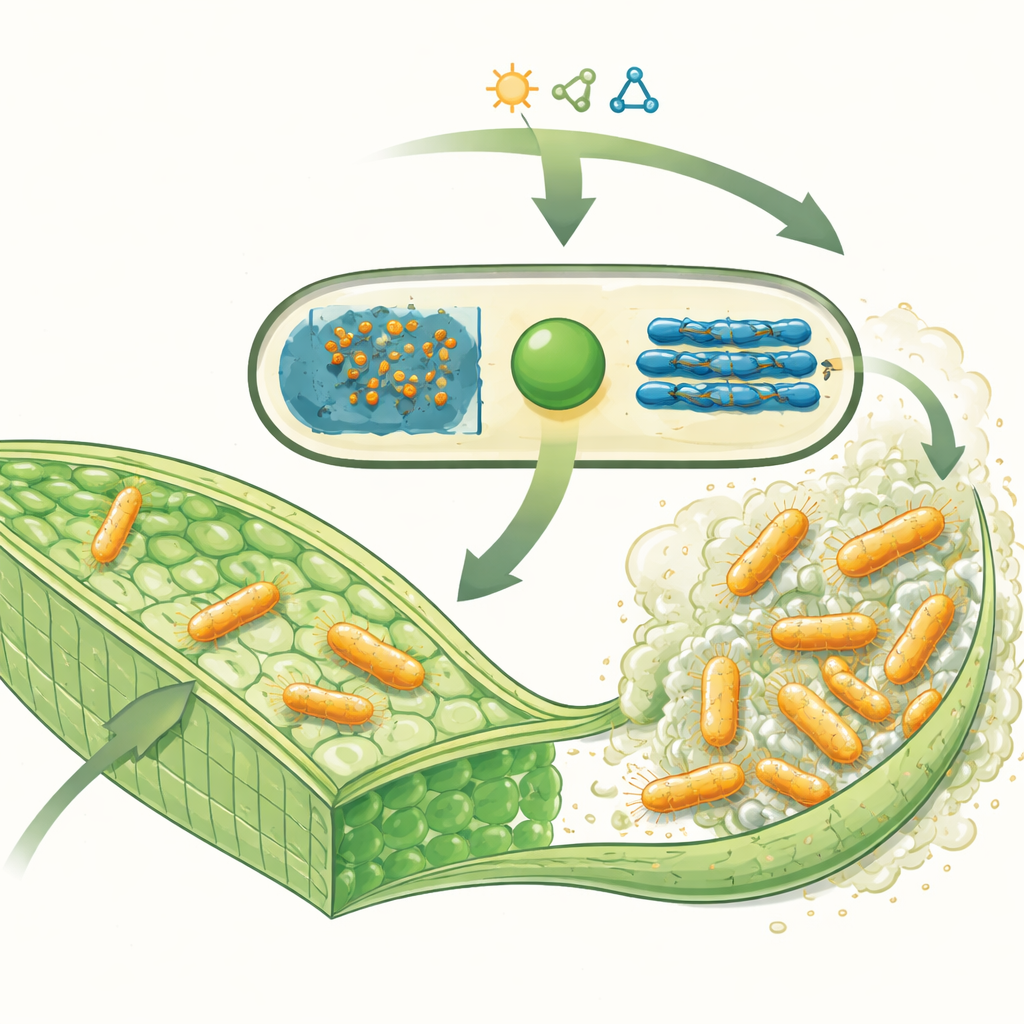
Il microbo che infetta le piante e il suo’armatura zuccherina
Xanthomonas campestris penetra nelle vene delle crucifere — piante come cavolo, cavolfiore e senape — e produce grandi quantità di una sostanza vischiosa chiamata xanthan gum. Questo materiale è costituito da lunghe catene di unità zuccherine e rappresenta una parte importante del biofilm che aiuta i batteri ad aderire ai tessuti vegetali, resistere alle difese della pianta e sopravvivere in condizioni avverse. Nella pianta, questi spessi strati zuccherini possono bloccare il flusso d’acqua, portando a tessuti necrotici e alle caratteristiche lesioni a forma di V sulle foglie tipiche della ruggine nera. Curiosamente, la stessa xanthan gum è ampiamente utilizzata come addensante negli alimenti e in altri prodotti, rendendo questo zucchero batterico sia un nemico agricolo sia una risorsa industriale.
Un allarme interno che modella il comportamento batterico
All’interno di molti batteri, una piccola molecola segnale chiamata ppGpp funziona come un allarme d’emergenza. Quando le risorse nutritive scarseggiano o sorgono altri stress, i livelli di ppGpp aumentano e innescano una vasta «risposta stringente» che rimodella crescita, metabolismo e strategie di sopravvivenza. Studi precedenti hanno mostrato che ppGpp può favorire la formazione di biofilm in diverse specie e che la sua rimozione in Xanthomonas indebolisce la capacità del batterio di formare biofilm e causare malattia. Ciò che restava poco chiaro era come questa minuscola molecola si collegasse concretamente alla macchina che costruisce lo spesso rivestimento di esopolisaccaride (EPS) in questo specifico patogeno delle piante.
Tracciare il percorso dal segnale allo zucchero
I ricercatori hanno confrontato batteri normali con mutanti incapaci di sintetizzare ppGpp. Su piastre ricche di zucchero, i mutanti privi di ppGpp formavano colonie più piccole e meno mucose, e misurazioni dirette hanno mostrato che producevano quantità significativamente inferiori di EPS. Tuttavia, l’impronta chimica ottenuta mediante spettroscopia infrarossa e le immagini al microscopio elettronico hanno rivelato che la composizione di base e l’architettura di ordine superiore dell’EPS rimanevano le stesse: i mutanti semplicemente ne producevano meno. L’attenzione si è quindi rivolta al cluster genico «gum», un gruppo di geni che codificano gli enzimi che assemblano la xanthan gum. Attraverso misure di espressione genica e sequenziamento RNA, il team ha rilevato che quasi tutti i geni gum risultavano downregolati nelle cellule carenti di ppGpp, collocando ppGpp a monte di questo cluster nella gerarchia di controllo.
Un mediatore chiave: l’interruttore HpaR1
Tra l’allarme ppGpp e i geni gum si trova una proteina regolatoria chiamata HpaR1, un fattore di trascrizione che si lega al DNA e potenzia l’attività dei geni gum. Lo studio ha mostrato che ppGpp interviene su due fronti. Primo, le cellule prive di ppGpp presentavano livelli ridotti dell’attività del gene hpaR1, il che significa che era disponibile meno proteina HpaR1. Secondo, in prove di laboratorio con proteine purificate, l’aggiunta di ppGpp rafforzava direttamente l’aderenza di HpaR1 alle regioni del DNA che controllano i geni gum e persino alla sua stessa regione di controllo. A livelli moderati di ppGpp questo legame risultava chiaramente potenziato, sebbene livelli estremamente elevati ne indebolissero in parte l’effetto, suggerendo un equilibrio finemente regolato. Quando gli scienziati aumentarono artificialmente i livelli di HpaR1, la produzione di EPS tornò ad aumentare — anche nei batteri privi di ppGpp — confermando che HpaR1 è il mediatore cruciale tra il segnale d’allarme e la macchina produttrice di zuccheri.
Cosa significa questo circuito di controllo per le colture e oltre
In termini semplici, questo lavoro svela un sistema a tre passaggi all’interno di un patogeno delle piante: una molecola di allarme interna (ppGpp) aumenta e rafforza un interruttore legante il DNA (HpaR1), che a sua volta aumenta l’attività di una fabbrica di zuccheri (i geni gum), portando a un rivestimento protettivo più spesso di muco intorno ai batteri. Mappando in dettaglio la via ppGpp–HpaR1–gum, lo studio spiega come segnali ambientali di stress possano essere convertiti in cambiamenti nella produzione della matrice del biofilm. Per agricoltori e scienziati delle piante, queste intuizioni suggeriscono nuovi bersagli per interrompere l’armatura del batterio e ridurre i danni da ruggine nera. Per i microbiologi in generale, i risultati aggiungono un tassello importante al quadro di come segnali di stress universali controllino la formazione di comunità microbiche complesse.
Citazione: Bai, K., Xu, X., Yu, C. et al. The ppGpp-HpaR1-gum regulatory pathway modulates exopolysaccharides production in Xanthomonas campestris pv. campestris. npj Biofilms Microbiomes 12, 60 (2026). https://doi.org/10.1038/s41522-026-00926-8
Parole chiave: biofilm batterici, agenti patogeni delle piante, xanthan gum, segnalazione dello stress, esopolisaccaridi