Clear Sky Science · it
Caratterizzazione metabolica in tempo reale e ad alta risoluzione di batteri vivi mediante imaging ottico metabolico senza marcatori
Osservare i germi reagire in tempo reale
I batteri sono ovunque, dentro e sopra di noi, e influenzano silenziosamente la nostra salute. Aiutano a digerire il cibo, proteggono la pelle e talvolta causano infezioni ostinate che resistono agli antibiotici. Questo studio introduce un modo per osservare i batteri vivi mentre reagiscono a stress e farmaci in tempo reale, a livello della singola cellula, senza aggiungere coloranti o marcatori. Questa capacità potrebbe alla fine aiutare i medici a scegliere il trattamento giusto più rapidamente e consentire agli scienziati di capire perché alcune infezioni sono così difficili da curare.
La luce come finestra sulla vita batterica
Invece di aggiungere coloranti o tag genetici, i ricercatori sfruttano il fatto che i batteri emettono naturalmente un flebile bagliore quando certe molecole al loro interno vengono eccitate da un raggio laser. Due di queste molecole, note come NAD(P)H e FAD, sono attori centrali nel modo in cui le cellule trasformano il cibo in energia. Usando microscopia laser rapida e ad alta risoluzione, il team può misurare sia l’intensità sia il piccolo ritardo temporale di questo bagliore, rivelando quanto è attivo il metabolismo di una cellula. Poiché il metodo è senza marcatori e non distruttivo, gli stessi batteri vivi possono essere seguiti per secondi e minuti mentre il loro ambiente cambia. 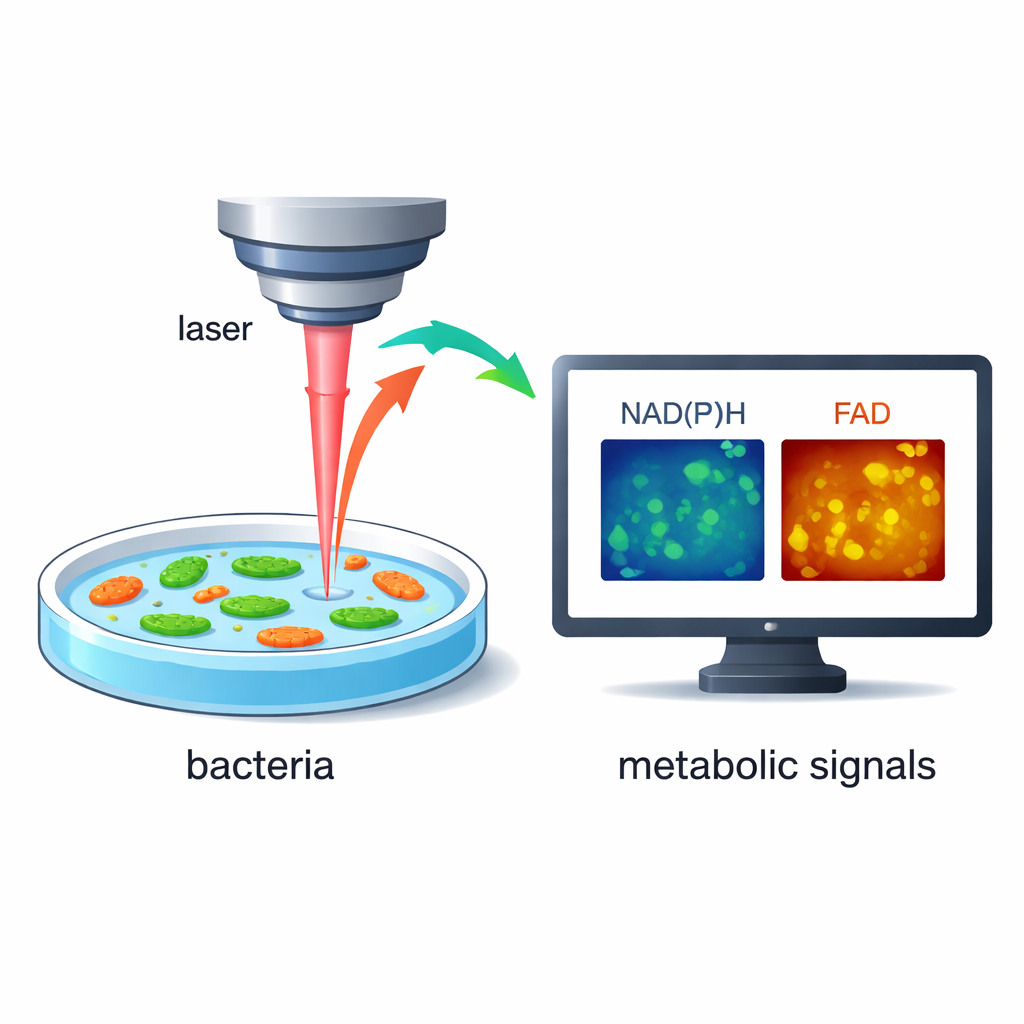
Vedere le differenze tra singoli batteri
La maggior parte dei test di laboratorio standard aggrega milioni di batteri e fornisce solo una risposta media. Qui, gli autori mostrano che il loro metodo di imaging può identificare singole cellule di Staphylococcus aureus in coltura liquida e analizzarle separatamente, anche ad alte densità cellulare. Quando hanno confrontato due colonie di S. aureus cresciute nelle stesse condizioni, un segnale chiave (derivato da FAD) differiva tra le colonie, e all’interno di ciascuna colonia c’era una distribuzione di valori. Questo significa che anche batteri geneticamente simili nello stesso flacone possono trovarsi in stati metabolici molto diversi, una diversità nascosta che i test di massa potrebbero non rilevare ma che può influire su come le infezioni rispondono al trattamento.
Osservare gli antibiotici all’opera in pochi secondi
Il team ha poi seguito singole cellule di S. aureus mentre venivano esposte a vari trattamenti antibatterici, compresi antibiotici di uso comune e la candeggina domestica. Con il loro sistema di imaging veloce, hanno catturato i cambiamenti dal momento in cui la soluzione del farmaco ha toccato le cellule fino ai successivi 30 minuti. I trattamenti più intensi hanno fatto calare i segnali di NAD(P)H e salire quelli di FAD, spesso entro pochi secondi, riflettendo un arresto della produzione di energia e uno spostamento verso uno stato più ossidato all’interno della cellula. I tempi e i modelli esatti di questi cambiamenti dipendevano dal tipo e dalla dose del farmaco: per esempio, antibiotici che bloccano la sintesi proteica o quelli che mirano la parete cellulare hanno prodotto un breve calo seguito da una parziale ripresa, mentre la candeggina ha indotto uno spostamento netto e sostenuto. Queste distinte “firme luminose” suggeriscono che la tecnica può percepire non solo se le cellule sono stressate o morenti, ma anche come vengono danneggiate. 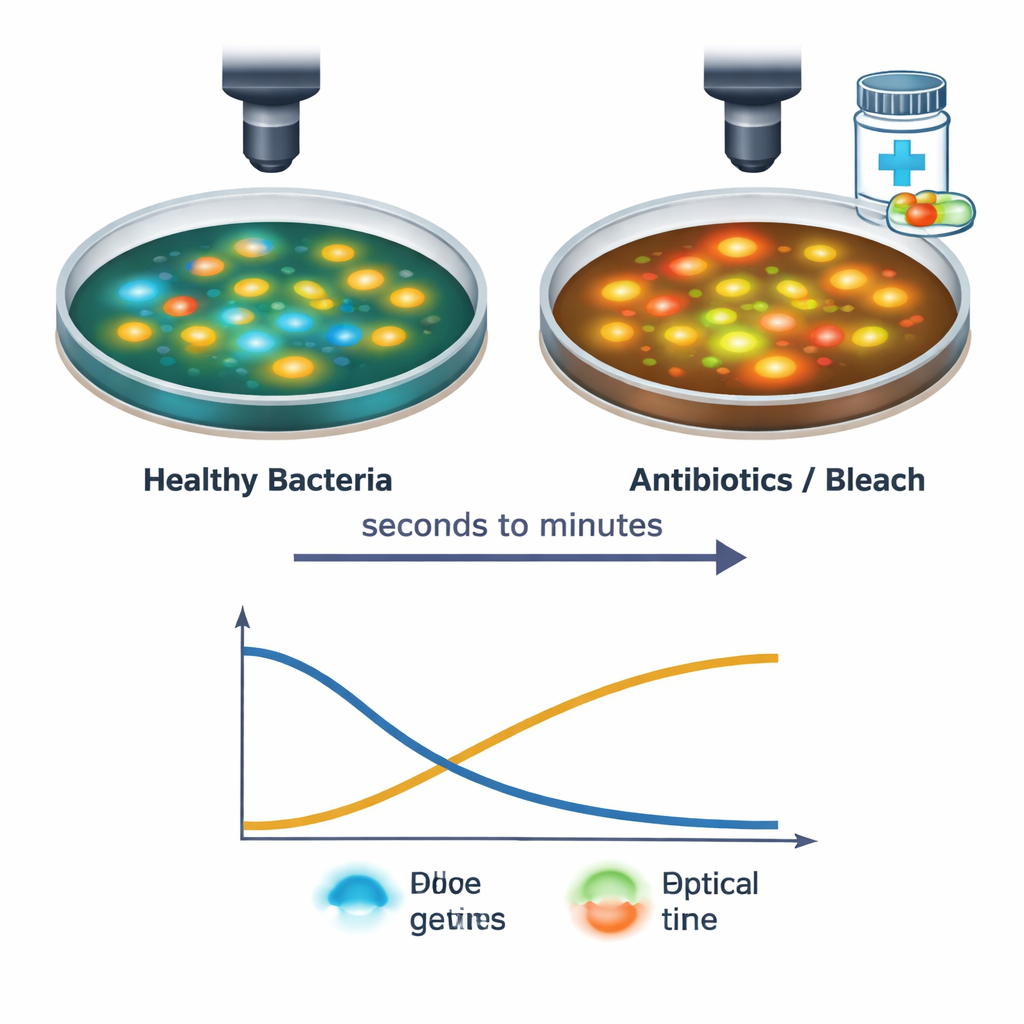
Scrutare il mondo nascosto dei biofilm
I batteri raramente vivono isolati in natura; costruiscono invece comunità viscose e protettive chiamate biofilm su superfici che vanno dagli impianti medici ai denti. In questi strati densi, alcune cellule possono essere molto attive mentre altre restano dormienti, una miscela che aiuta la comunità a sopravvivere agli antibiotici. Utilizzando immagini ampie cucite insieme, i ricercatori hanno mappato il paesaggio metabolico all’interno dei biofilm di S. aureus e lo hanno confrontato con le cellule libere. Hanno trovato tasche luminose e metabolicamente attive circondate da regioni meno attive e hanno mostrato che, in diverse specie, i batteri nei biofilm tendevano ad avere un profilo metabolico più ossidato rispetto ai corrispondenti planctonici. Segnali ottici aggiuntivi suggerivano la presenza di lipidi e proteine extra, coerenti con il materiale adesivo che tiene insieme i biofilm.
Perché questo è importante per la medicina futura
Complessivamente, questi risultati mostrano che l’imaging ottico metabolico senza marcatori può fornire istantanee rapide, dettagliate e non invasive di come i batteri vivono, si adattano e muoiono. Per il lettore non specialistico, il messaggio chiave è che gli scienziati possono ora “ascoltare” l’uso di energia da parte dei batteri in tempo reale, senza disturbare le cellule, usando solo luce calibrata. A lungo termine, questo tipo di tecnologia potrebbe aiutare a identificare batteri difficili da coltivare, individuare sacche di cellule tolleranti ai farmaci all’interno dei biofilm o testare rapidamente come l’infezione di un paziente risponde a diversi antibiotici. Ciò potrebbe favorire trattamenti più rapidi e personalizzati e approfondire la nostra comprensione dei mondi microbici invisibili che influenzano la nostra salute quotidiana.
Citazione: Sorrells, J.E., Yang, L., Iyer, R.R. et al. Real-time, high-resolution metabolic characterization of live bacteria using label-free optical metabolic imaging. npj Biofilms Microbiomes 12, 55 (2026). https://doi.org/10.1038/s41522-026-00920-0
Parole chiave: metabolismo batterico, imaging ottico, biofilm, risposta agli antibiotici, microbioma