Clear Sky Science · it
Modulazione immunitaria guidata dalla microbiota orale lungo l’asse orale–intestino: dai segnali locali all’infiammazione sistemica
Perché la tua bocca conta per tutto il corpo
I batteri che vivono nella bocca fanno molto più che causare carie o alito cattivo. Questo articolo di revisione spiega come i microbi orali possano scendere nell’intestino, disturbare le sue difese delicate e contribuire a scatenare un’infiammazione che raggiunge organi come il fegato e il cervello. Comprendere questo nascosto “asse orale–intestino” offre nuovi indizi su problemi comuni che vanno dalla malattia del fegato grasso all’Alzheimer, e indica passi sorprendentemente semplici — come una migliore igiene orale e scelte alimentari — che possono proteggere la nostra salute complessiva.
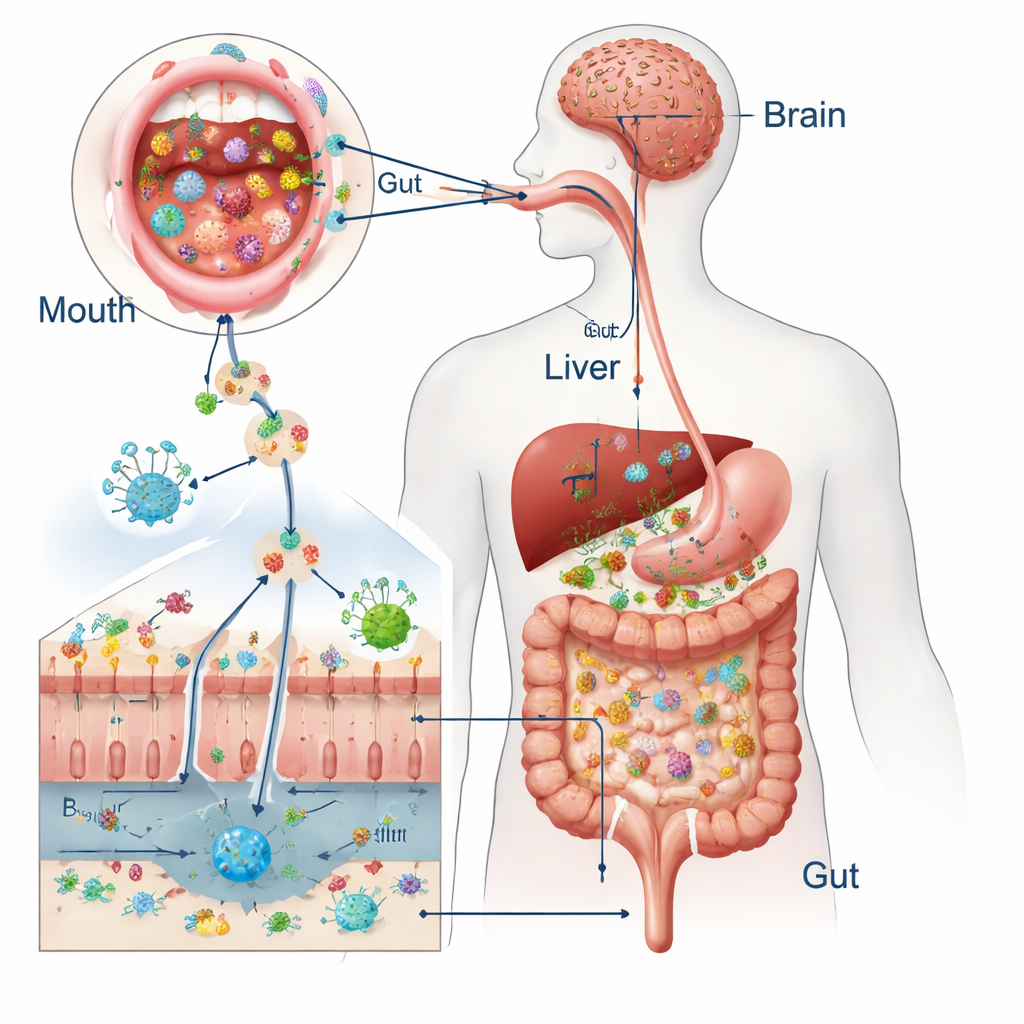
Dalla deglutizione agli effetti sistemici
Ogni giorno inghiottiamo circa un litro e mezzo di saliva piena di miliardi di microrganismi orali. Nelle persone sane, forti difese — gli antimicrobici naturali della saliva, l’acidità gastrica, la bile, il muco viscoso e le giunzioni strette tra le cellule intestinali — impediscono a molti di questi ospiti di stabilirsi. Studi che confrontano i germi della bocca e delle feci mostrano che solo una frazione piccolissima dei microbi intestinali proviene direttamente dalla bocca quando tutto funziona bene. Tuttavia i due ecosistemi si sovrappongono abbastanza da permettere che specie orali come Streptococcus e Veillonella vengano talvolta rilevate nell’intestino, sollevando la domanda su quando esse diventino qualcosa di più di semplici passanti innocui.
Quando le barriere si rompono
Il quadro cambia sotto stress. L’invecchiamento, la bocca secca, una scarsa igiene orale e le malattie gengivali croniche possono sovraccaricare la cavità orale di batteri dannosi. Farmaci come antibiotici e inibitori dell’acidità gastrica indeboliscono le difese intestinali assottigliando il muco, allentando le giunzioni tra le cellule e permettendo a più microrganismi di sopravvivere al passaggio attraverso lo stomaco. Infezioni orali e procedure dentali possono persino spingere i batteri nel flusso sanguigno. La revisione sottolinea anche le vescicole extracellulari batteriche — “pacchetti” nanoscopici rilasciati dai microbi — che possono infiltrarsi nei tessuti e trasportare segnali infiammatori lontano dalla loro fonte. Alcuni batteri orali, come Porphyromonas gingivalis e Fusobacterium nucleatum, si nascondono persino all’interno di cellule immunitarie e viaggiano nel corpo come un “cavallo di Troia” microbico.
Come i batteri orali imparano a vivere nell’intestino
Non tutti i microbi orali che raggiungono l’intestino riescono a restarci. Quelli che lo fanno tendono ad avere astuzie particolari per sopravvivere. Alcuni ceppi rimodellano le loro membrane cellulari per resistere ad acidi forti o alla bile; altri si nutrono degli zuccheri del muco che riveste la parete intestinale o si associano ai batteri residenti dell’intestino per formare biofilm aderenti. Allo stesso tempo imparano a eludere il sistema immunitario. Alcuni bloccano la capacità di uccidere delle cellule natural killer e dei linfociti T; altri interferiscono con i sensori di allarme precoce che normalmente rilevano componenti microbici e scatenano risposte protettive. Spostando l’equilibrio delle cellule immunitarie verso tipi più infiammatori e meno freni regolatori, creano una nicchia in cui la colonizzazione a lungo termine e a basso livello diventa possibile.
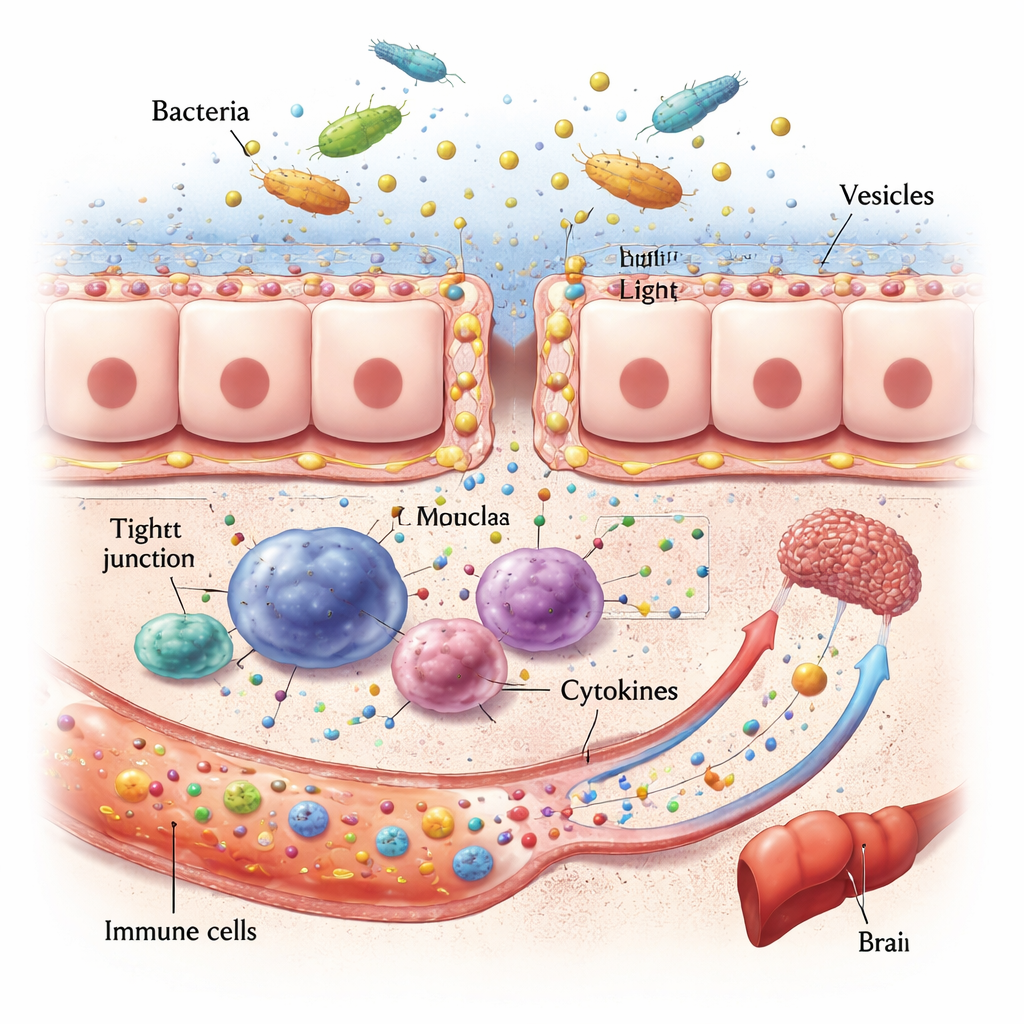
Dal gut leak agli organi malati
Una volta insediati, i microbi orali invasivi e le loro vescicole possono danneggiare la prima linea intestinale. Digeriscono le proteine che sigillano le cellule vicine, assottigliano lo strato di muco e possono persino uccidere direttamente le cellule intestinali. Ciò rende la parete intestinale più permeabile, permettendo a frammenti batterici e tossine di filtrare nel circolo sanguigno. Lì attivano cellule immunitarie e innescano ondate di molecole segnale chiamate citochine. Poiché il sangue proveniente dall’intestino fluisce direttamente al fegato, quest’organo è particolarmente esposto: dati animali e umani collegano patogeni orali a steatosi epatica, fibrosi e peggioramento dell’infiammazione. Percorsi simili collegano la disbiosi orale e la perturbazione intestinale al cervello, dove l’infiammazione cronica e i metaboliti microbici alterati sembrano aggravare l’accumulo di proteine legate all’Alzheimer e disturbare umore e funzioni cognitive.
Nuove modalità di intervento
Riconoscere l’asse orale–intestino apre strategie multilivello per prevenzione e terapia. In bocca, trattamenti parodontali di routine, terapie a base di luce e peptidi antimicrobici naturali possono ridurre i batteri dannosi e diminuire il numero che raggiunge l’intestino. Nell’intestino, probiotici, diete ricche di fibra e integratori che ripristinano gli acidi grassi a catena corta aiutano a ricostruire la barriera intestinale e a calmare un sistema immunitario iperattivo. In prospettiva, sofisticati dispositivi “organ-on-a-chip” che collegano tessuti in miniatura di bocca, intestino, fegato e cervello, insieme a mappe di big data su quali microbi provocano quali reazioni immunitarie, potrebbero consentire approcci personalizzati per prevenire le malattie infiammatorie croniche.
Cosa significa per te
Per il lettore non specialista, il messaggio centrale è che la bocca non è un compartimento isolato: i suoi microbi possono modellare la salute intestinale e, attraverso l’intestino, influenzare l’intero organismo. Quando i batteri orali bypassano o erodono le barriere naturali, possono contribuire a guidare un’infiammazione prolungata in organi lontani come il fegato e il cervello. L’articolo conclude che proteggere la salute orale, preservare la barriera intestinale e orientare con delicatezza le nostre comunità microbiche con trattamenti mirati potrebbe diventare uno strumento importante nella lotta contro le malattie croniche moderne.
Citazione: Li, C., Fan, Y. & Chen, X. Oral microbiota–driven immune modulation along the oral–gut axis: from local signals to systemic inflammation. npj Biofilms Microbiomes 12, 46 (2026). https://doi.org/10.1038/s41522-026-00912-0
Parole chiave: microbioma orale, barriera intestinale, infiammazione sistemica, malattie epatiche, salute cerebrale