Clear Sky Science · it
La terapia antibiotica potenziata con enzimi riduce i biofilm a livelli non rilevabili in un modello di infezione associata a impianto
Perché le infezioni persistenti sugli impianti sono importanti
Le protesi d’anca e di ginocchio cambiano la vita, ma quando i batteri colonizzano questi impianti metallici possono formare comunità viscide chiamate biofilm. Questi biofilm funzionano come città corazzate che proteggono i germi sia dal sistema immunitario sia dagli antibiotici, causando infezioni dolorose e prolungate che sono molto difficili da curare. Questo studio esplora un nuovo trattamento a due punte che prima aiuta a smantellare le difese del biofilm e poi irriga l’area con alte dosi di antibiotici — un approccio che un giorno potrebbe aiutare a salvare più impianti invece di sostituirli.
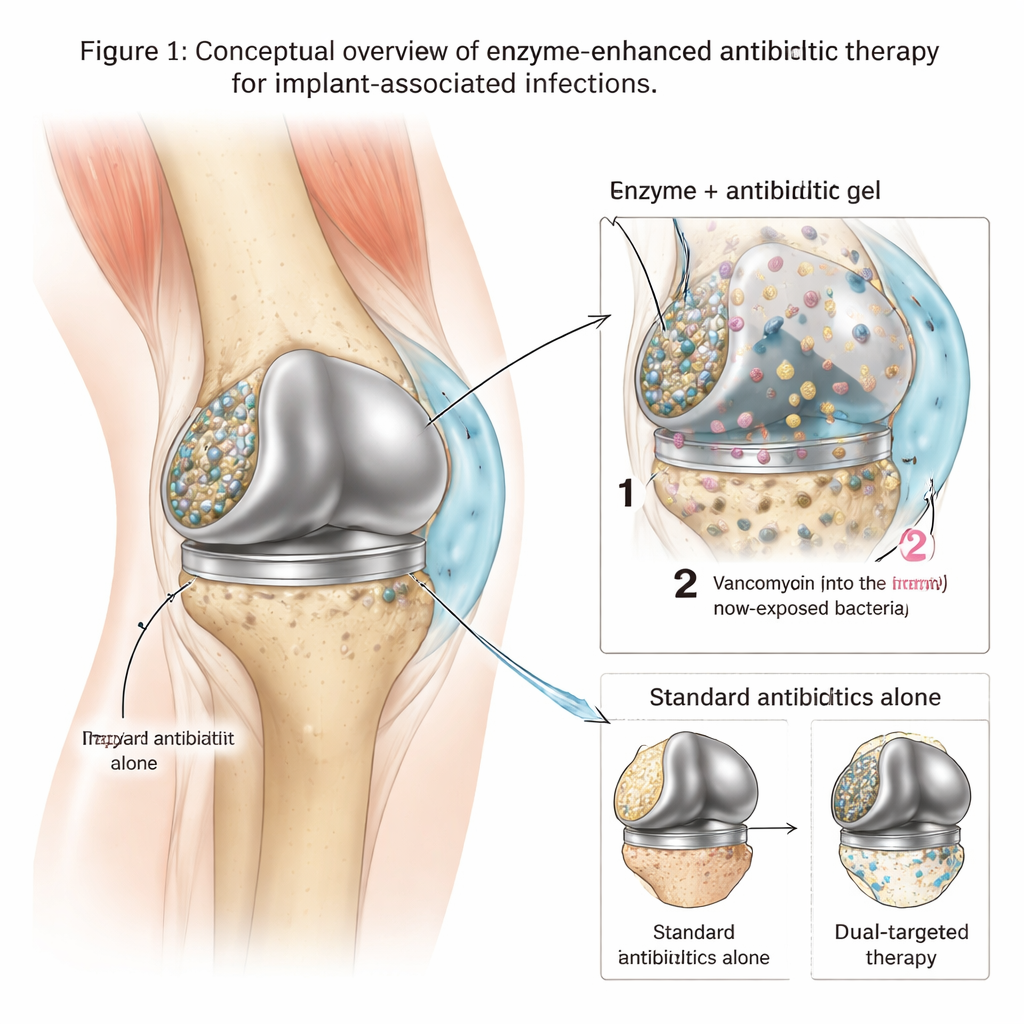
I bastioni nascosti sugli impianti metallici
Quando batteri come lo Staphylococcus aureus resistente alla meticillina (MRSA) si attaccano a un’articolazione artificiale, costruiscono rapidamente una matrice appiccicosa di DNA, zuccheri e altre molecole sulla superficie metallica. All’interno di questo biofilm protetto, i batteri crescono lentamente, modificano il loro comportamento e possono tollerare concentrazioni di antibiotico centinaia o addirittura migliaia di volte superiori a quelle che uccidono i germi liberi in sospensione. Di conseguenza, i trattamenti standard — anche farmaci potenti come la vancomicina — spesso non riescono a eliminare completamente l’infezione, costringendo i pazienti a sottoporsi a interventi ripetuti o alla sostituzione totale dell’impianto. I medici hanno bisogno di strumenti che non solo uccidano i batteri, ma rompano anche la loro fortezza protettiva affinché i farmaci possano raggiungerli.
Un gel intelligente che rilascia enzimi e antibiotici
I ricercatori hanno ideato un trattamento locale basato su un idrogel termosensibile ottenuto da un composto chiamato poloxamero 407. Questo gel è liquido a freddo, il che lo rende facile da iniettare attorno a un impianto, ma si trasforma rapidamente in un solido morbido alla temperatura corporea, aiutandolo a rimanere in sede. Nel gel il team ha caricato due ingredienti chiave: un potente antibiotico (vancomicina) e un cocktail di tre enzimi che degradano componenti principali della matrice del biofilm. Nei test di laboratorio, hanno tarato il gel in modo che gli enzimi vengano rilasciati per primi — allentando e assottigliando il biofilm — mentre la vancomicina viene rilasciata più lentamente nel corso di diversi giorni, mantenendo livelli locali di farmaco molto elevati proprio dove vivono i batteri.
Dalle piastre di laboratorio ai porcellini d’India
Per verificare se la strategia funzionasse davvero, il team l’ha testata prima sui biofilm cresciuti su frammenti di titanio in laboratorio e poi in un modello su porcellino d’India che imita impianti infetti. In vitro, due applicazioni del gel enzimatico‑antibiotico, a 48 ore di distanza, hanno ridotto il numero di batteri vivi sulle superfici metalliche di oltre 100.000 volte e hanno quasi azzerato la massa del biofilm. Negli animali, i ricercatori hanno collocato chirurgicamente gabbie perforate contenenti perline di titanio sotto la pelle, le hanno infettate con MRSA e poi le hanno trattate con diverse combinazioni di antibiotici sistemici e gel locali. Il regime più efficace ha combinato: (1) il gel locale contenente sia enzimi sia vancomicina, somministrato due volte, e (2) un trattamento sistemico con vancomicina più un secondo antibiotico, la rifampicina, che penetra particolarmente bene nei biofilm.
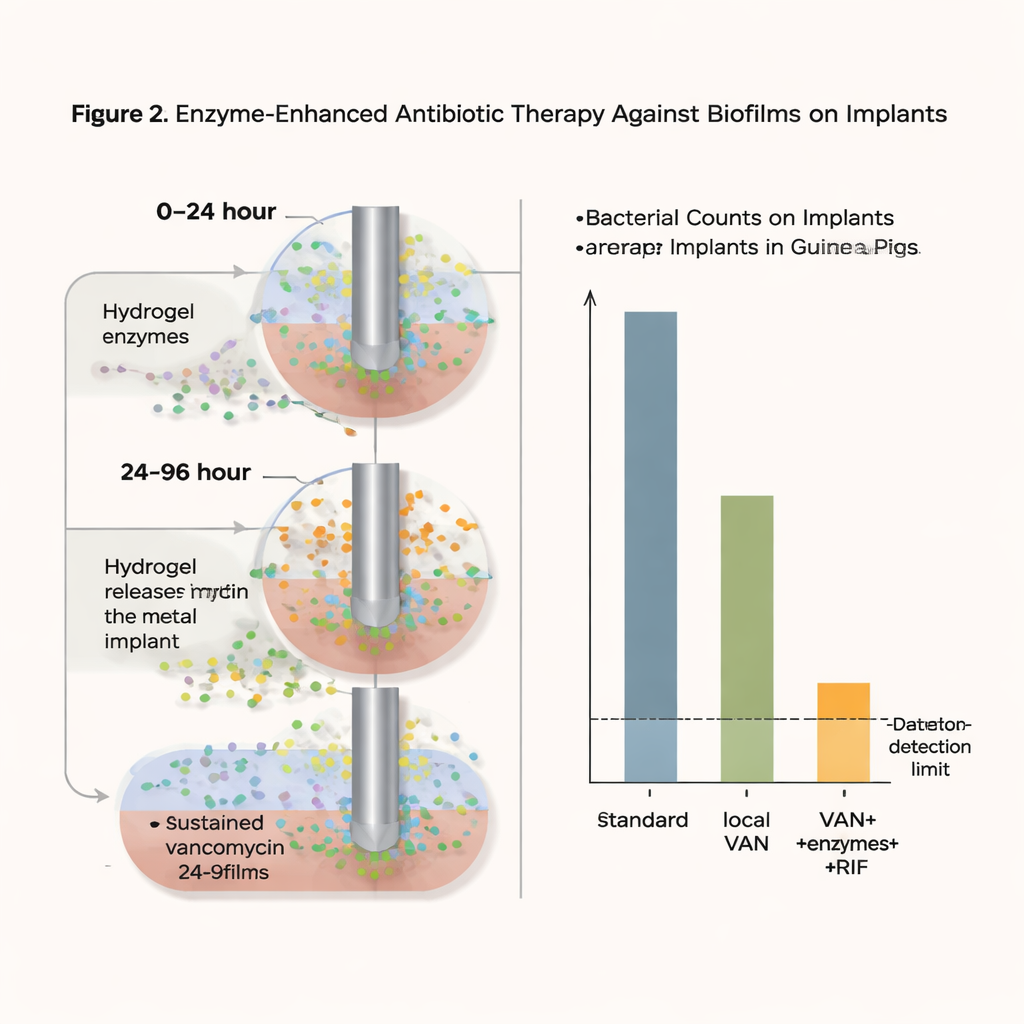
Quello che il nuovo approccio ha ottenuto
Con questa strategia intensiva ma localizzata, i conteggi batterici sul materiale dell’impianto sono scesi fino al limite di rilevamento — effettivamente «nessun batterio recuperabile» in questo modello — nel 75% delle gabbie trattate un giorno dopo la fine della terapia, e nel 37,5% anche cinque giorni dopo. Importante, non è stato osservato alcun aumento della resistenza alla vancomicina, e gli alti livelli locali di vancomicina sembravano prevenire l’emergere di ceppi resistenti alla rifampicina. I test di sicurezza su cellule in coltura e su un modello di pelle umana ricostruita non hanno mostrato segni di tossicità o irritazione dalle formulazioni in gel. Sebbene in alcuni casi si sia verificata una lieve ricrescita batterica e il periodo di trattamento sia stato più breve rispetto a quello che i pazienti ricevono tipicamente, i risultati dimostrano che combinare enzimi che distruggono i biofilm con una somministrazione locale sostenuta di antibiotici può ridurre drasticamente infezioni altrimenti ostinate.
Cosa potrebbe significare per i pazienti
Per le persone alle prese con infezioni legate a impianti, questo lavoro indica un futuro in cui i chirurghi potrebbero iniettare un gel intelligente attorno a un’articolazione infetta, invece di rimuovere o sostituire immediatamente l’hardware. Indebolendo prima lo scudo del biofilm e poi inondando l’area con dosi alte e sostenute di antibiotici — supportate da un trattamento sistemico — questa strategia a doppio bersaglio punta a ridurre i numeri batterici fino a livelli non rilevabili e a diminuire il rischio di resistenza. Sebbene siano necessari ulteriori studi, trattamenti più lunghi e trial clinici sull’uomo, l’approccio offre un progetto promettente per trasformare alcune delle infezioni ortopediche più persistenti in problemi più gestibili e potenzialmente curabili.
Citazione: Buzisa Mbuku, R., Poilvache, H., Maigret, L. et al. Enzymes-enhanced antibiotic therapy reduces biofilms to undetectable levels in an implant-associated infection model. npj Biofilms Microbiomes 12, 44 (2026). https://doi.org/10.1038/s41522-026-00910-2
Parole chiave: infezione da biofilm, impianti ortopedici, vancomicina, terapia enzimatica, rifampicina