Clear Sky Science · it
Esplorazione teorica dei protocolli per il trattamento delle infezioni delle protesi articolari con combinazioni di antibiotici e batteriofagi
Perché le infezioni degli impianti articolari sono importanti
Le sostituzioni di anca e ginocchio hanno trasformato la vita di milioni di persone, permettendo di camminare senza dolore. Ma quando i batteri colonizzano queste articolazioni artificiali, possono formare comunità viscose chiamate biofilm che si attaccano saldamente a superfici metalliche e plastiche. Una volta che un biofilm è stabilito, dosi normali di antibiotici e le difese immunitarie dell’organismo spesso faticano a eliminarlo, costringendo talvolta i pazienti a sottoporsi a ulteriori interventi chirurgici. Questo studio si chiede se l’aggiunta di virus che attaccano specificamente i batteri—detti batteriofagi, o fagi—agli antibiotici standard possa offrire un modo migliore per trattare queste infezioni ostinate.
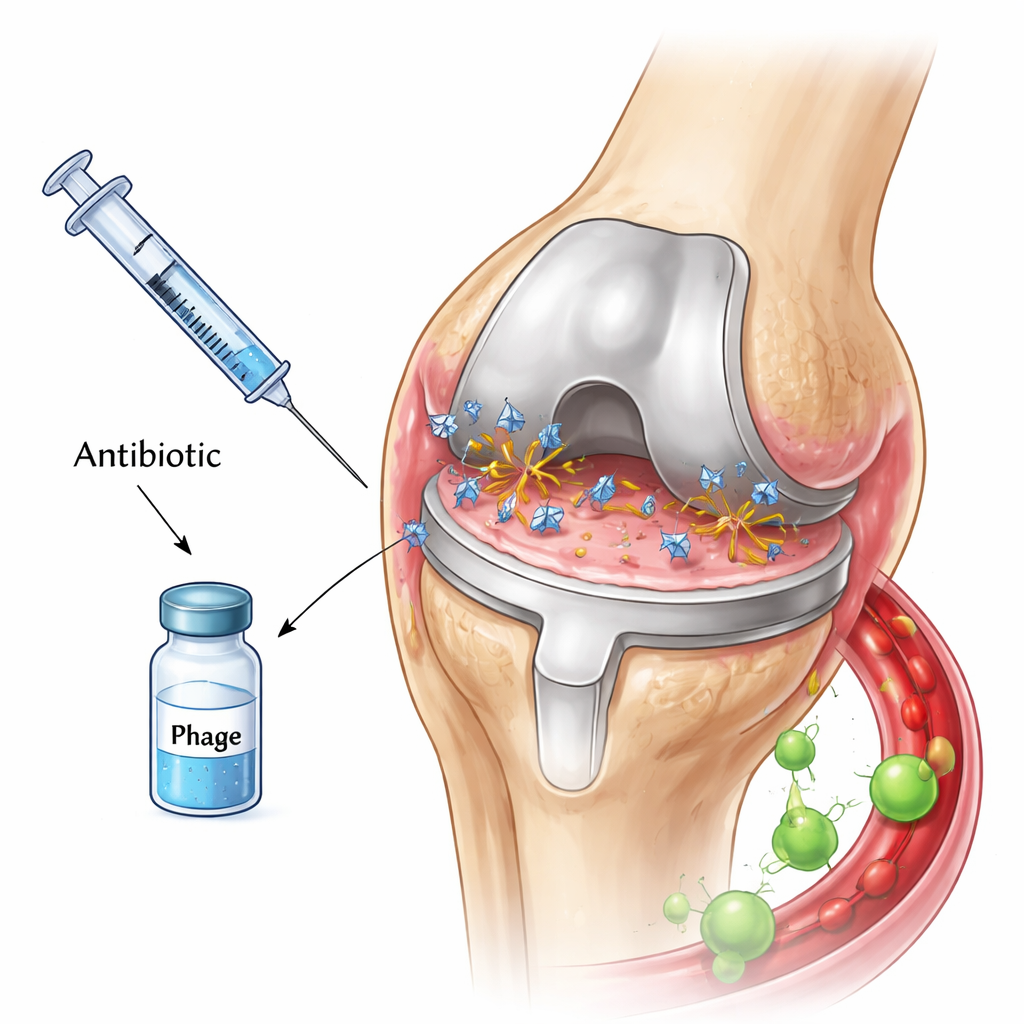
Virus minuscoli che cacciano i batteri
I fagi sono predatori naturali dei batteri. Si attaccano a una cellula batterica, iniettano il loro materiale genetico, trasformano la cellula in una fabbrica di virus e infine la fanno esplodere, liberando uno sciame di nuovi fagi. Alcuni fagi portano anche enzimi in grado di degradare il materiale viscoso che circonda i biofilm, aprendo potenzialmente strati protettivi che proteggono i batteri dai farmaci. Grazie a queste caratteristiche, molti ricercatori sperano che la combinazione di fagi e antibiotici possa offrire un potente doppio colpo contro le infezioni delle protesi articolari, soprattutto quando i batteri diventano resistenti ai farmaci.
Costruire le infezioni dentro un computer
Invece di passare subito a esperimenti su animali o a studi clinici, gli autori hanno prima costruito un modello matematico e computazionale dettagliato di un’infezione da protesi articolare. Il loro sistema virtuale aveva due zone principali: batteri liberi nei fluidi corporei e batteri incorporati in un biofilm sulla superficie dell’impianto. Il modello teneva anche traccia delle cellule immunitarie, dei nutrienti per la crescita batterica, degli antibiotici e dei fagi, tutti in movimento dentro e fuori dall’articolazione. Variando condizioni come la dose del farmaco, i tempi e la presenza di batteri resistenti agli antibiotici, potevano esplorare molte strategie terapeutiche difficili, lente o costose da testare in pazienti reali.
Quando i medicinali funzionano da soli e insieme
Le simulazioni hanno mostrato che né il sistema immunitario né gli antibiotici da soli riescono facilmente a eliminare le infezioni associate ai biofilm. Gli antibiotici riducevano fortemente i batteri liberi, ma a malapena intaccavano la popolazione nei biofilm. I fagi potevano inizialmente controllare l’infezione in modo più efficace, ma introducevano cicli di boom e crollo: quando i fagi uccidevano i batteri, le prede diventavano troppo scarse, provocando un calo dei fagi e permettendo ai batteri di riprendersi. Quando antibiotici e fagi venivano somministrati contemporaneamente, l’antibiotico tendeva a dominare l’esito, e l’aggiunta del fago spesso faceva poco più di quanto l’antibiotico potesse ottenere da solo.
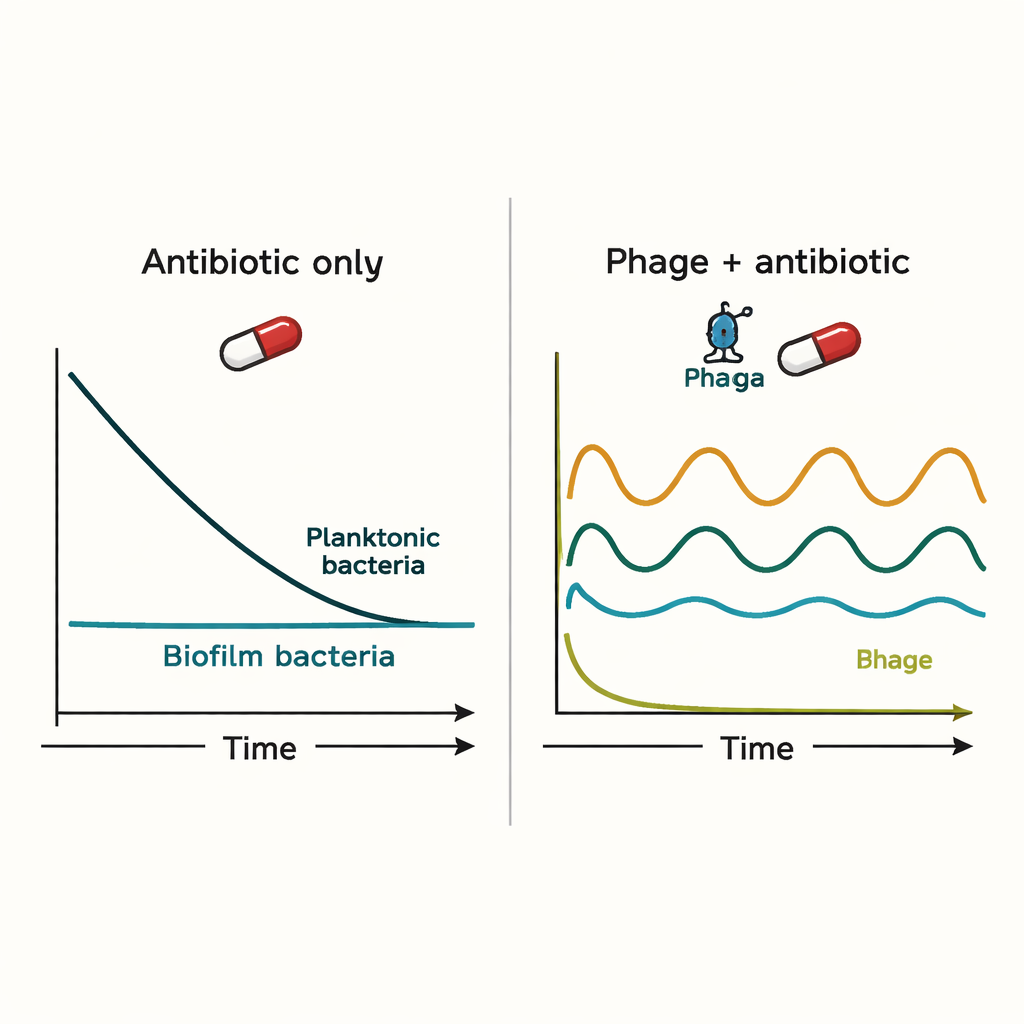
Il ruolo speciale dei tempi e della resistenza
Il modello diventava più promettente quando si includevano batteri resistenti agli antibiotici. I fagi riuscivano ad attaccare queste cellule resistenti, talvolta eliminandole completamente. Se il trattamento con fagi veniva iniziato per primo e gli antibiotici erano aggiunti poche ore dopo, la strategia combinata riduceva i batteri liberi di molti ordini di grandezza ed eliminava le sottopopolazioni resistenti nelle simulazioni. Anche così, i batteri associati al biofilm non venivano completamente debellati; piuttosto, il loro numero veniva mantenuto a livelli inferiori che potrebbero essere più facili da gestire per il sistema immunitario. Questo suggerisce che i fagi potrebbero essere più utili non come proiettili magici, ma come assistenti che prevengono la resistenza e mantengono le infezioni sotto controllo.
Cosa significa per pazienti e medici
Per le persone con un impianto articolare infetto, questo lavoro offre allo stesso tempo cautela e speranza. Il modello suggerisce che aggiungere semplicemente i fagi agli antibiotici standard difficilmente guarirà da solo le infezioni profonde da biofilm. Tuttavia, i fagi potrebbero comunque essere strumenti preziosi: possono aiutare a eliminare i batteri resistenti agli antibiotici e ridurre il numero totale di germi a livelli che il corpo può affrontare, specialmente se usati prima o con un timing attento rispetto agli antibiotici. Gli autori sottolineano che queste sono predizioni teoriche, non prove cliniche. Il loro messaggio principale è che sono necessari esperimenti pensati con cura—guidati da modelli come questo—per scoprire quando la terapia con fagi può davvero migliorare gli esiti per i pazienti con infezioni di protesi articolari.
Citazione: Levin, B.R., Gil-Gil, T., Berryhill, B.A. et al. A theoretical exploration of protocols for treating prosthetic joint infections with combinations of antibiotics and bacteriophage. npj Biofilms Microbiomes 12, 51 (2026). https://doi.org/10.1038/s41522-025-00908-2
Parole chiave: infezione di protesi articolare, biofilm, terapia con batteriofagi, resistenza agli antibiotici, modellizzazione matematica