Clear Sky Science · it
Fasi della formazione di condensati biomolecolari nell’assemblaggio del pro-β-carboxysoma
Perché contano le piccole fabbriche del carbonio
Le catene alimentari della Terra dipendono dalla fotosintesi, eppure l’enzima chiave che estrae anidride carbonica (CO2) dall’aria, la Rubisco, è lento e facilmente confondibile dall’ossigeno. I cianobatteri — microbi fotosintetici microscopici — hanno risolto questo problema tempo fa costruendo “micro‑fabbriche” proteiche chiamate carboxysomi che intrappolano CO2 attorno alla Rubisco. Questo studio svela come un complesso adattatore cruciale, composto dalle proteine ApN e CM, si auto‑assembli in fasi per contribuire a costruire un carboxysoma funzionante. Capire questa coreografia potrebbe guidare gli sforzi per installare sistemi simili di potenziamento del CO2 nelle piante coltivate e aumentare le rese.
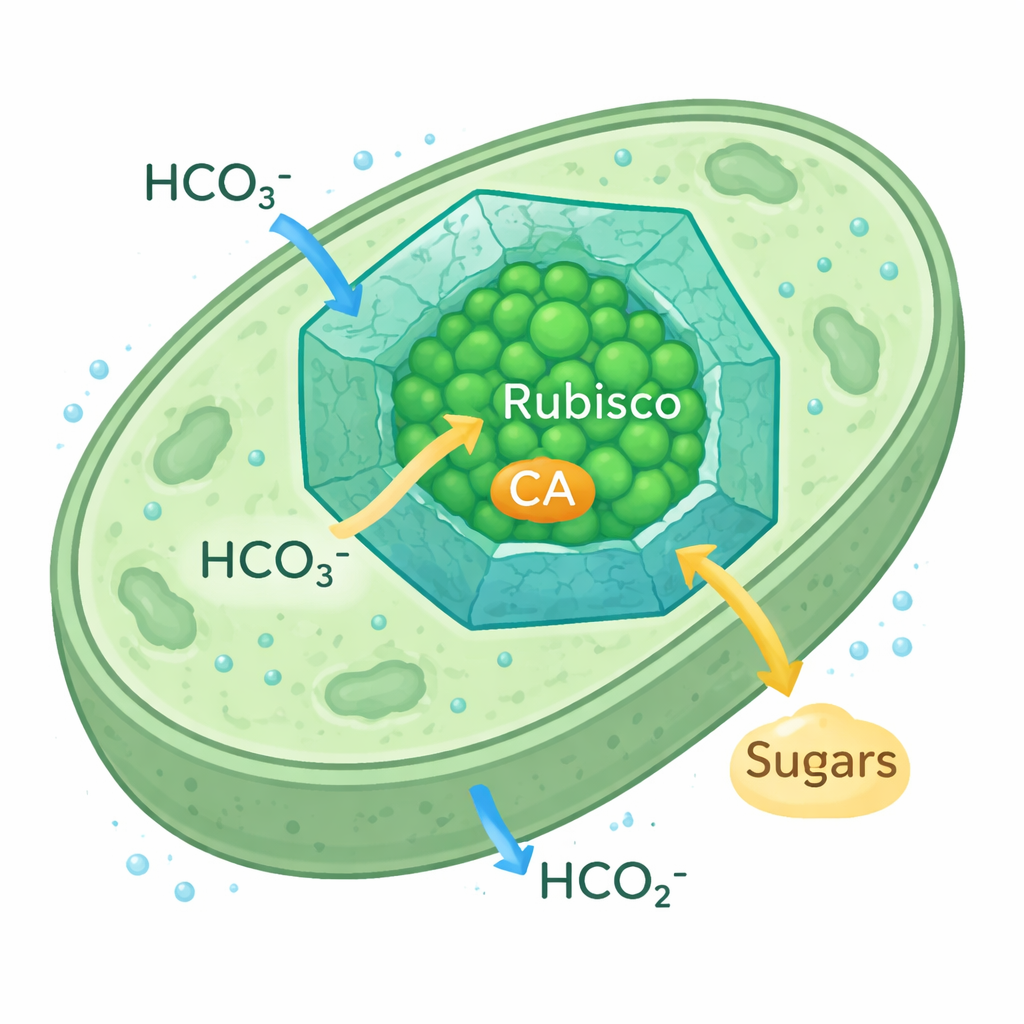
Come i microbi potenziano la cattura del carbonio
I carboxysomi dei cianobatteri sono piccoli compartimenti proteici icosaedrici che si trovano all’interno della cellula. Il loro involucro proteico lascia entrare gli ioni bicarbonato rallentando al contempo la fuga del CO2, creando una bolla ricca di CO2 attorno alla Rubisco e al suo enzima partner, l’anidrasi carbonica (CA), che converte il bicarbonato in CO2. Questo meccanismo di concentrazione del CO2 permette ai cianobatteri di prosperare anche quando la CO2 ambientale è scarsa. Poiché la forma di Rubisco usata in questi carboxysomi somiglia a quella delle piante, i ricercatori li considerano un modello realistico per reingegnerizzare i cloroplasti delle piante al fine di catturare il carbonio più efficacemente.
Il pezzo del puzzle che si collega all’involucro
Prima della formazione dell’involucro proteico rigido, i cianobatteri costruiscono prima un condensato morbido simile a una goccia, il “pro‑carboxysoma”. Studi precedenti avevano mostrato che una proteina impalcatura chiamata CM porta insieme Rubisco e CA in questa goccia. Il collegamento mancante era come la proteina adattatrice dell’involucro, ApN, si unisse a questa struttura e in seguito la connettesse alle proteine dell’involucro. Gli autori hanno scoperto che quando ApN è espressa da sola forma un fascio a quattro parti che ignora gli altri componenti del carboxysoma. In questo stato ApN non viene incorporata nelle gocce con Rubisco, CM e CA, suggerendo che durante il vero assemblaggio del carboxysoma sia impiegata una forma diversa di ApN.
Adattatori co‑costruiti e un interruttore redox
Osservando l’organizzazione genica nei cianobatteri, il gruppo ha notato che apn si trova immediatamente dopo cm nello stesso operone, perciò le due proteine sono solitamente sintetizzate insieme. Riproducendo questa situazione in batteri, hanno co‑espresso ApN e CM da un unico frammento di DNA. In queste condizioni ApN non formò più un tetramero indipendente. Invece, tre subunità di ApN e una subunità di CM si assemblarono in un complesso adattatore specifico a quattro parti, indicato come (ApN)3:CM. Questo eterocomplesso si legava facilmente a Rubisco, CA e CM e poteva unirsi ai condensati. Modellistica strutturale e crio‑microscopia elettronica mostrarono che ApN e CM si incontrano tramite un’interfaccia finemente sintonizzata a “lingua e scanalatura”; quando residui chiave di ApN in questa interfaccia furono mutati, l’adattatore non si formava e le cellule non riuscivano a costruire carboxysomi corretti.
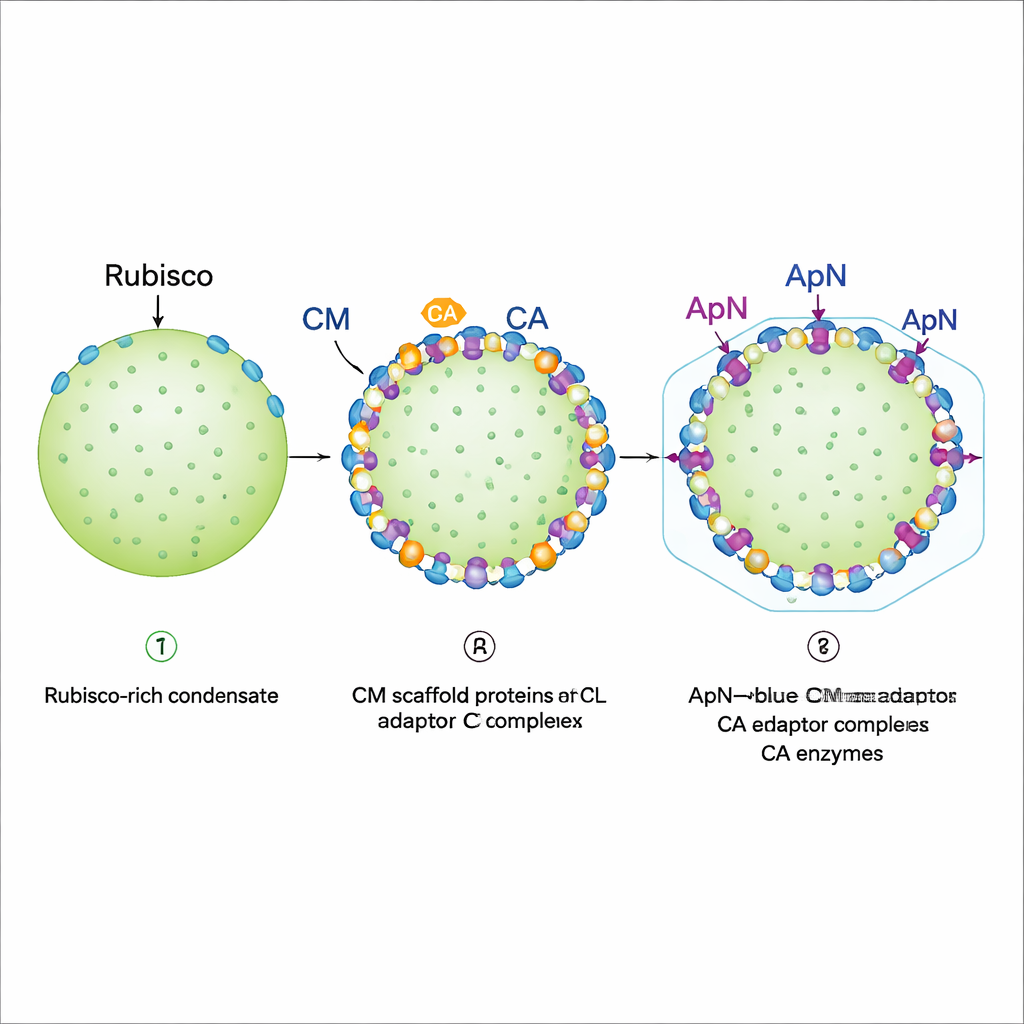
Posizionamento al margine e preparazione per l’involucro
L’imaging a fluorescenza di gocce ricostituite ha rivelato un programma di assemblaggio passo dopo passo. Prima, Rubisco, CM a lunghezza intera e una variante più corta di CM formano un condensato denso che si comporta come un gel: Rubisco è essenzialmente bloccata in posizione. Successivamente vengono aggiunte CA e il complesso (ApN)3:CM. Entrambi tendono a stabilirsi al bordo esterno della goccia esistente, a condizione che la CA arrivi prima o insieme a (ApN)3:CM. Questa localizzazione al margine è cruciale perché la coda di ApN porta un “peptide di incapsulamento” che si lega alle proteine dell’involucro. Gli autori hanno inoltre scoperto un interruttore redox incorporato: man mano che l’interno del carboxysoma in maturazione diventa più ossidante, due residui di cisteina conservati in ApN possono ossidarsi, spostando l’adattatore da un tetramero (ApN)3:CM verso un trimero (ApN)2:CM. Nelle cellule cianobatteriche viventi, alterare queste cisteine rallentava la crescita e produceva carboxysomi sovradimensionati ma ancora funzionali, sottolineandone il ruolo nel perfezionare la maturazione.
Lezioni per costruire colture migliori
Per un non specialista questi dettagli molecolari possono suonare arcani, ma si riducono a un messaggio semplice: tempismo e collaborazione sono importanti. Il lavoro mostra che ApN deve essere co‑prodotta con CM per evitare di formare un auto‑aggregato inutile e diventare invece un adattatore che si posiziona sulla superficie del pro‑carboxysoma, pronto a reclutare l’involucro. Un passaggio sensibile al redox aiuta poi a rimodellare questo adattatore mentre il compartimento si chiude e la chimica interna cambia. Per gli ingegneri delle piante che sperano di trapiantare nei raccolti il macchinario cianobatterico di concentrazione del CO2, lo studio evidenzia che non basta trasferire singole parti; bisogna anche rispettare l’ordine, i rapporti e gli interruttori chimici che guidano l’assemblaggio del carboxysoma in natura.
Citazione: Zang, K., Hong, X., Nguyen, N.D. et al. Stages of biomolecular condensate formation in pro-β-carboxysome assembly. Nat. Plants 12, 447–464 (2026). https://doi.org/10.1038/s41477-026-02227-6
Parole chiave: assemblaggio del carboxysoma, meccanismo di concentrazione del CO2 nei cianobatteri, condensati di Rubisco, condensati biomolecolari, fotosintesi sintetica