Clear Sky Science · it
Profilazione molecolare multilivello informa la diagnosi e la terapia mirata del tumore desmoplastico a piccole cellule
Un tumore raro che richiede risposte migliori
Il tumore desmoplastico a piccole cellule (DSRCT) è un cancro estremamente raro e aggressivo che colpisce principalmente bambini, adolescenti e giovani adulti. Poiché è così infrequente e può imitare altri tumori al microscopio, i medici spesso faticano a diagnosticarlo correttamente e a scegliere terapie efficaci. Questo studio pone una domanda semplice ma potente: se analizziamo a fondo i tumori DSRCT su molti livelli molecolari — non solo il DNA, ma anche l’RNA, i profili proteici e i marchi chimici sul DNA — possiamo sia affinare la diagnosi sia scoprire nuove opzioni terapeutiche più precise per pazienti che hanno esaurito le terapie standard?
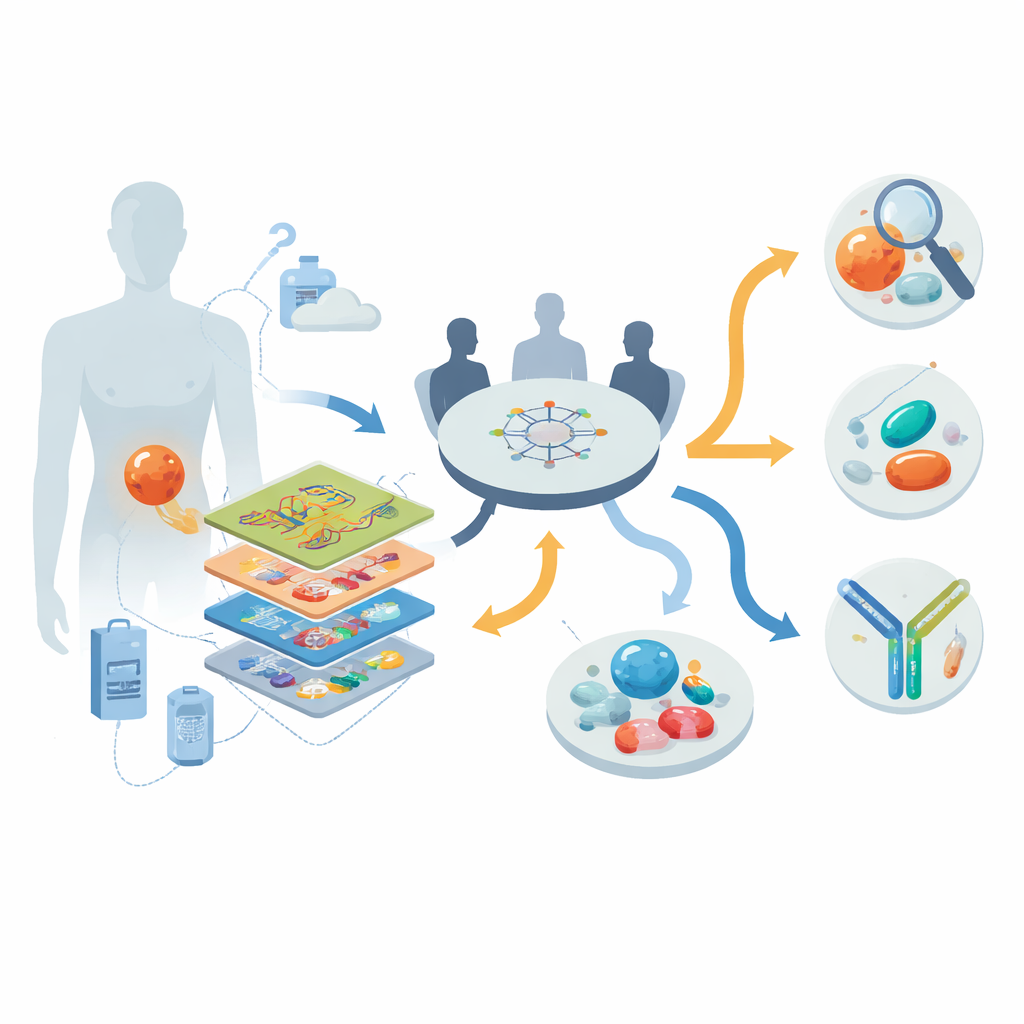
Esaminare i tumori strato dopo strato
I ricercatori hanno operato all’interno di un programma nazionale di oncologia di precisione in Germania, arruolando 30 persone con DSRCT avanzato, per lo più resistente ai trattamenti, tra il 2013 e il 2022. Per ciascun paziente hanno applicato un kit multi-omico: sequenziamento dell’intero genoma o dell’esoma per studiare il DNA; sequenziamento dell’RNA per osservare quali geni sono attivamente espressi; profilazione della metilazione del DNA per catturare impronte epigenetiche; e, in nove pazienti, misurazioni dettagliate di proteine e fosfoproteine che rivelano quali vie di segnalazione sono effettivamente attive. Un tumor board multidisciplinare ha quindi riesaminato questi dati insieme alla storia clinica di ciascun paziente per generare raccomandazioni individualizzate per chiarire la diagnosi, proporre farmaci mirati e valutare trial clinici.
Correggere diagnosi errate e rivelare bersagli nascosti
Un risultato sorprendente è stato quanto spesso la profilazione approfondita abbia corretto la diagnosi iniziale. In otto dei 30 pazienti, tumori inizialmente classificati come altre entità — come tumori di origine sconosciuta o sarcomi vagamente definibili — sono stati riclassificati come DSRCT una volta identificata una fusione genica caratteristica (EWSR1::WT1) e un pattern di metilazione tipico. Allo stesso tempo, il DNA di questi tumori si è rivelato relativamente tranquillo: c’erano poche mutazioni e solo cambiamenti occasionali nel numero di copie, quindi gli approcci classici «gene mutato = bersaglio farmacologico» hanno dato poco. I suggerimenti più ricchi sono invece emersi dai livelli di RNA e proteici. Confrontando l’attività genica nel DSRCT con centinaia di altri sarcomi, il team ha rilevato una ripetuta sovraespressione di diverse molecole di superficie ed enzimi di segnalazione che, in linea di principio, potrebbero essere attaccati con farmaci esistenti o emergenti.
Dai segnali molecolari a terapie su misura
Sulla base di questi pattern, il tumor board ha emesso 107 suggerimenti gestionali informati molecolarmente per 28 dei 30 pazienti. La maggior parte delle raccomandazioni riguardava farmaci che bloccano le tirosin-chinasi — enzimi chiave che guidano la crescita cellulare e la formazione dei vasi — o strategie più nuove che si legano a proteine di superficie altamente espresse. Tra gli esempi, inibitori di chinasi a piccola molecola come pazopanib; radioterapia peptidica mirata ai recettori della somatostatina; CAR-T sperimentali dirette contro la molecola di adesione CLDN6; e coniugati anticorpo–farmaco che veicolano tossine alle cellule che esprimono il recettore ERBB2 (HER2). Diciassette pazienti sono stati considerati idonei per trial clinici con biomarcatori abbinati, sottolineando come dati molecolari dettagliati possano aprire porte a studi altrimenti difficili da raggiungere per persone con una malattia ultra-rara.
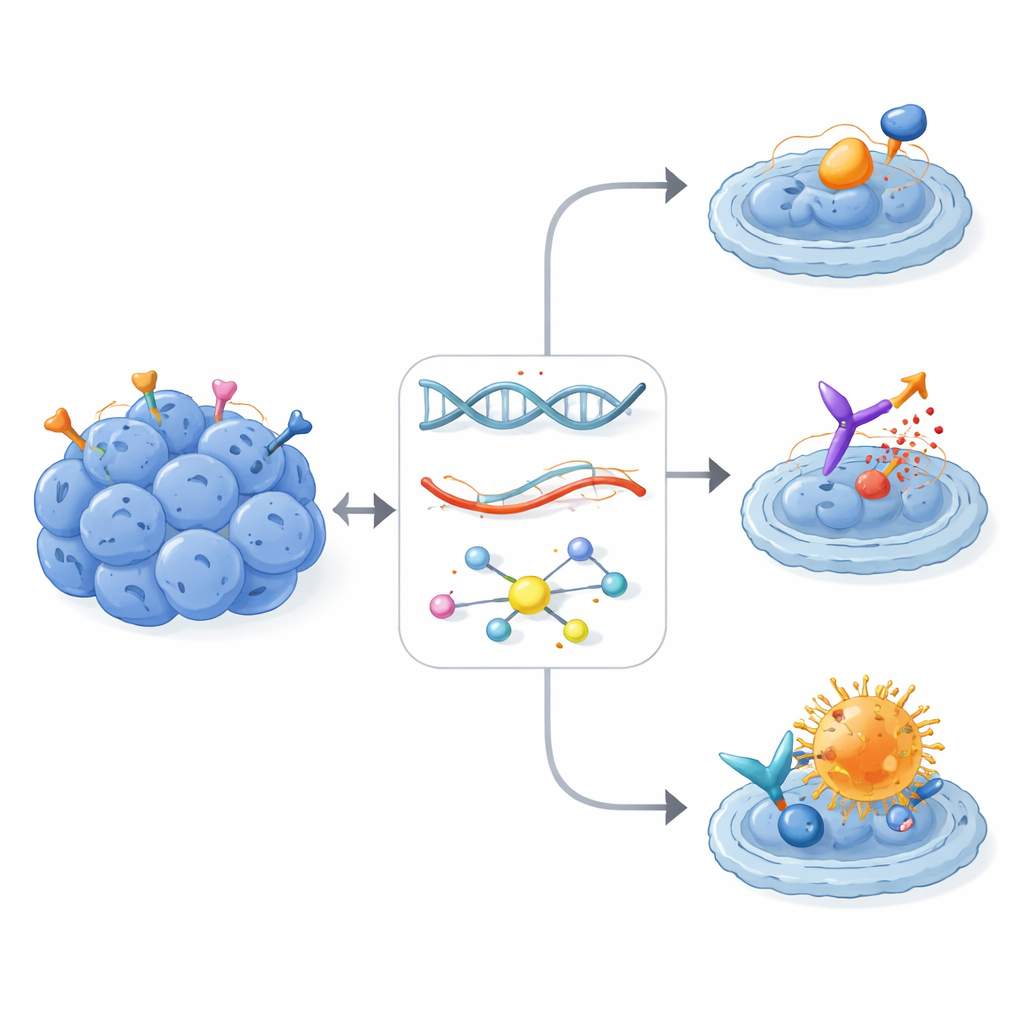
Impatto nel mondo reale in pazienti pesantemente pretrattati
Di tutte le terapie personalizzate raccomandate, 16 sono state effettivamente somministrate a 13 pazienti, tutte guidate da segnali a livello di RNA e talvolta raffinate dai dati sulle fosfoproteine. Sebbene questi individui avessero già affrontato molteplici cicli di chemioterapia e trattamenti locali, otto dei 13 hanno raggiunto il controllo della malattia — cinque con riduzione parziale del tumore e tre con malattia stabile. Gli inibitori multi-target delle tirosin-chinasi, più spesso il pazopanib, hanno prodotto benefici rilevanti e talvolta duraturi in diversi pazienti, specialmente quando i bersagli noti del farmaco erano chiaramente iperattivi nel tumore. Forse più notevoli sono stati due pazienti con alta espressione di ERBB2 che hanno ricevuto il coniugato anticorpo–farmaco trastuzumab deruxtecan (T-DXd). Entrambi hanno avuto risposte prolungate durate fino a due anni o più, nonostante avessero esaurito molte linee terapeutiche precedenti e nonostante il recettore ERBB2 non mostrasse il pattern di attivazione forte tipicamente richiesto per i farmaci classici anti-ERBB2.
Cosa significa per i pazienti e per le cure future
Per le persone con DSRCT, lo studio offre un messaggio di cauto ottimismo. Sebbene questo cancro presenti poche mutazioni evidenti del DNA da sfruttare, l’osservazione attraverso molteplici livelli molecolari può sia correggere diagnosi errate sia rivelare debolezze sfruttabili che sono invisibili ai test standard. Il lavoro dimostra che, anche in una malattia rara e aggressiva, un approccio guidato dalla biologia può produrre benefici clinici reali, incluse risposte durature a farmaci come pazopanib e trastuzumab deruxtecan. Più in generale, sostiene che i pazienti con DSRCT — e per estensione altri tumori ultra-rari — possono trarre vantaggio dall’accesso routinario a una profilazione molecolare completa e a una revisione esperta, aprendo la strada a futuri trial in cui i trattamenti sono scelti non solo in base al tipo di tumore, ma alle impronte molecolari uniche del cancro di ciascuna persona.
Citazione: Renner, M., Oleś, M., Paramasivam, N. et al. Multi-layered molecular profiling informs the diagnosis and targeted therapy of desmoplastic small round cell tumor. Nat Commun 17, 3397 (2026). https://doi.org/10.1038/s41467-026-71636-0
Parole chiave: tumore desmoplastico a piccole cellule, oncologia di precisione, profilazione multi-omica, terapia mirata, coniugati anticorpo-farmaco