Clear Sky Science · it
Interazione tra O-acetilazione dei sialici nel Golgi dipendente e indipendente da SLC33A1 nella catalisi di CASD1
Come piccole modifiche zuccherine possono influenzare salute e malattia
Le nostre cellule sono rivestite da catene zuccherine complesse che funzionano come carte d’identità molecolari, guidando l’immunità, lo sviluppo e persino il modo in cui i virus si agganciano. Questo studio esplora una modifica sottile ma potente di quegli zuccheri — l’aggiunta di piccoli “cappucci” chimici chiamati gruppi acetile a uno zucchero terminale chiamato acido sialico — e rivela una sorprendente macchina molecolare a due componenti che controlla questo processo all’interno dell’apparato del Golgi. Capire questo sistema nascosto aiuta a spiegare alcuni gravi disturbi neurologici e offre indizi su come le cellule regolano finemente la loro superficie in salute e malattia. 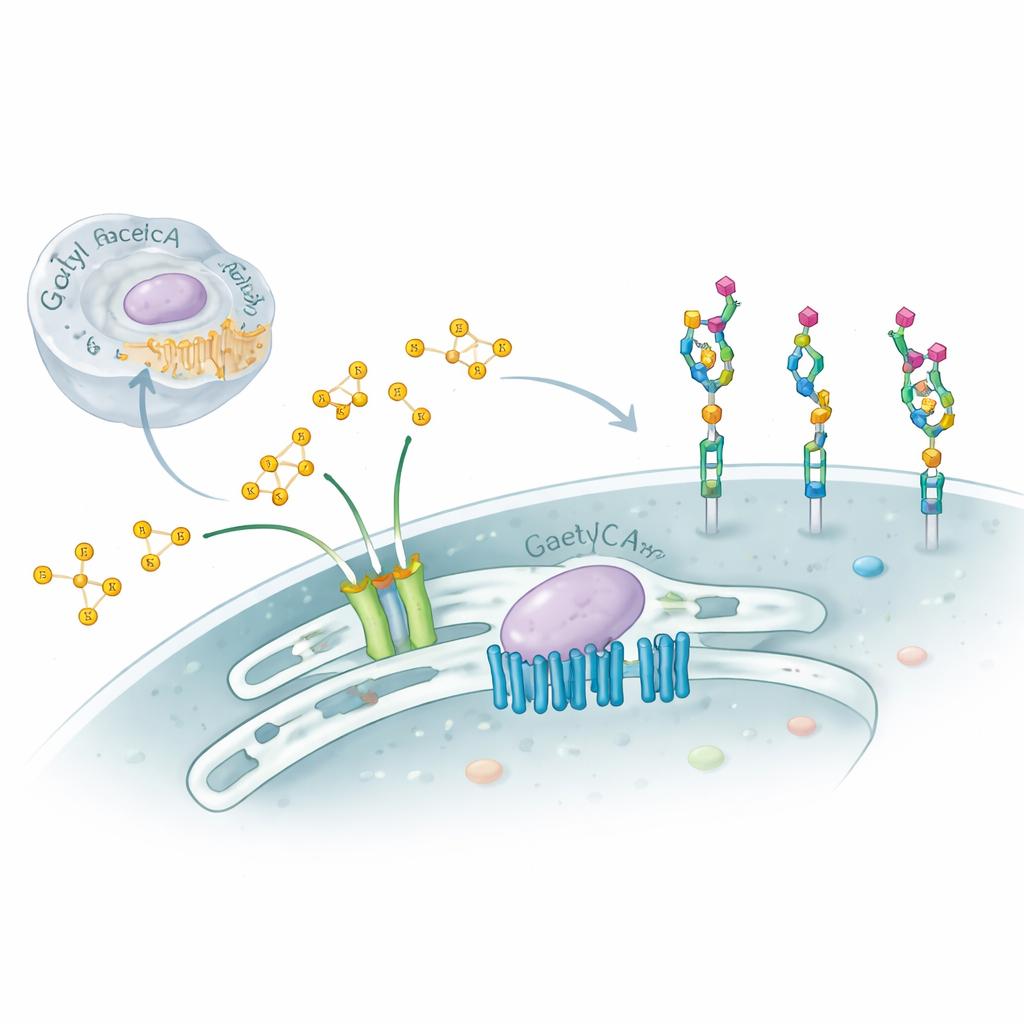
Gli zuccheri speciali in superficie cellulare
Gli acidi sialici si trovano alle estremità esterne di molti zuccheri di superficie su proteine e lipidi, in particolare su molecole chiamate gangliosidi nel cervello. Modificando lievemente gli acidi sialici — per esempio aggiungendo uno o due gruppi acetile in posizioni specifiche — le cellule possono mascherare siti di riconoscimento esistenti o crearne di nuovi. Virus come l’influenza C e alcuni coronavirus cercano specificamente questi zuccheri modificati, e i gangliosidi acetilati possono influenzare la sopravvivenza dei neuroni così come la crescita dei tumori. Eppure, nonostante la loro importanza, il funzionamento interno della macchina cellulare che inserisce questi gruppi acetile nel Golgi è rimasto poco compreso.
Un trasportatore e un enzima che lavorano mano nella mano
I ricercatori si sono concentrati su due proteine che risiedono nel Golgi o nei suoi dintorni: SLC33A1, un trasportatore che sposta acetil‑CoA (il principale donatore di acetile della cellula) attraverso le membrane, e CASD1, un enzima noto per trasferire gruppi acetile sugli acidi sialici. Utilizzando l’editing genetico in linee cellulari umane e di criceto, hanno rimosso SLC33A1 e osservato cosa accadeva su specifici gangliosidi. Le cellule prive di SLC33A1 potevano ancora sintetizzare i gangliosidi di base GD3 e GD2, ma perdevano completamente le loro forme 9‑O‑acetilate, una modifica caratteristica collegata al cancro e alla funzione neuronale. Reintrodurre SLC33A1 umano ha ripristinato questi gangliosidi acetilati, dimostrando che SLC33A1 è un fornitore cruciale di acetil‑CoA per questa via. 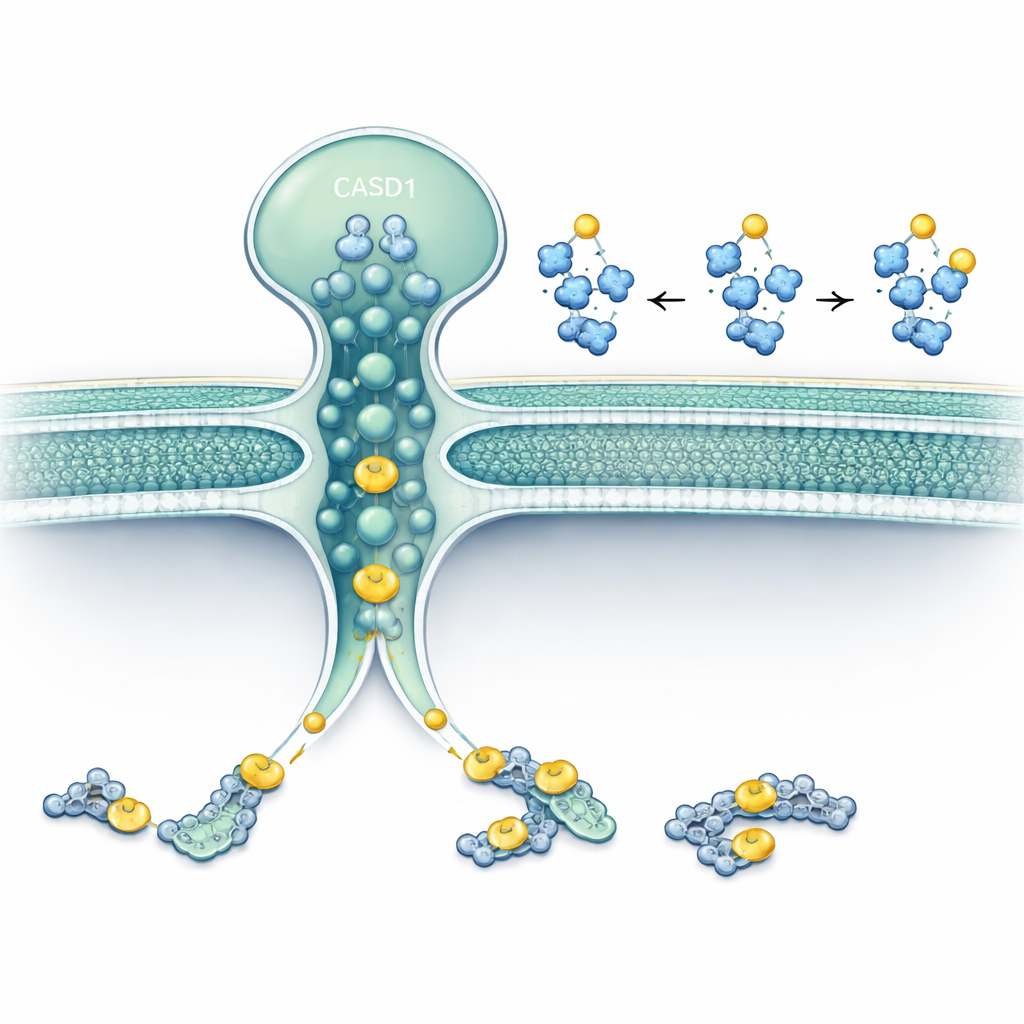
Mutazioni nei pazienti rivelano rilevanza clinica
SLC33A1 è stato implicato in diverse condizioni neurologiche rare, tra cui una grave malattia infantile (sindrome di Huppke–Brendel), una forma di paraplegia spastica ereditaria e atassia cerebellare ad insorgenza tardiva. Il team ha ricreato quattro varianti di SLC33A1 derivate da pazienti in cellule prive del trasportatore normale e ha testato se queste proteine alterate potessero ripristinare l’acetilazione dei gangliosidi. Tutte e quattro mostravano una funzione ridotta, e le mutazioni più gravi ad esordio infantile ripristinavano a malapena alcuna acetilazione. Guidati da una struttura tridimensionale recentemente risolta di SLC33A1, gli autori hanno mappato queste mutazioni sulla proteina e mostrato come probabilmente ne compromettano l’architettura o la capacità di legare acetil‑CoA. Ciò suggerisce con forza che l’incapacità di acetilare correttamente i gangliosidi contribuisca ai sintomi neurologici osservati nei pazienti.
Un secondo sito attivo nascosto in CASD1
Il lavoro ha inoltre rivelato una svolta inaspettata: CASD1 sembra essere un enzima a doppio scopo. La sua porzione nota nel lume del Golgi usa l’acetil‑CoA fornito da SLC33A1. Ma quando SLC33A1 è stato eliminato, le cellule sono comunque riuscite ad aggiungere un singolo gruppo acetile su certi acidi sialici in alcune condizioni, sebbene non riuscissero ad aggiungere il secondo gruppo acetile necessario per schemi più complessi. Utilizzando predizioni strutturali avanzate e simulazioni molecolari, gli autori hanno dimostrato che la parte transmembrana di CASD1 somiglia molto a un acetiltransferasi transmembrana nota dei lisosomi. Hanno individuato aminoacidi chiave in questa regione che legano acetil‑CoA sul lato citosolico e trasferiscono il gruppo acetile attraverso la membrana direttamente all’acido sialico. Quando questi residui sono stati mutati, CASD1 ha perso questa seconda attività sia in saggi in vitro sia in cellule vive.
Due vie, un codice zuccherino finemente regolato
I dati supportano nel complesso un modello a “due siti catalitici”. Una via dipende da SLC33A1 che porta acetil‑CoA nel lume del Golgi, dove il dominio luminale di CASD1 aggiunge un gruppo acetile all’acido sialico, permettendo schemi di acetilazione semplici e doppi. L’altra via è incorporata nel nucleo transmembrana di CASD1, che attinge direttamente all’acetil‑CoA citosolico e può comunque eseguire un livello base di acetilazione anche quando SLC33A1 manca. In termini semplici, ciò significa che un unico enzima, alimentato da due diverse riserve di acetile, scrive sottili “segni di punteggiatura” sugli zuccheri di superficie cellulare. Quando il trasportatore o una delle parti dell’enzima è difettoso, questi segni risultano spostati o mancanti, il che può contribuire a spiegare alcune malattie neuroevolutive e neurodegenerative e mette in luce un nuovo livello di regolazione di come le cellule modellano la propria identità esterna.
Citazione: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
Parole chiave: acido sialico, acetilazione del Golgi, gangliosidi, SLC33A1, CASD1