Clear Sky Science · it
La N‑acetiltransferasi B associata al ribosoma coordina la proteostasi globale e l'autofagia nelle piante creando Ac/N‑degroni
Come le piante mantengono l'equilibrio delle loro proteine
Ogni cellula di una pianta è piena di proteine che devono essere costantemente sintetizzate, riparate e rimosse. Quando questo equilibrio vacilla, la crescita rallenta e lo stress può diventare letale. Questo studio rivela come un piccolo tag chimico posto all'estremità iniziale di molte proteine aiuti le piante a decidere quali proteine riciclare rapidamente e quanto intensamente attivare un processo interno di pulizia chiamato autofagia. Comprendere questo sistema di controllo spiega come le piante sopravvivono a lunghi periodi senza luce o nutrienti e potrebbe un giorno aiutarci a selezionare colture più resistenti a condizioni difficili.
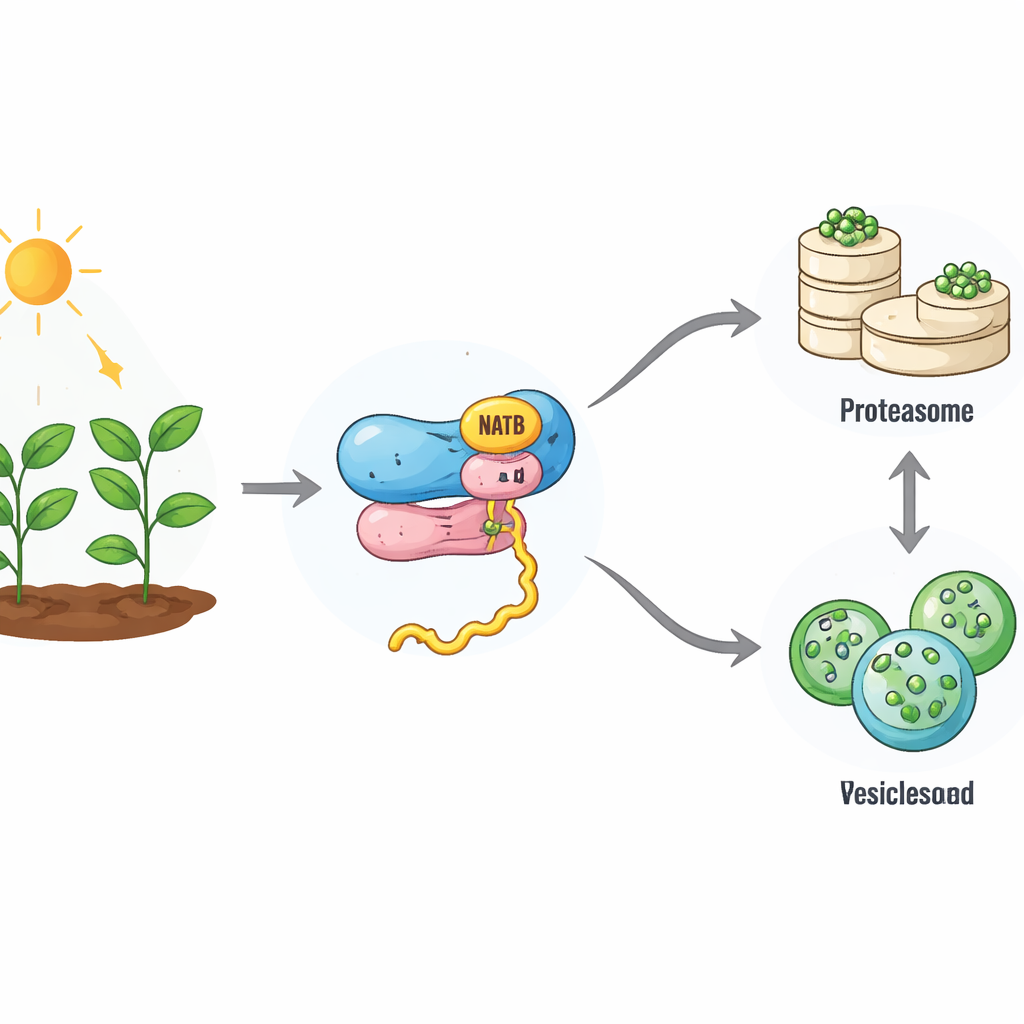
Un piccolo tag con grandi conseguenze
Durante la sintesi delle nuove proteine sui ribosomi, esse possono essere “incappate” da un gruppo chimico alla loro estremità N‑terminale. Nelle piante, un complesso enzimatico legato al ribosoma chiamato NatB aggiunge questa cappatura a circa un quinto di tutte le proteine. Fino ad oggi, gli scienziati non comprendevano appieno cosa significhi questa marcatura così diffusa per il destino di quelle proteine. Utilizzando l'editing genico CRISPR per disattivare la parte catalitica di NatB in Arabidopsis, gli autori hanno creato piante che in gran parte mancano di questa modificazione sui consueti bersagli di NatB. Sorprendentemente, queste piante erano nanizzate ma sopravvivevano, a differenza degli animali privi di NatB, suggerendo che le cellule vegetali possano compensare in parte la perdita. Tuttavia molte proteine che normalmente portano il marcatore NatB sono risultate solo parzialmente o per nulla modificate, offrendo una finestra sul funzionamento di questo sistema.
Ricambio proteico più lento e uno spostamento nel sistema di riciclo cellulare
Quando il gruppo ha misurato la velocità di degradazione delle proteine, ha rilevato che le piante senza NatB presentano una macchina di riciclo cellulare rallentata. La principale via di distruzione delle proteine, il sistema ubiquitina‑proteasoma, funzionava meno efficacemente: la sua attività è diminuita e le proteine destinate a questa via portavano meno dei consueti segnali “da eliminare”. Contemporaneamente è calato anche il tasso complessivo di nuova sintesi proteica. Indagini proteomiche dettagliate hanno mostrato che molte proteine dipendenti da NatB risultavano ora più stabili e si accumulavano nella cellula, indicando che il tag NatB normalmente contribuisce a rendere alcune proteine componenti a vita breve. Tuttavia non tutti i bersagli di NatB si comportavano in questo modo, indicando un effetto più selettivo modellato dalla sequenza e dal contesto di ciascuna proteina.
L'autofagia interviene come piano di riserva
Lo studio ha rivelato che, quando la via del proteasoma rallenta, un'altra via di riciclo si attiva. Questo secondo sistema, l'autofagia, racchiude porzioni della cellula in bolle di membrana che vengono consegnate a un compartimento dove il contenuto viene degradato e riutilizzato. Le piante prive di NatB mostravano livelli più elevati delle proteine core dell'autofagia e un flusso maggiore di materiale attraverso questa via, soprattutto durante il buio quando l'energia scarseggia. Le piante senza NatB sopravvivevano molto più a lungo in condizioni di oscurità prolungata o sotto carenza di azoto e zolfo rispetto alle piante normali, ma questo vantaggio scompariva quando i geni dell'autofagia venivano disattivati. Ciò indica che l'aumento dell'autofagia aiuta a compensare l'indebolimento del sistema del proteasoma, evitando il collasso dell'economia proteica cellulare.
Un sensore energetico chiave al centro dell'interruttore
Per capire cosa sposta l'equilibrio dall'uso del proteasoma verso l'autofagia, gli autori si sono concentrati su un complesso proteico sensore energetico chiamato SnRK1. Due subunità strettamente correlate, KIN10 e KIN11, iniziano con sequenze che le rendono probabili clienti di NatB. I ricercatori hanno dimostrato che NatB può marcare direttamente queste proteine in saggi in vitro. Nelle piante privi di NatB, solo KIN11 si accumulava fortemente, e la sua forma attiva fosforilata era più abbondante. Il monitoraggio accurato della degradazione proteica ha rivelato che quando KIN11 porta il tag NatB viene più facilmente destinata alla distruzione tramite proteasoma, mentre KIN11 non marcata persiste. Le piante che mancavano sia di NatB sia di KIN11 perdevano la resistenza aggiuntiva allo stress da oscurità, mentre piante ingegnerizzate per sovraesprimere KIN11 da sole diventavano più tolleranti all'oscurità prolungata. Questi risultati individuano KIN11 come un messaggero cruciale che, quando stabilizzato, spinge la cellula a favorire l'autofagia e la conservazione energetica.
Cosa significa per la sopravvivenza delle piante
In termini semplici, NatB scrive un marchio rimovibile di “usa e scarta” su proteine specifiche, incluso il sensore energetico KIN11. Quando NatB è attivo, KIN11 è tenuta sotto controllo, il ricambio proteico tramite il proteasoma è veloce e le piante crescono rapidamente in condizioni favorevoli. Quando l'attività di NatB viene persa o ridotta, KIN11 viene risparmiata dalla distruzione rapida, l'autofagia aumenta e le piante entrano in una modalità di sopravvivenza che conserva risorse e affronta meglio lunghi periodi di oscurità o scarsa nutrizione. Questo lavoro rivela NatB come un coordinatore centrale tra due principali sistemi di riciclo nelle cellule vegetali e spiega come un sottile tag chimico all'inizio di una proteina possa far pendere l'equilibrio tra crescita e resistenza.
Citazione: Gong, X., Pożoga, M., Boyer, JB. et al. The ribosome-associated N-terminal acetyltransferase B coordinates global proteostasis and autophagy in plants by creating Ac/N-degrons. Nat Commun 17, 3116 (2026). https://doi.org/10.1038/s41467-026-71208-2
Parole chiave: controllo qualità delle proteine, autofagia, tolleranza allo stress nelle piante, modificazione post‑traduzionale, degradazione delle proteine