Clear Sky Science · it
Dinâmica strutturale di midnolin-proteasoma durante il ricambio di substrati indipendente dall’ubiquitina
Come la cellula elimina rapidamente i rifiuti
All’interno di ogni cellula, le proteine vengono continuamente sintetizzate e distrutte. Molte vengono etichettate con piccole molecole chiamate ubiquitina prima di essere immesse nella principale macchina di riciclo cellulare, il proteasoma. Ma alcune proteine nucleari devono essere eliminate così in fretta che non c’è tempo per l’etichettatura. Questo studio rivela come una proteina ausiliaria poco nota, midnolin, si inserisca direttamente nel proteasoma per eliminare questi bersagli urgenti, offrendo indizi su come le cellule mantengano il controllo dell’attività genica in modo rapido e stringente.
Una scorciatoia verso il trituratore cellulare
Il proteasoma 26S è un complesso a forma di barile che sminuzza le proteine in piccoli frammenti. Tradizionalmente riconosce i bersagli leggendo catene di ubiquitina attaccate a questi ultimi. Studi recenti hanno scoperto una via alternativa: una «scorciatoia» in cui midnolin accompagna alcune proteine nucleari—soprattutto i prodotti dei geni ad attivazione immediata che attivano e disattivano i geni molto rapidamente—direttamente al proteasoma senza alcun marchio di ubiquitina. Queste proteine, come fattori di trascrizione coinvolti nelle risposte allo stress e nell’infiammazione, devono comparire e scomparire in pochi minuti. Il nuovo articolo combina microscopia crioelettronica ad alta risoluzione con esperimenti biochimici per mappare, quasi fotogramma per fotogramma, come midnolin si aggancia al proteasoma e posiziona il suo carico per la distruzione.
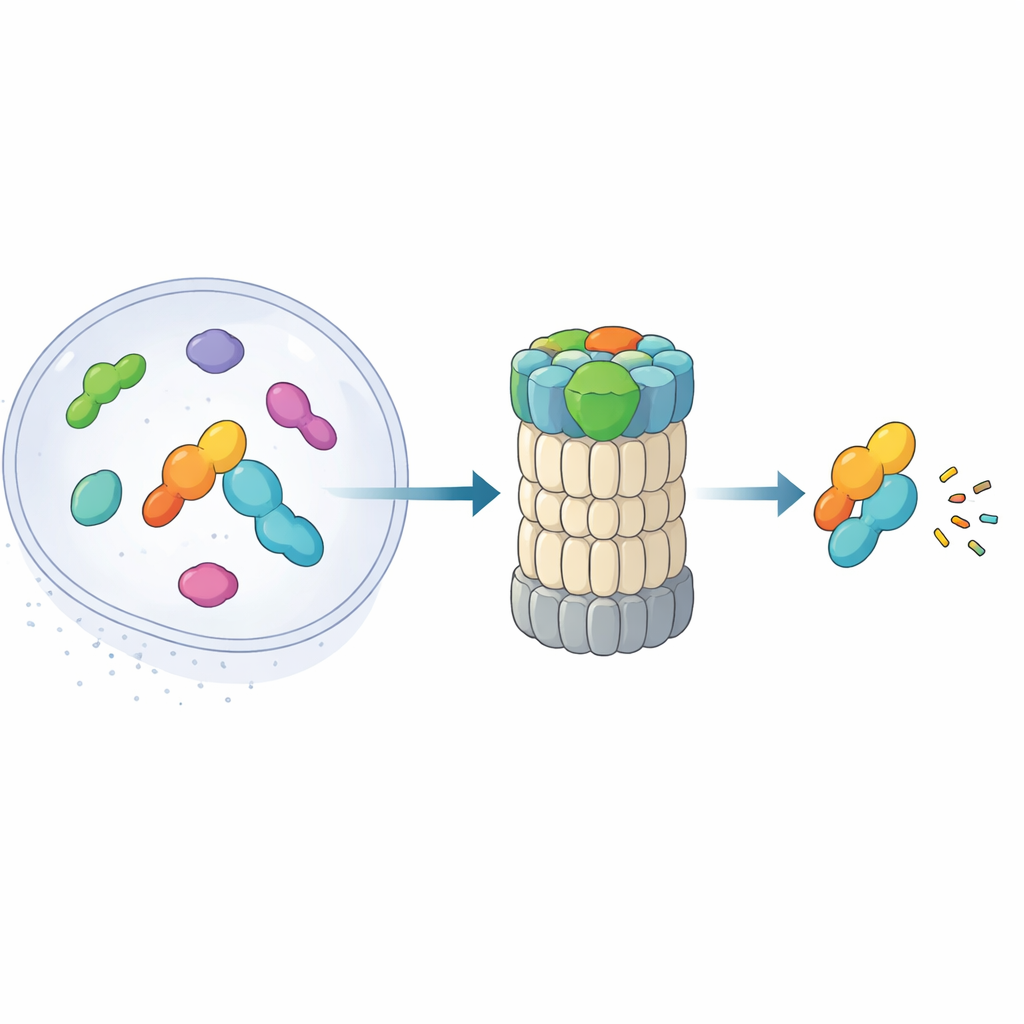
L’aiutante in tre parti che afferra e mira i bersagli
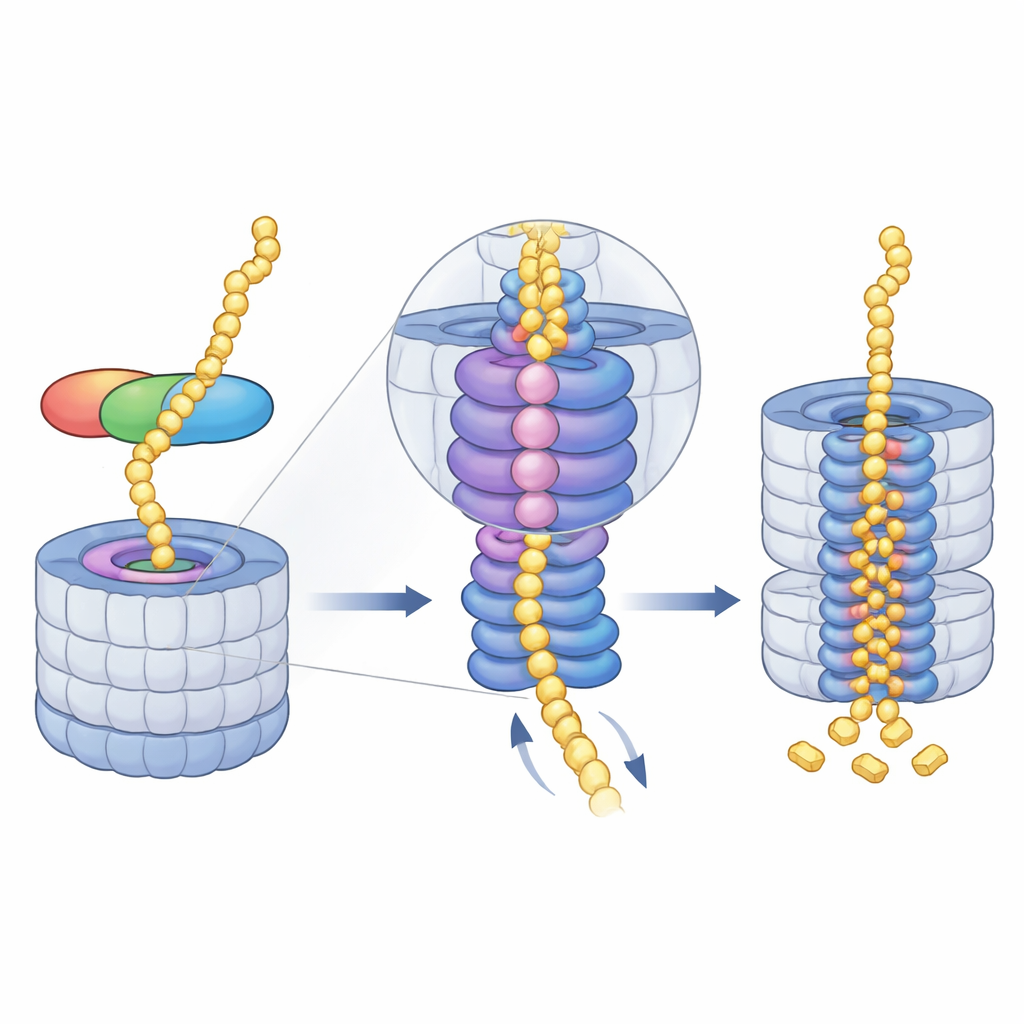
Midnolin funziona come un multiutensile con tre moduli chiave. Un’estremità, un’elica C-terminale, si inserisce in un sito di ancoraggio su una componente del proteasoma chiamata RPN1, fissando midnolin alla macchina di riciclo. Una regione centrale, definita «Catch», riconosce e afferra una specifica struttura filamentosa (un degron) nelle proteine bersaglio. All’estremità opposta si trova un dominio simile all’ubiquitina. Sorprendentemente, questo dominio non è principalmente per legare il proteasoma, come avviene in proteine shuttle simili. Gli autori mostrano invece che si adagia contro RPN11, un enzima che normalmente rimuove l’ubiquitina dai substrati. Qui, RPN11 agisce più come uno scaffold: abbracciando il segmento ubiquitina-similare di midnolin, aiuta a mantenere la regione Catch e il suo carico direttamente sopra il restringimento d’ingresso nel proteasoma.
Guidare la proteina nel nucleo triturante
Una volta che midnolin si è ancorato, prende il sopravvento il motore energivoro del proteasoma—un anello AAA+ ATPasi. Questo anello si trova appena sotto il poro d’ingresso e tira le catene proteiche disfatte nel nucleo, passo dopo passo. Gli istantanee da crio-EM rivelano una serie di posizioni a «scala a chiocciola» assunte dai sei subunità del motore mentre afferrano e trasferiscono il substrato attraverso il canale centrale. Gli autori hanno catturato quattro stadi consecutivi di questo ciclo, tutti con materiale legato a midnolin infilato attraverso il poro, e hanno persino osservato come il rilascio di uno ione magnesio in una subunità coincida con uno spostamento verso il basso dell’intero anello. Ciò suggerisce che l’uso coordinato di ATP e il rilascio di magnesio aiutino a far avanzare a scatti la proteina più in profondità nella camera dove risiedono i siti di taglio.
Perché il posizionamento e la co-espressione contano
Il team ha testato come ciascun modulo di midnolin contribuisca all’efficienza. L’elica di ancoraggio da sola può legare RPN1 ma non aumenta in modo significativo l’attività del proteasoma. Rimuovere la regione Catch lascia molti proteasomi bloccati in uno stato inattivo, privi di substrato, anche se midnolin può ancora attaccarsi; sostituire la Catch con un substrato fuso permanentemente non riesce a ripristinare l’attività completa. Questi risultati indicano che Catch fa più che afferrare il bersaglio—deve anche orientare la proteina in modo preciso all’ingresso del poro. Dati biochimici e trascrittomici tumorali mostrano inoltre che midnolin tende a essere prodotto insieme ai suoi substrati. Quando co‑espresso, midnolin si ripiega meglio e forma complessi stabili, creando un pacchetto «degradami» pronto all’uso che può essere rapidamente consegnato al proteasoma quando la cellula deve ripristinare l’espressione genica.
Autopulizia e potenziali prospettive mediche
Dopo che la proteina bersaglio è stata tirata dentro e sminuzzata, midnolin stesso non viene risparmiato. Le sue regioni non strutturate possono essere infilate nel motore e immesse nella stessa camera di distruzione, assicurando che l’ausiliare non si accumuli inutilmente. Illuminando questa via al proteasoma priva di ubiquitina, lo studio amplia la nostra comprensione di come le cellule gestiscono la vita delle proteine su ritmi molto serrati. Suggerisce anche nuove strategie terapeutiche: ingegnerizzando molecole basate su midnolin che vincolino direttamente le proteine nucleari dannose al proteasoma, i ricercatori potrebbero un giorno eliminare più rapidamente e selettivamente bersagli «non drogabili», inclusi alcuni driver del cancro.
Citazione: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
Parole chiave: proteasoma, midnolin, degradazione proteica, via indipendente dall’ubiquitina, geni ad attivazione immediata