Clear Sky Science · it
La competenza trascrizionale definisce il potenziale di nucleazione dell’eterocromatina delle unità MSR isolate
Interruttori nascosti nel nostro DNA
I nostri genomi sono compattati nel nucleo cellulare in due stati principali: regioni attive che ospitano geni e tratti fortemente compattati a lungo considerati la “materia oscura” genetica. Questo studio pone una domanda apparentemente semplice: che cosa indica a un tratto di DNA di diventare questo materiale altamente compattato e silenziante dei geni—noto come eterocromatina—in primo luogo? Analizzando una specifica classe di DNA ripetuto nel topo, gli autori rivelano che non tutte le ripetizioni sono uguali: solo quelle in grado di supportare un tipo particolare di trascrizione possono azionare l’interruttore che costruisce e mantiene questi vicinati silenti del DNA.
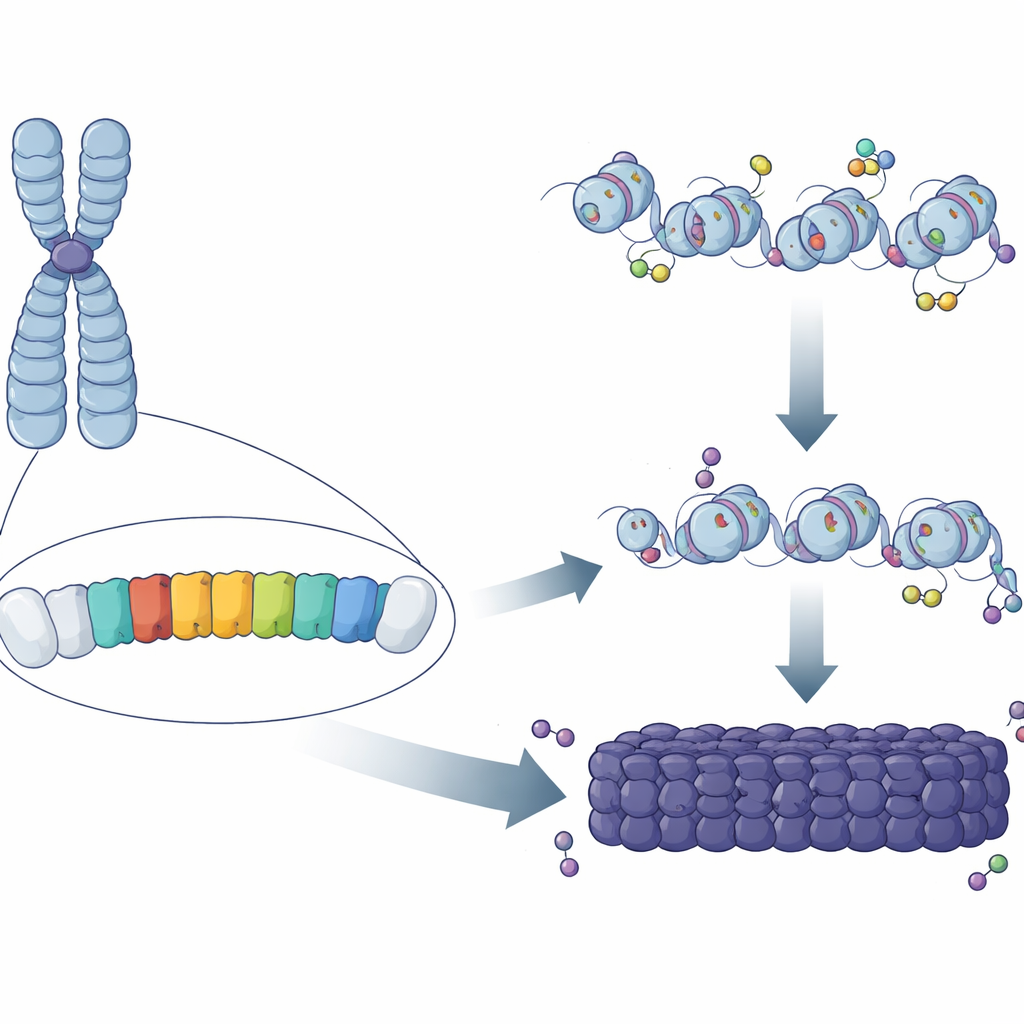
Pattern ripetuti nel genoma
Quasi la metà del DNA dei mammiferi è costituita da sequenze ripetute, molte delle quali raggruppate in regioni attorno al centro del cromosoma. Nel topo, uno dei componenti principali di queste regioni è la “major satellite repeat” (MSR), una breve sequenza ricca di A/T copiata centinaia di migliaia di volte. Lavori classici hanno mostrato che queste regioni sono rivestite di marche chimiche e proteine che bloccano il DNA in uno stato compatto e protettivo. Tuttavia restava un mistero perché alcune copie di MSR diventassero completamente eterocromatiche mentre altre, disperse altrove nel genoma, non lo facevano. Gli autori hanno ipotizzato che piccole differenze nella sequenza o nel comportamento di singole unità MSR potessero determinare se esse siano in grado di innescare, o “nucleare”, una porzione di eterocromatina.
Costruire un sito di prova nel genoma
Per testare questa idea in modo pulito, il gruppo ha ingegnerizzato cellule staminali embrionali di topo per contenere una piattaforma artificiale in un tratto silenzioso del cromosoma 2—una regione senza geni o ripetizioni vicine e senza attività rilevabile. In questo sito neutro hanno inserito diversi frammenti di DNA: unità MSR intatte, varianti MSR fortemente rimescolate e elementi di controllo come promotori virali o sezioni di elementi mobili. Questo ha permesso di chiedere, unità per unità, quali sequenze sono in grado di attrarre le caratteristiche distintive dell’eterocromatina: un segno chimico specifico sulle proteine istoniche (H3K9me3), il legame delle proteine HP1 e l’incorporazione dell’istone linker H1, tutte caratteristiche che insieme addensano e stabilizzano la cromatina locale.
Sono solo le ripetizioni pronte per la trascrizione a generare cromatina silente
I risultati sono stati sorprendentemente selettivi. Una singola unità MSR intatta inserita nel sito di prova non era sufficiente a modificare la cromatina. Tuttavia, tre o più copie tandem della sequenza MSR intatta convertirono la regione circostante in un “isolotto” di eterocromatina, con forte H3K9me3, HP1 e istone H1. Al contrario, tratti della stessa lunghezza di sequenze MSR rimescolate, o di un altro tipo di ripetizione (la regione 5' non tradotta del LINE-1), non riuscirono a farlo, anche se potevano sostenere una trascrizione intensa. La differenza chiave era che le unità MSR intatte multi-copia supportavano una modesta trascrizione bidirezionale che produceva brevi molecole di RNA non standard strettamente associate alla cromatina. Questo schema, piuttosto che una trascrizione alta e simile a quella genica, correlava con la capacità di nucleare l’eterocromatina.
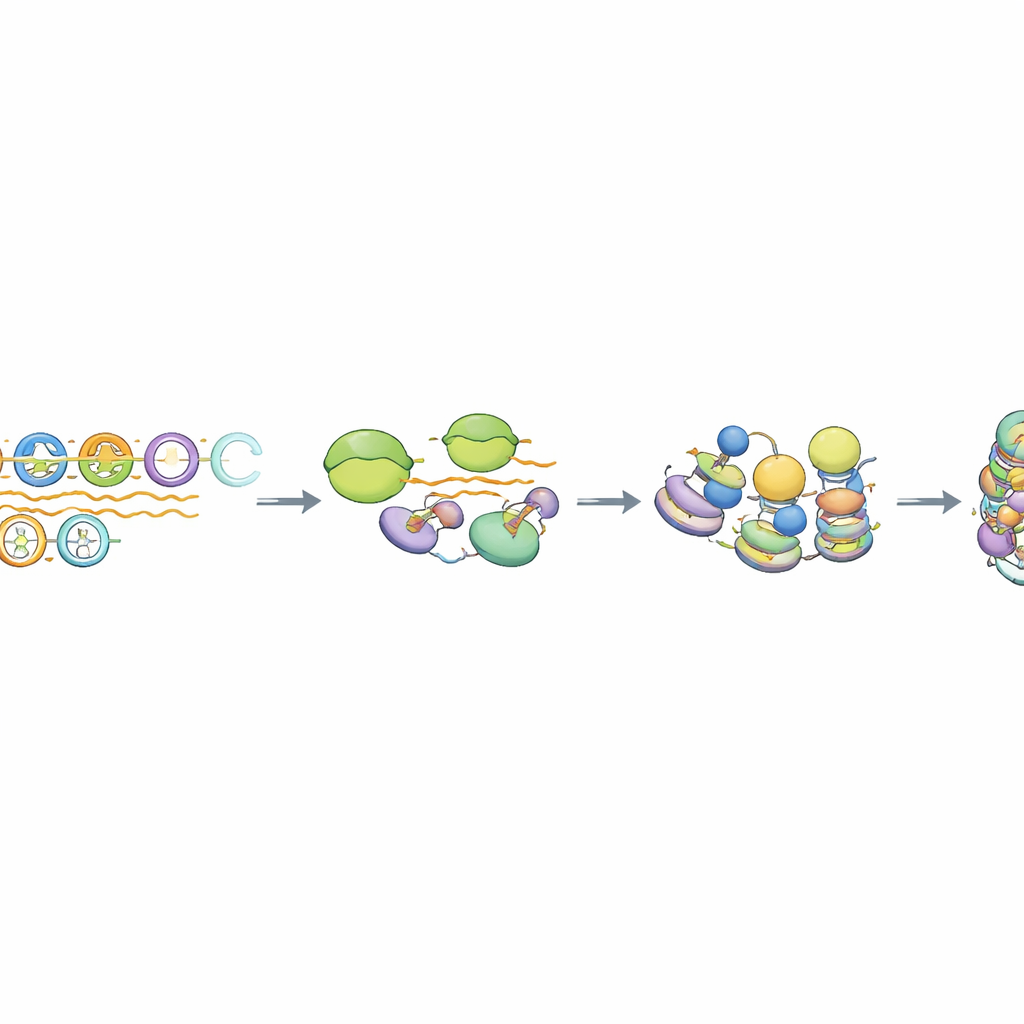
Un tipo speciale di trascrizione e processamento dell’RNA
Approfondendo, gli autori hanno scoperto che la RNA polimerasi II, l’enzima che normalmente produce RNA messaggero, si impegna brevemente con gli array MSR ma non procede in modo efficiente verso trascritti lunghi. Gli RNA risultanti mancano dei caratteri tipici degli mRNA come il cappuccio 5' protettivo e lunghe code poli‑A, e rimangono vicino al DNA che li ha prodotti. Una macchina proteica chiamata complesso Integrator, nota per rifinire e terminare certi RNA non codificanti, risultò specificamente arricchita presso le unità MSR intatte. Quando l’attività di taglio dell’Integrator fu ridotta, i livelli di RNA derivati da MSR aumentarono sostanzialmente, ma il marcatore istonico repressivo principale rimase mentre il legame di HP1 cambiò in modo sottile. L’analisi a livello di genoma mostrò che solo il ~10–15% delle copie MSR più integre si comporta in questo modo, evidenziando un sottoinsieme di ripetizioni “competenti” programmato per questa via di silenziamento accoppiata alla trascrizione.
DNA srotolato che imita un promotore
Il gruppo ha anche esplorato come lo stesso DNA MSR favorisca questa trascrizione insolita. Gli array MSR multi‑copia, ma non le copie singole o doppie, mostravano chiari segnali di DNA localmente srotolato e ibridi RNA:DNA, caratteristiche strutturali spesso osservate vicino a promotori attivi e siti di pausa. Queste configurazioni erano amplificate quando gli enzimi topoisomerasi venivano inibiti, e coincidevano con una maggiore trascrizione delle MSR e con caratteristiche di eterocromatina più forti. Gli autori propongono che tre o più unità MSR in tandem creino una topologia del DNA che imita un promotore, invitando la polimerasi e i fattori di trascrizione a ingaggiare quanto basta per generare brevi RNA che, insieme a proteine specifiche, rinforzano un’architettura della cromatina compatta.
Perché questo è importante per la salute del genoma
Per un osservatore non specialistico, questo lavoro rivela che parti del nostro DNA “spazzatura” funzionano come interruttori finemente tarati, usando una combinazione di conformazione del DNA, trascrizione a basso livello e processamento dell’RNA per costruire l’involucro protettivo del genoma. Solo le unità MSR in grado di supportare questa trascrizione controllata e non messaggera possono innescare nuova eterocromatina, mentre elementi rimescolati o eccessivamente attivi non ci riescono. Questa logica basata su DNA/RNA aiuta a spiegare come le cellule distinguano tra regioni da mantenere silenti e altre che possono ospitare geni, e perché RNA satellitari mal regolati siano associati a cancro e problemi dello sviluppo. In sostanza, lo studio mostra che il “fondo” ripetitivo del genoma non è un riempitivo passivo, ma un attore attivo nell’ingegneria dell’architettura nucleare e della stabilità.
Citazione: Lo, YH., Shukeir, N., Erikson, G. et al. Transcriptional competence defines the heterochromatin nucleating potential of isolated MSR units. Nat Commun 17, 2653 (2026). https://doi.org/10.1038/s41467-026-70991-2
Parole chiave: eterocromatina, DNA satellite, RNA non codificante, struttura della cromatina, stabilità del genoma