Clear Sky Science · it
Eterogeneità spaziale delle MDSC mediata dal segnalamento ANXA1‑FPRs guida la soppressione immunitaria nella progressione dell’OSCC
Perché le difese dell’organismo faticano contro alcuni tumori della bocca
Il carcinoma squamoso orale, una forma comune di tumore orale, spesso resiste ai trattamenti oncologici più promettenti di oggi: le immunoterapie che liberano le difese dell’organismo. Questo studio pone una domanda semplice ma cruciale: perché cellule immunitarie potenti, che dovrebbero riconoscere e distruggere il cancro, falliscono così spesso in questi tumori? Mappando la posizione delle diverse cellule all’interno del tumore e come comunicano tra loro, i ricercatori rivelano un gioco mutevole di "gatto e topo" tra cellule tumorali, cellule soppressorie immunitarie e linfociti T citotossici che aiuta a spiegare il fallimento terapeutico — e suggerisce un modo per correggerlo. 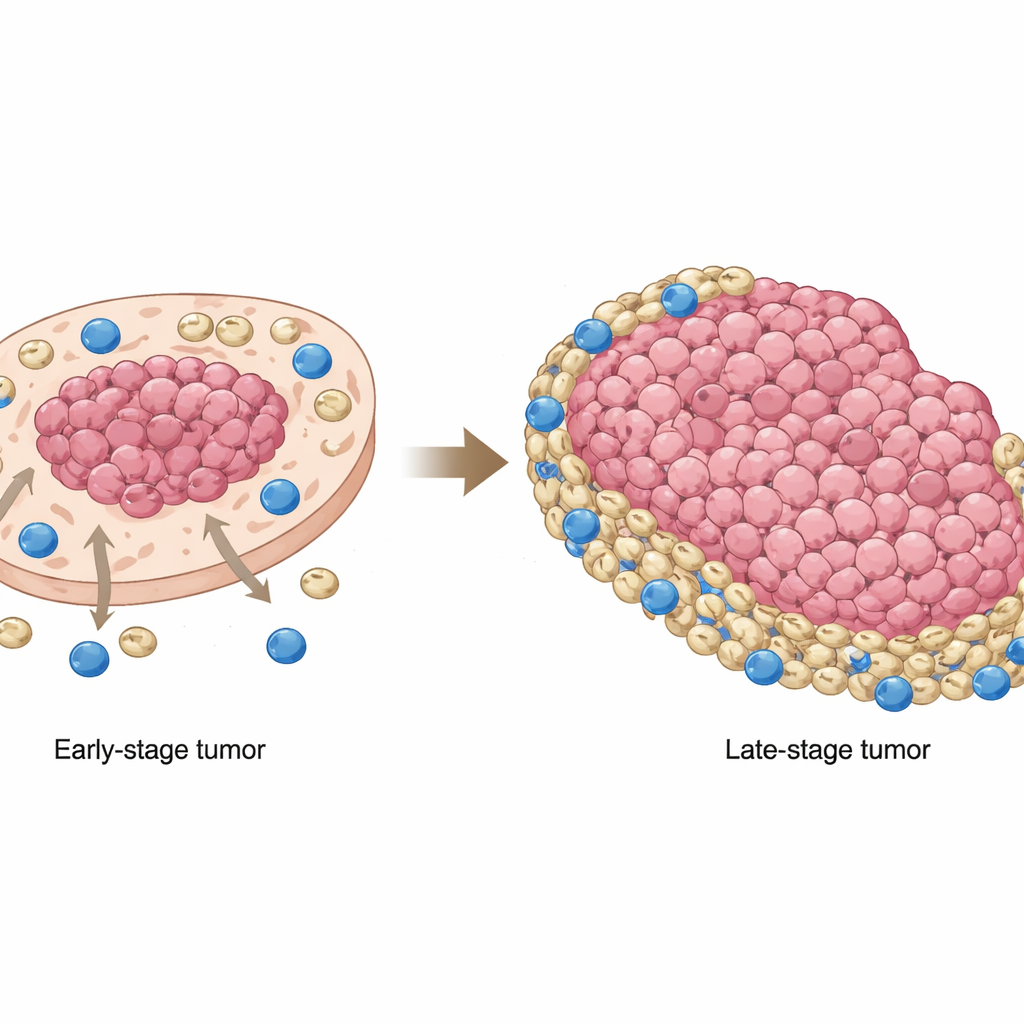
Il paesaggio nascosto all’interno di un tumore
Gli autori hanno combinato due approcci all’avanguardia: il sequenziamento dell’RNA a singola cellula, che legge l’attività delle singole cellule, e la trascrittomica spaziale, che mostra dove si trovano quelle cellule nei campioni di tessuto tumorale. Analizzando tumori di pazienti con carcinoma orale in stadio precoce e avanzato, hanno identificato i principali protagonisti cellulari: cellule epiteliali cancerose, linfociti CD8 citotossici, altri linfociti T e B, fibroblasti che costituiscono il supporto strutturale e cellule immunitarie specializzate chiamate cellule soppressorie di derivazione mieloide (MDSC). Mentre i tumori precoci contenevano più linfociti CD8 attivi, i tumori in stadio avanzato mostravano segnali T più deboli e segnali immunosoppressivi più forti dalle cellule mieloidi, indicando un ambiente progressivamente più ostile per l’immunità antitumorale.
Cellule soppressorie in movimento
Una delle osservazioni più rilevanti è stata come la posizione delle MDSC cambiasse con l’avanzare del tumore. Nei tumori in stadio precoce, queste cellule soppressorie tendevano a raggrupparsi all’interno delle regioni ricche di cellule tumorali, vicino al nucleo tumorale. Negli stadi successivi, si spostavano verso l’esterno, accumulandosi in aree povere di cellule tumorali e ai margini, dove i linfociti CD8 erano più frequenti. Ciò comportava che nei tumori avanzati i linfociti citotossici fossero in gran parte relegati alle periferie e si trovassero di fronte a una cintura di MDSC che attenuava la loro capacità di attaccare le cellule tumorali. Campioni di pazienti e modelli murini hanno confermato che questa ridistribuzione non era una semplice curiosità: quando le MDSC si sovrapponevano meno alle cellule tumorali e invece si stabilivano in regioni non tumorali, i pazienti avevano una sopravvivenza complessiva peggiore. 
Un interruttore di segnalazione tra cellule tumorali e soppressorie
Lo studio ha approfondito una "conversazione" molecolare tra cellule tumorali e MDSC che coinvolge una proteina chiamata annexina A1 (ANXA1) sulle cellule tumorali e una famiglia di recettori chiamata FPR sulle cellule mieloidi. Nelle fasi iniziali della malattia, ANXA1 sulle cellule tumorali interagiva fortemente con FPR1 e FPR3, in particolare su MDSC e macrofagi associati al tumore, contribuendo a reclutare e mantenere queste cellule soppressorie nel nucleo tumorale. Con la progressione del cancro, i livelli di ANXA1 sulle cellule tumorali diminuivano, indebolendo queste connessioni iniziali. Allo stesso tempo, un numero maggiore di MDSC cominciava a esprimere un altro recettore, FPR2, ed emergeva il segnalamento ANXA1–FPR2 come via compensatoria per mantenere l’impegno delle MDSC. Un sottogruppo specifico di cellule tumorali con alti livelli di ANXA1, che mostrava anche caratteristiche simili a cellule staminali, sembrava agire da "esca", attirando le MDSC nelle fasi iniziali; quando ANXA1 calava, le MDSC non erano più ancorate al nucleo e si spostavano verso regioni ricche di CD8.
Spegnere lo scudo per aiutare l’immunoterapia a funzionare
Per verificare se interrompere questa comunicazione potesse migliorare il trattamento, i ricercatori hanno utilizzato un modello murino di carcinoma orale e hanno bloccato FPR2 con un inibitore a piccola molecola chiamato WRW4. Da solo, l’inibizione di FPR2 ha ridotto la presenza di MDSC e aumentato i linfociti CD8 nel microambiente tumorale ma non ha rallentato sufficientemente la crescita tumorale. Allo stesso modo, il trattamento con un anticorpo anti–PD‑1 da solo ha prodotto benefici modesti, perché le MDSC continuavano a formare una barriera soppressiva. Quando entrambi i farmaci sono stati combinati, tuttavia, la crescita tumorale è stata fortemente contenuta e i topi hanno vissuto più a lungo. In questi animali, l’infiltrazione di MDSC è diminuita drasticamente mentre i linfociti CD8 hanno penetrato più in profondità nelle regioni ricche di cellule tumorali, suggerendo che il blocco di FPR2 rimuove uno scudo chiave che normalmente protegge le cellule tumorali dall’attacco immunitario.
Cosa significa questo per la cura del cancro in futuro
Nel complesso, il lavoro mostra che non solo i tipi di cellule ma anche la loro disposizione spaziale e le loro partnership di segnalazione determinano se l’immunoterapia può avere successo nel carcinoma orale. Con l’avanzare del tumore, le MDSC migrano dal centro ai margini, dove intercettano i linfociti citotossici, e il segnalamento ANXA1–FPR2 contribuisce a mantenere questa disposizione soppressiva. Interrompendo questa via — specialmente in combinazione con gli attuali farmaci checkpoint — i medici potrebbero essere in grado di rimodellare il microambiente tumorale in modo che le cellule immunitarie dell’organismo possano nuovamente riconoscere e distruggere il cancro. Questo suggerisce una strategia concreta: associare inibitori di FPR2 con l’immunoterapia potrebbe migliorare gli esiti per i pazienti i cui carcinomi orali attualmente resistono ai migliori trattamenti disponibili.
Citazione: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
Parole chiave: carcinoma squamoso orale, microambiente tumorale, cellule soppressorie di derivazione mieloide, trascrittomica spaziale, immunoterapia oncologica