Clear Sky Science · it
La segnalazione FGFR stabilisce gradienti spaziali di identità delle cellule secretorie lungo l’asse prossimale-distale delle vie aeree
Come le nostre vie aeree ordinano silenziosamente e difendono l’aria che respiriamo
Ogni respiro libera l’aria su milioni di cellule che rivestono la trachea e i polmoni. Queste cellule fanno molto più che fornire una superficie passiva: detossificano gli inquinanti, combattono i germi e aiutano a impedire il collasso dei minuscoli alveoli. Questo studio rivela che le cellule secretorie nelle vie aeree del topo non sono tutte uguali. Piuttosto, sono organizzate in gradienti graduali dalla porzione prossimale (verso la gola) a quella distale (verso il parenchima polmonare), e una via di segnalazione chiave, chiamata FGFR2b, contribuisce a stabilire e mantenere questi cambiamenti graduali nell’identità e nella funzione cellulare. Capire questo ordine nascosto aiuta a comprendere come i polmoni restano sani e cosa può andare storto nelle malattie polmonari croniche.
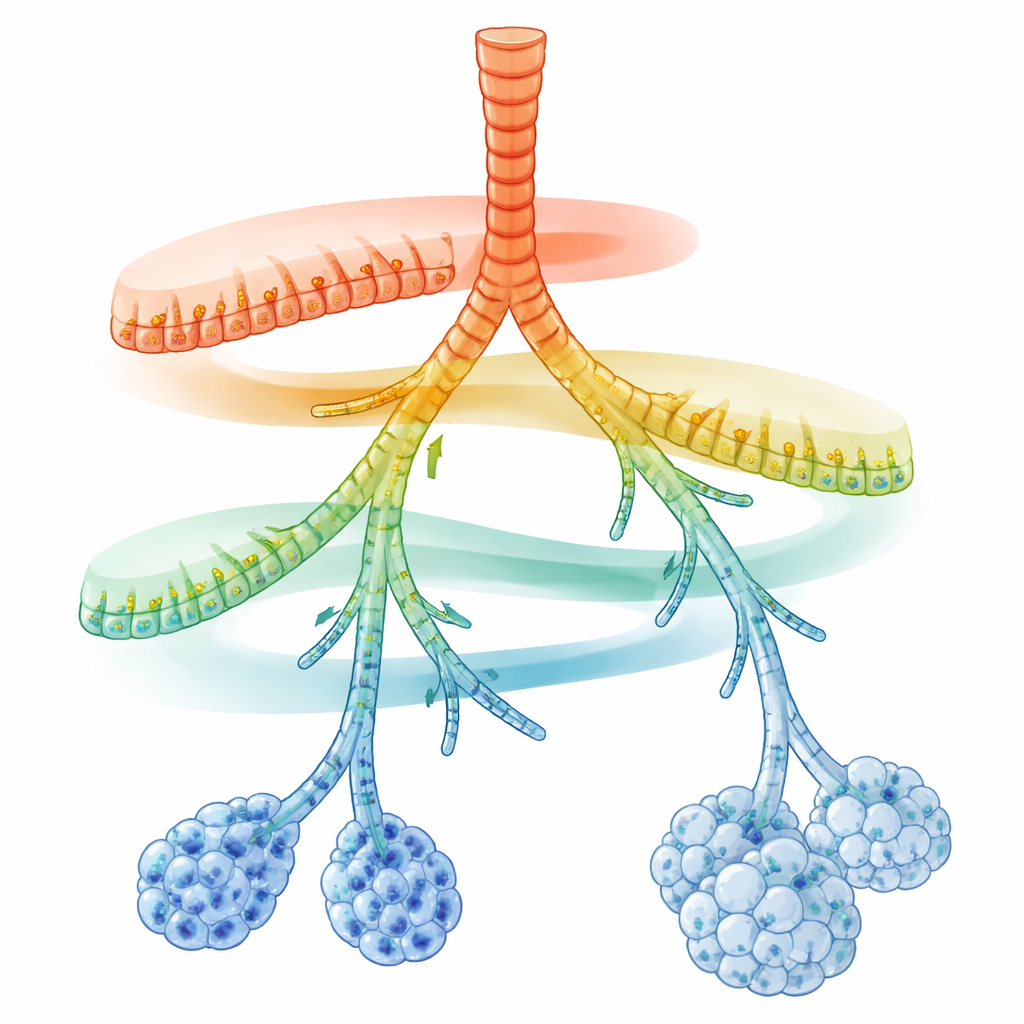
Una mappa nascosta lungo i tubi respiratori
I ricercatori si sono concentrati sulle cellule secretorie, che rivestono i condotti aerei e secernono muco, peptidi antimicrobici e surfattante. Usando il sequenziamento dell’RNA a singola cellula, hanno letto i geni attivi in migliaia di singole cellule provenienti dai polmoni di topo adulto. Proiettando queste cellule su una mappa di similarità molecolare, le cellule secretorie non si sono raggruppate in pochi tipi rigidi. Invece, hanno formato una catena continua di stati che collega le vie aeree grandi agli alveoli. Oltre a un programma centrale condiviso per la detossificazione dei composti inalati, sono emersi due gradienti opposti di espressione genica: vicino alle vie aeree maggiori erano più elevati i geni implicati nella difesa innata rapida; verso i rami più distali e gli alveoli, dominavano i geni per la gestione dei lipidi, la produzione di surfattante e la presentazione degli antigeni.
Da un punto di partenza a molti stati cellulari specializzati
Per capire come emerge questo schema, il team ha marcato i precursori secretori durante la vita fetale tardiva e ha seguito i loro discendenti nell’età precoce con tracciamento di linea cellulare e analisi a singola cellula. Queste cellule marcate formavano inizialmente un pool immaturo con marcata attività della macchina proteica e geni legati alla costruzione tessutale. Dopo la nascita, quando iniziarono la respirazione e l’esposizione all’ambiente esterno, queste cellule si diversificarono gradualmente in diversi gruppi maturi: cellule secretorie prossimali ricche di geni per la difesa innata, cellule più centrali con firme di sviluppo e regolazione, cellule doppio-positive che fanno da ponte tra identità delle vie aeree e alveolari, e cellule alveolari di tipo 2 specializzate per il surfattante. Il programma di detossificazione si attivò precocemente e in modo diffuso, mentre i programmi di immunità innata e presentazione degli antigeni si accesero più tardi e in regioni distinte, indicando che le caratteristiche delle cellule secretorie si acquisiscono secondo una sequenza temporale definita.
Come un segnale di crescita modella l’identità delle vie aeree distali
Un indizio importante su ciò che guida questi gradienti è venuto da un recettore chiamato FGFR2b, parte di una via di segnalazione del fattore di crescita già nota per essere essenziale nelle cellule alveolari di tipo 2. FGFR2b e i suoi geni bersaglio risultavano più attivi nelle cellule delle vie aeree distali e negli alveoli rispetto a quelle prossimali. Quando i ricercatori hanno disattivato FGFR2b specificamente nelle cellule secretorie subito dopo la nascita, il normale programma distale è venuto meno. I geni necessari per la produzione di surfattante e il traffico delle vescicole sono diminuiti, mentre sono aumentati geni tipici delle piatte cellule alveolari di tipo 1, componenti mitocondriali, canali ionici e fattori di sopravvivenza allo stress. Alcune cellule intermedie delle vie aeree hanno iniziato a coesprimere livelli moderati sia di marcatori prossimali per la difesa innata sia di marcatori distali, sfumando di fatto il normale schema spaziale. Negli organoidi coltivati a partire da cellule delle vie aeree, l’aggiunta di ligandi FGFR ha soppresso i marcatori prossimali della difesa innata e potenziato i geni correlati al surfattante in modo coerente con i risultati in vivo, confermando che l’attivazione di FGFR2b è sufficiente a spingere le cellule verso un’identità secretoria distale.
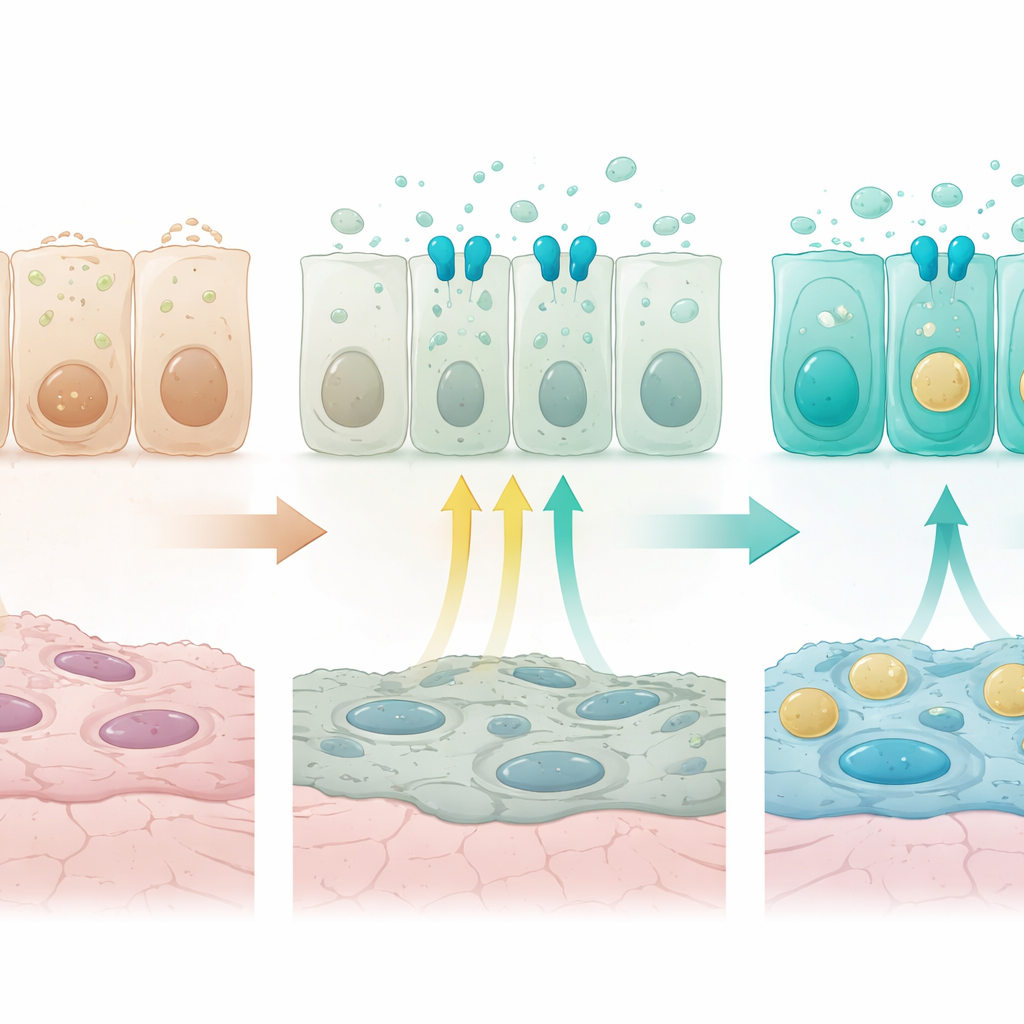
Regolazione fine tramite interazione con altri segnali
Il team ha anche indagato come la segnalazione FGFR2b interagisca con un’altra via mediata da VEGFA, nota soprattutto per modellare i vasi sanguigni. Negli organoidi, la sola VEGFA poteva attenuare alcuni geni della difesa innata, e il blocco del suo recettore alterava certi marcatori distali, ma non poteva sostituire completamente FGFR2b. Infatti, la perdita di FGFR2b in vivo riduceva l’espressione di Vegfa, e la stimolazione combinata di entrambe le vie portava a un feedback che abbassava i livelli di FGFR2b, suggerendo un complesso dialogo incrociato tra questi sistemi di segnalazione. Nei topi adulti, lo spegnimento di FGFR2b non rimodellava più drasticamente i gradienti dell’immunità innata, ma era comunque necessario per mantenere l’espressione di marcatori distali chiave, come il gene del surfattante Sftpb e il classico marcatore secretorio delle vie aeree Scgb1a1, e per preservare le cellule ibride airway–alveolar.
Perché questi gradienti sono importanti per la salute polmonare
Il quadro che emerge è quello di un rivestimento delle vie aeree come paesaggio finemente graduato piuttosto che come un mosaico di zone isolate. Le regioni prossimali sono tarate per una difesa rapida basata sul muco, mentre le regioni distali combinano produzione di surfattante e comunicazione immunitaria più specializzata. La segnalazione FGFR2b contribuisce a stabilire e sostenere questa organizzazione, specialmente nei compartimenti distali, promuovendo programmi legati ai lipidi e alle vescicole e reprimendo caratteristiche inappropriate di tipo prossimale. La perturbazione di questi gradienti, per cause genetiche, ambientali o patologiche, potrebbe alterare l’equilibrio tra difesa, detossificazione e supporto allo scambio gassoso, contribuendo a condizioni in cui le vie aeree distali assumono tratti più prossimali. Questo quadro offre un nuovo modo di pensare ai disturbi polmonari che “ripatternizzano” l’albero bronchiale e può guidare strategie future per riportare l’organizzazione cellulare corretta.
Citazione: Sountoulidis, A., Theelke, J., Liontos, A. et al. FGFR signaling establishes spatial gradients of secretory cell identities along the airway proximal-distal axis. Nat Commun 17, 2651 (2026). https://doi.org/10.1038/s41467-026-70842-0
Parole chiave: epitelio delle vie aeree, cellule secretorie, segnalazione FGFR2b, sviluppo polmonare, gradienti spaziali