Clear Sky Science · it
I canali per protoni governano la chimica carbonatica vescicolare nelle cellule mineralizzanti di un calcificatore marino
Come i minuscoli costruttori modellano il nostro pianeta
Gran parte delle scogliere calcaree e dei reef corallini della Terra è costruita da piccoli artigiani microscopici che prelevano ingredienti disciolti nell’acqua di mare e li trasformano in roccia solida. Questo studio esplora uno di questi costruttori — lo stadio larvale di un riccio di mare — per porre una domanda sorprendentemente fondamentale: come controllano le sue cellule l’acidità mentre costruiscono uno scheletro di carbonato di calcio? La risposta rivela un elegante trucco elettrico che può anche spiegare perché gli organismi marini che formano conchiglie sono così vulnerabili a un oceano più acido.
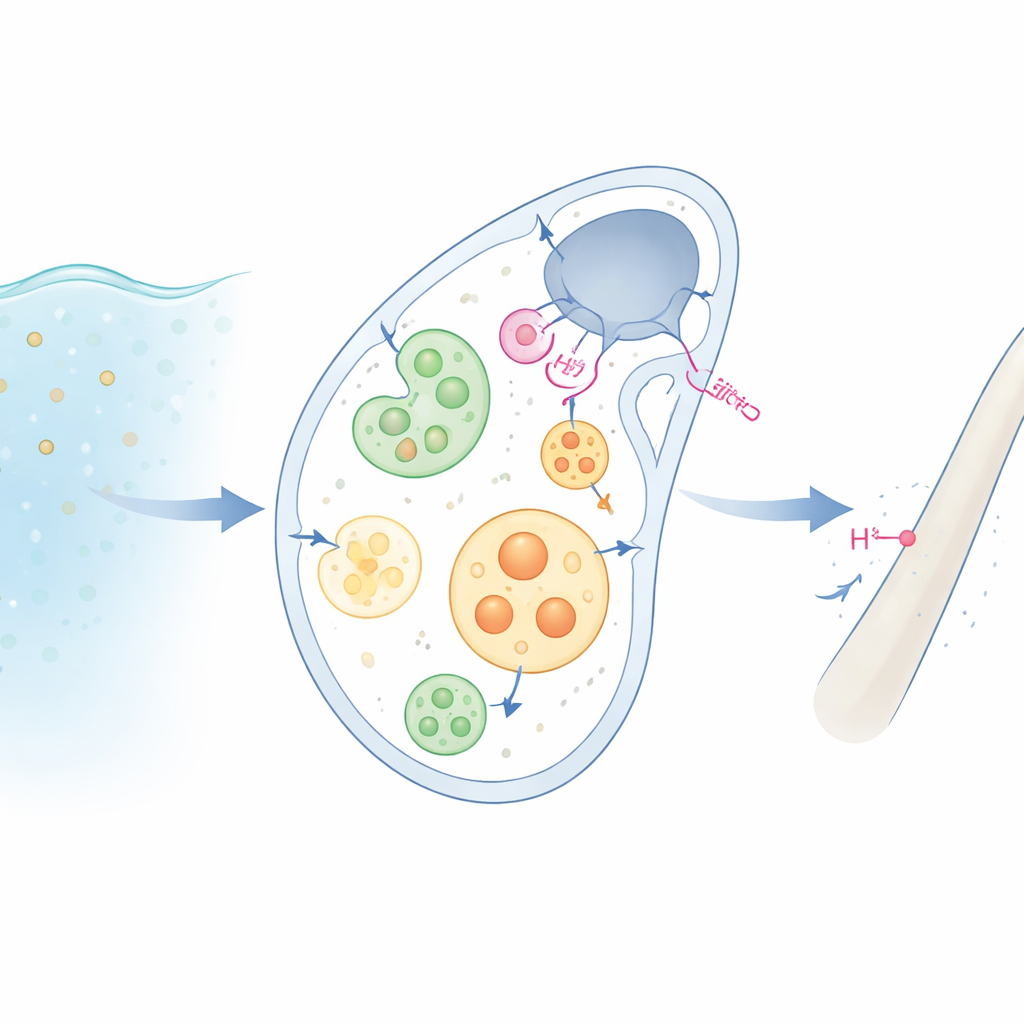
Dall’acqua di mare allo scheletro
Le larve di riccio di mare induriscono il loro corpo con minuscoli bastoncini di calcite composti da carbonato di calcio. Per farlo, cellule specializzate «mineralizzanti» aspirano prima l’acqua di mare, confezionandola in piccole goccioline interne, o vescicole. All’interno di queste goccioline, gli ingredienti per il minerale — calcio, carbonato e altri ioni — vengono concentrati in un precursore amorfo e vitreo che poi si indurisce in cristallo. Ma ogni volta che si forma carbonato di calcio, si produce anche acidità in eccesso (protoni). Se quell’acidità si accumulasse, dissolverebbe il minerale che le cellule stanno cercando di creare. Come le cellule evitino questa autodistruzione è stato a lungo un mistero.
Misurare l’acidità dentro goccioline in movimento
I ricercatori hanno usato imaging in vivo e coloranti fluorescenti sensibili al pH per osservare la chimica all’interno di queste vescicole in tempo reale. Hanno scoperto che quasi la metà delle vescicole era fortemente alcalina — più basica dell’acqua di mare normale — mentre il resto era neutro o leggermente acido. Quando hanno cambiato brevemente l’acidità dell’acqua di mare circostante, sia l’interno delle cellule sia quello delle vescicole si sono spostati, mostrando che i protoni possono muoversi relativamente liberamente attraverso queste membrane. Tuttavia, le vescicole risultavano parzialmente schermate rispetto all’interno della cellula: rispondevano più lentamente e in modo meno marcato, suggerendo una «permeabilità» controllata che aiuta a mantenere condizioni favorevoli alla formazione del minerale.
Perdite elettriche che rimuovono l’acido
Per scoprire cosa crea questa permeabilità, il gruppo si è concentrato su una proteina canale per protoni chiamata Otop2l, precedentemente collegata alla crescita dello scheletro del riccio. Con anticorpi hanno osservato che Otop2l si trova non solo nella membrana esterna delle cellule mineralizzanti ma anche sulle membrane di grandi vescicole interne. Quando hanno ridotto i livelli di Otop2l con un bloccante genetico mirato, sia le cellule sia le loro vescicole sono diventate meno reattive ai cambiamenti di pH esterno, indicando che questo canale è una via principale per l’uscita dei protoni. Registrazioni elettriche in uova di rana e in cellule umane ingegnerizzate per esprimere Otop2l hanno mostrato che il canale si apre ampiamente in condizioni alcaline e in presenza di calcio e magnesio — esattamente la situazione nelle vescicole calcificanti. In sostanza, le cellule sfruttano la loro naturale differenza di voltaggio attraverso la membrana, insieme a Otop2l, per espellere l’acido senza consumare molta energia metabolica.
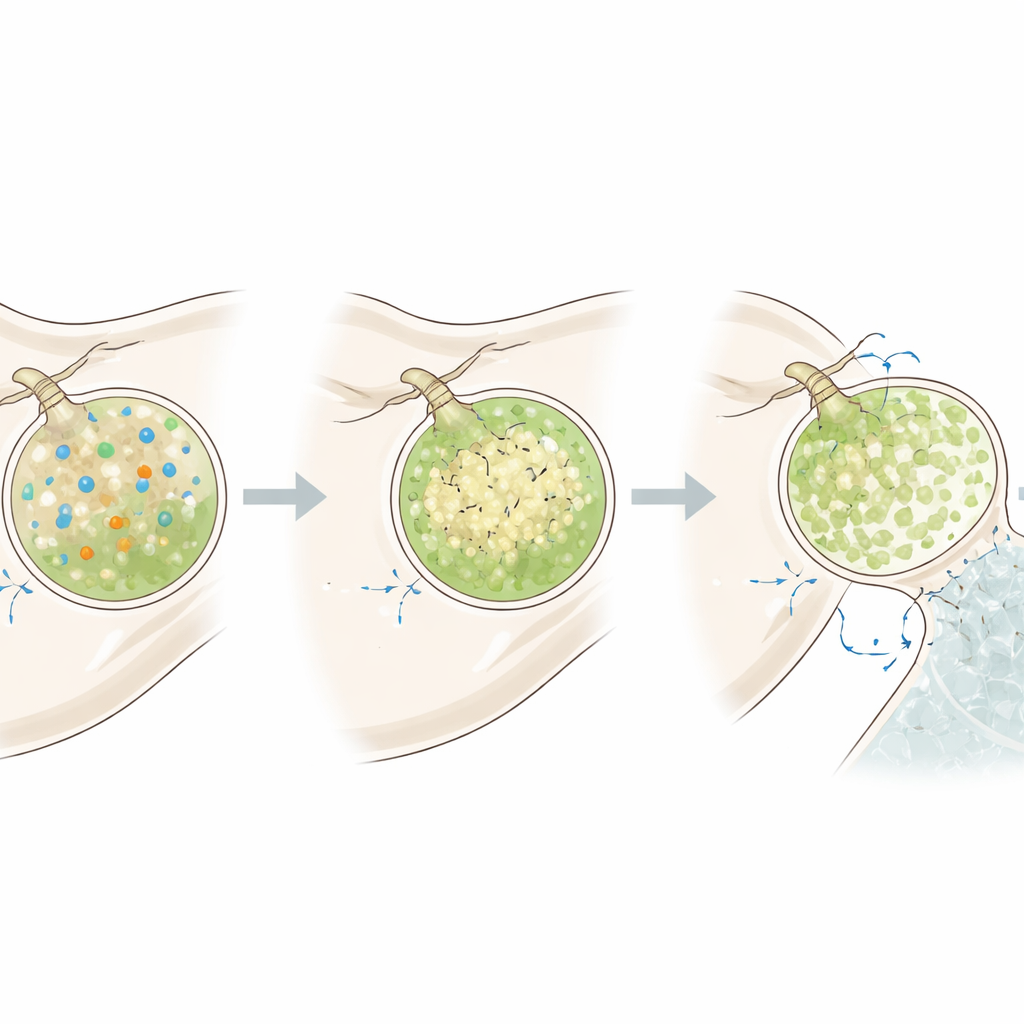
Vescicole che si potenziano per la riparazione
Il gruppo ha poi chiesto cosa accade quando le larve devono ricostruire lo scheletro dopo un danno. Hanno dissolto gli scheletri larvali esponendoli brevemente ad acqua di mare a pH basso, quindi li hanno rimessi in acqua normale e hanno seguito le vescicole durante la ricrescita. In questa fase ad alta richiesta, le cellule mineralizzanti hanno prodotto più vescicole in generale, con un forte aumento di quelle alcaline e ricche di calcio. Queste vescicole riuscivano a recuperare rapidamente il loro pH elevato dopo un impulso acido, e anche l’interno delle cellule divenne più alcalino. Tuttavia il potenziale elettrico delle cellule è rimasto simile, il che implica che esse si adattano principalmente aumentando l’apporto di carbonato e la conduttanza dei protoni piuttosto che cambiando radicalmente il loro stato elettrico.
Perché l’acidificazione degli oceani conta
Messe insieme, le scoperte supportano un modello in cui le cellule mineralizzanti del riccio di mare operano come un sistema «aperto»: endocitosano continuamente acqua di mare, pompano carbonio nelle vescicole e si affidano a canali per protoni e al voltaggio di membrana per scaricare l’acido in eccesso nell’oceano circostante. Questa strategia è efficiente finché il pH esterno rimane nell’intervallo ristretto e stabile che ha caratterizzato gran parte della storia recente della Terra. Ma se l’acqua di mare diventa più acida — come sta accadendo oggi per l’aumento di anidride carbonica — questo flusso verso l’esterno di protoni può indebolirsi o addirittura invertirsi. Il lavoro fornisce quindi una comprensione meccanicistica del motivo per cui molti calcificatori marini faticano con l’acidificazione degli oceani: gli stessi canali che un tempo rendevano la biomineralizzazione economica e robusta possono diventare un punto debole in un mare in rapido cambiamento.
Citazione: Jonusaite, S., Przibylla-Diop, C., Musinszki, M. et al. Proton channels govern vesicular carbonate chemistry in mineralizing cells of a marine calcifier. Nat Commun 17, 2578 (2026). https://doi.org/10.1038/s41467-026-70837-x
Parole chiave: biominiralizzazione, larve di riccio di mare, canali per protoni, acidificazione degli oceani, carbonato di calcio