Clear Sky Science · it
Recettori meccanici sintetici a base di aptamer consentono il rilevamento della forza specifico per cellula e il controllo temporale tramite circuiti di DNA
Ascoltare le cellule attraverso lievi trazioni
I nostri corpi sono pieni di cellule che spingono e tirano continuamente sull’ambiente circostante, usando forze piccolissime per decidere quando crescere, muoversi o differenziarsi. Questo studio descrive un nuovo modo per origliare tali forze con dispositivi a base di DNA che possono essere tarati su tipi cellulari specifici e attivati o disattivati nel tempo. Una tecnologia del genere potrebbe un giorno aiutare gli ingegneri a guidare la crescita dei tessuti, comprendere il comportamento dei tumori o progettare materiali intelligenti che reagiscono alle cellule viventi in tempo reale.
Usare il DNA come un piccolo interruttore meccanico
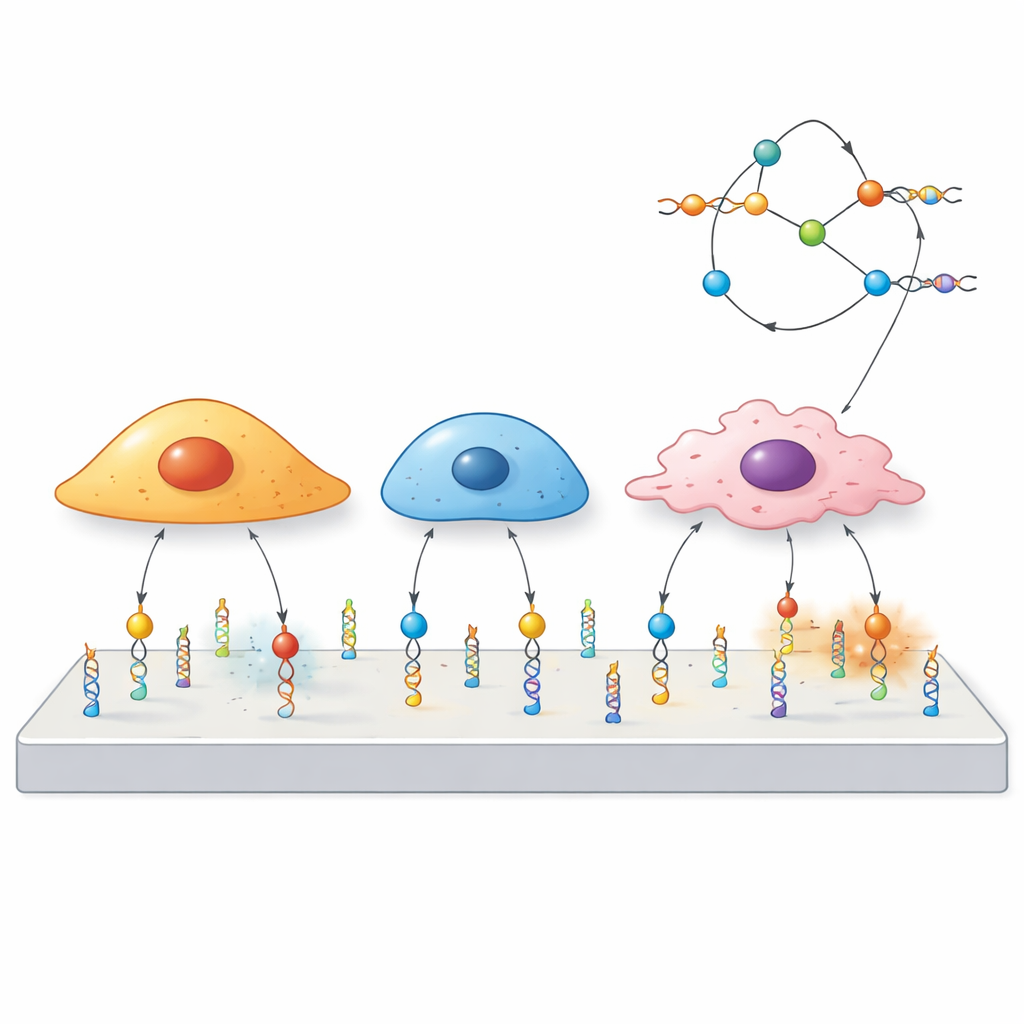
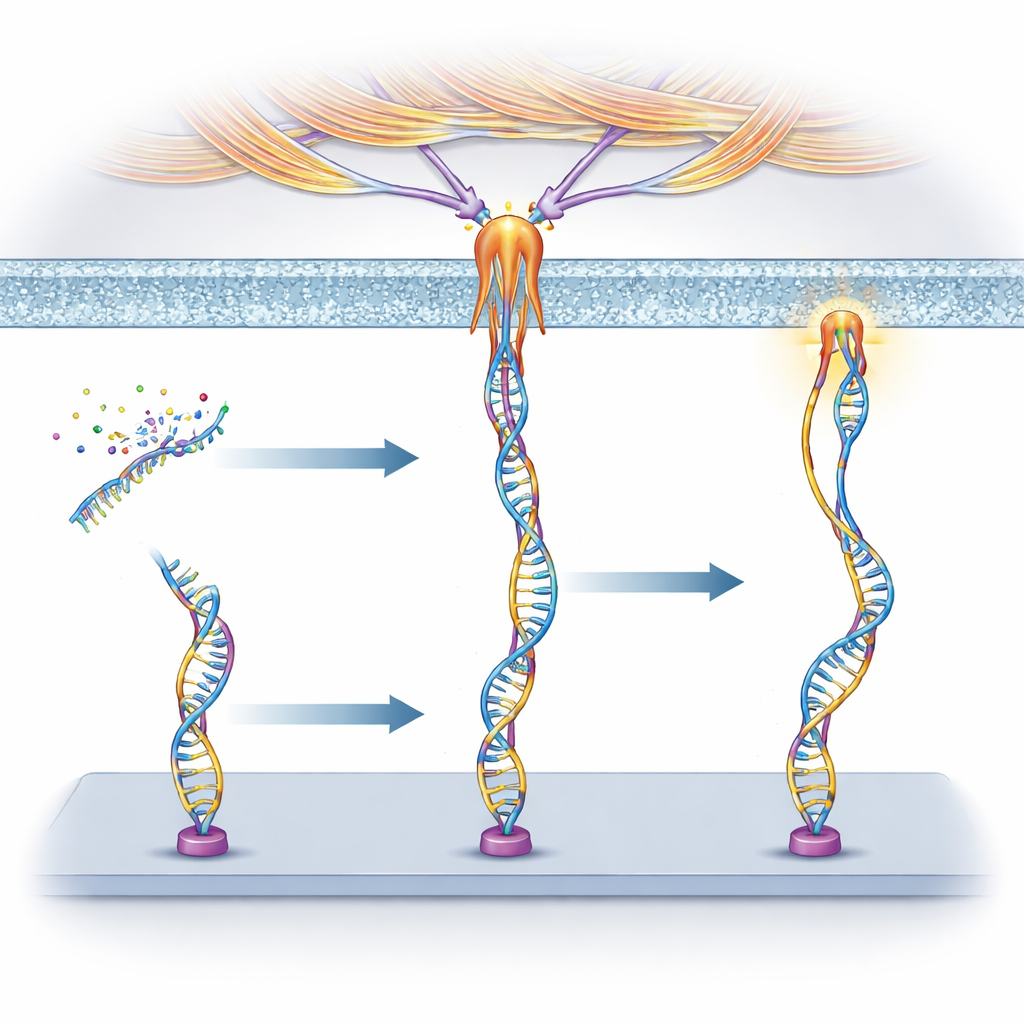
I ricercatori hanno costruito “meccanoprobe” di DNA, la stessa molecola che porta l’informazione genetica. Ogni sonda ha tre componenti: una breve sequenza di DNA detta aptamer che si lega a una proteina scelta sulla superficie cellulare, un segmento a doppio filamento che funge da molla tarata per rompersi a una certa forza, e una molecola fluorescente che si illumina quando quella molla si apre. Quando una cellula tira sul recettore legato dall’aptamer con forza sufficiente, il duplex di DNA si apre e il segnale si attiva. Poiché diversi aptamer si agganciano a recettori diversi, il gruppo può decidere in anticipo quali cellule o proteine potranno attivare la sonda.
Scoprire vie di forza nascoste sulla superficie cellulare
La maggior parte dei sensori di forza esistenti si concentra sugli integrine, proteine ben note che aiutano le cellule ad aggrapparsi all’ambiente ma presenti in molti tipi cellulari, il che limita la selettività. Qui, il team ha invece mirato a recettori “non canonici” che di solito non sono considerati meccanici. Hanno mostrato che un aptamer chiamato AS1411, che si lega a una proteina chiamata nucleolina comune nelle cellule tumorali, produce segnale solo quando riconosce specificamente il suo bersaglio. Progettando sonde che richiedevano forze più deboli o più forti per aprirsi, hanno scoperto che la nucleolina trasmette forze modeste rispetto agli integrine e di per sé non favorisce la diffusione cellulare su una superficie. Al contrario, un altro aptamer, Sgc8, che riconosce il recettore PTK7, riusciva a segnalare forze anche quando le cellule aderivano minimamente, formando pattern ad anello che suggerivano una diversa origine del movimento.
Tracciare l’origine delle forze
Per capire cosa tirasse su questi dispositivi di DNA, i ricercatori hanno usato farmaci che bloccano selettivamente diversi processi cellulari. Per la nucleolina, hanno trovato che le sue forze dipendevano fortemente dalla miosina, la stessa proteina motrice che favorisce la contrazione muscolare, e comparivano nei siti in cui la cellula forma adesioni focali—punti di contatto speciali usati per aggrapparsi e percepire la rigidità. Ciò suggerisce che la nucleolina sia collegata in modo indiretto al macchinario interno actina–miosina della cellula e possa condividere le sue forze contrattili. Per PTK7, invece, il blocco di un processo chiamato macropinocitosi—dove le cellule smuovono la membrana e inghiottono fluido—riduceva fortemente i segnali. Le forze derivavano principalmente dalle prime fasi di smusso della membrana guidate dalla crescita dell’actina, non dai passaggi successivi di sigillatura delle vescicole, rivelando una via meccanica distinta.
Regolare la selettività cellulare con precisione molecolare
Poiché ogni aptamer riconosce un recettore di superficie particolare, lo stesso impalcato di DNA può essere riprogrammato semplicemente sostituendo un aptamer con un altro. Il team ha dimostrato questo con sonde per tre bersagli diversi—PTK7, mucin-1 e EpCAM—su un pannello di linee cellulari tumorali con livelli alti o bassi di ciascuna proteina. Le cellule ricche di un dato recettore producevano segnali forti, mentre quelle con poco recettore rispondevano a malapena, anche quando mescolate nello stesso piatto. Sorprendentemente, cellule che condividevano lo stesso recettore potevano comunque mostrare diversi schemi spaziali di forza, sottolineando che il flusso di forza attraverso un recettore dipende non solo dalla sua presenza ma anche dall’organizzazione interna di ciascun tipo cellulare.
Programmare quando le cellule possono tirare
Sfruttando il fatto che gli aptamer sono fatti di DNA, i ricercatori hanno collegato le loro sonde a reti di reazione del DNA che controllano se l’aptamer può legarsi o meno. Fili complementari “bloccanti” possono temporaneamente nascondere l’aptamer, e fili “attivatori” possono poi rimuovere i bloccanti tramite una reazione di scambio di filamenti, ripristinando la sensibilità alla forza. Hanno anche progettato un bloccante a base di RNA che può essere tagliato da un enzima chiamato RNase H, rallentando ulteriormente questo taglio con molecole esca che competono per l’enzima. In questo modo hanno trasformato il meccanosensing in un programma temporizzato: le cellule potevano generare segnali solo dopo un ritardo incorporato o entro finestre temporali scelte.
Perché questo è importante per i materiali viventi futuri
In termini concreti, questo lavoro trasforma il DNA in una serratura meccanica intelligente che si apre solo per certe cellule, solo sotto certe forze e solo in momenti scelti. Rivelando che recettori meno ovvi come nucleolina e PTK7 possono veicolare informazioni meccaniche tramite vie molto diverse all’interno delle cellule, amplia la nostra visione di come le cellule “sentono” il loro ambiente. Poiché l’intero sistema è costruito con acidi nucleici, può integrarsi direttamente nella cassetta degli attrezzi in rapida crescita dei circuiti e dei nanodispositivi di DNA. Questo crea una base per materiali e tessuti ingegnerizzati che non solo rilevano quando le cellule premono o tirano, ma rispondono anche con azioni biochimiche temporizzate, potenzialmente guidando la guarigione, la crescita o il trattamento del cancro in modo altamente programmabile.
Citazione: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
Parole chiave: meccanotrasduzione, aptamer di DNA, meccanica cellulare, biologia sintetica, reti di reazione del DNA