Clear Sky Science · it
Frazzled/DCC dirige l’integrazione spaziale dei progenitori assicurando il ricambio intestinale in stato stazionario
Come l’intestino si rinnova silenziosamente
Ogni giorno le cellule che rivestono l’intestino si consumano e devono essere sostituite, eppure l’organo mantiene forma e dimensioni con sorprendente precisione. Questo studio, che utilizza la mosca della frutta come modello, svela un sistema di guida nascosto che indica alle cellule neo‑formate dell’intestino esattamente dove andare per colmare minuscoli vuoti nel rivestimento. Capire questo “controllo del traffico cellulare” non solo chiarisce come gli organi sani si mantengono, ma fa anche luce su come segnali di guida simili possano essere dirottati durante la diffusione del cancro.
Un alveare in movimento costante
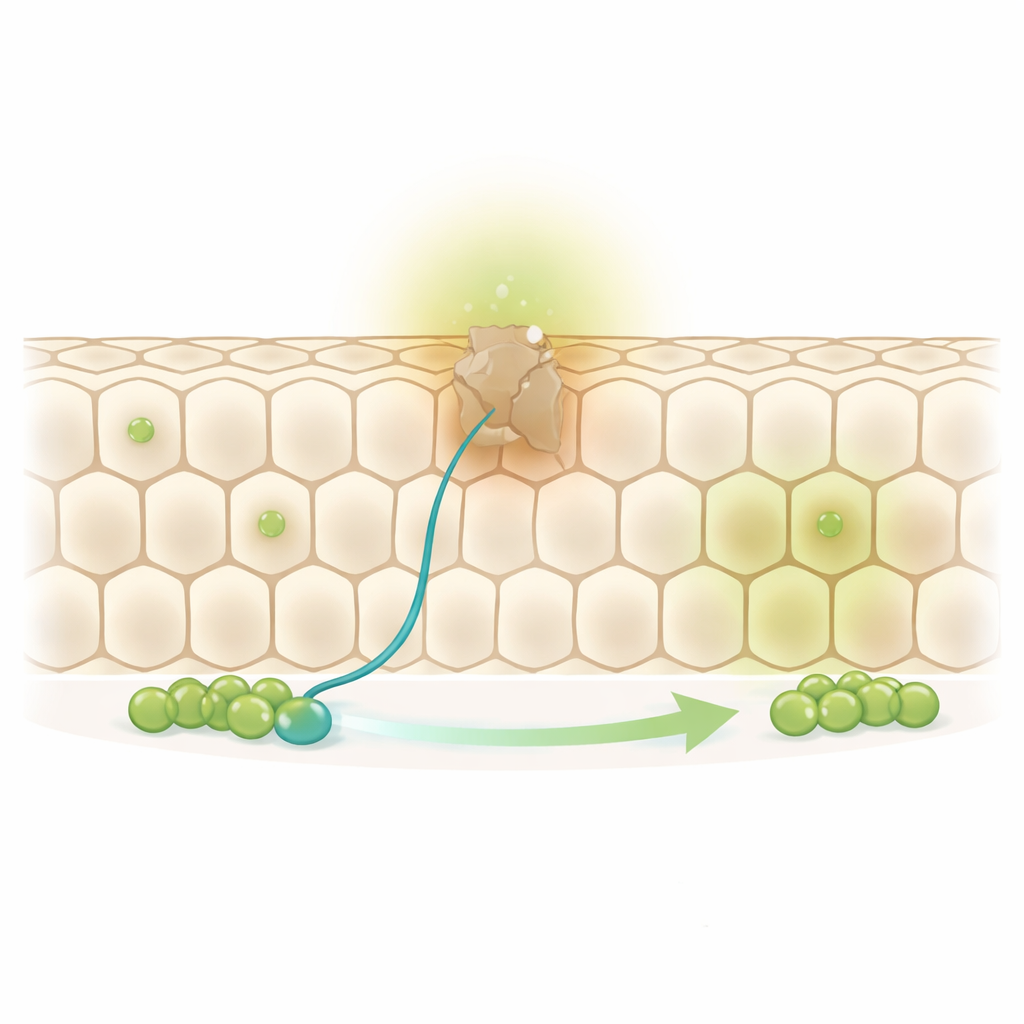
Il midgut della mosca è coperto da un singolo strato di grandi cellule assorbenti disposte come un alveare. Alla base di questo foglio si trovano cellule staminali sparse e le loro figlie immediate, chiamate progenitrici. Quando una cellula assorbente invecchia e arriva al termine della sua vita, una cellula staminale si divide e la sua figlia progenitrice alla fine sostituisce la vicina usurata. Tuttavia, gli autori hanno notato che circa un terzo delle cellule in questo alveare non ha una cellula staminale o una progenitrice direttamente accanto. Questo pone un enigma: come vengono rinnovate queste cellule “fuori portata” senza lasciare buchi nella barriera?
Nuove cellule in movimento
Tracciando eventi di rimpiazzo individuali per una settimana, i ricercatori hanno rilevato che queste cellule remote vengono rinnovate con la stessa frequenza di quelle adiacenti a una staminale. Ciò implica che le progenitrici devono spostarsi. Infatti, il gruppo ha osservato che le progenitrici estendono lunghe e sottili protrusioni—sensori cellulari—più lunghe e più frequentemente rispetto alle stesse cellule staminali. Queste protrusioni non sono casuali: in condizioni normali si orientano principalmente verso i vicini più vecchi e non ancora rimpiazzati piuttosto che verso quelli appena rinnovati, suggerendo un comportamento attivo di ricerca e soccorso rivolto alle cellule che più necessitano di sostituzione.
Un segnale di guida neuronale riadattato per l’intestino
Per capire come vengono dirette queste protrusioni, gli autori si sono rivolti a una famiglia di molecole nota soprattutto per l’orientamento dei circuiti cerebrali: le Netrine e i loro recettori Frazzled/DCC e Unc-5. Nel sistema nervoso, le Netrine agiscono come fari a lunga distanza che attraggono o respingono le fibre nervose in crescita. Nell’intestino della mosca, il gruppo ha mostrato che i recettori Frazzled/DCC e Unc-5 si trovano specificamente sulle cellule progenitrici, concentrati nelle loro protrusioni. Le cellule assorbenti usurate, a loro volta, cominciano a produrre e rilasciare una Netrina chiamata Netrin‑B. Quando i ricercatori hanno aumentato Netrin‑B in cellule selezionate, le progenitrici vicine hanno allungato protrusioni orientate verso la sorgente, quindi sono migrate per occupare quel punto. Quando hanno bloccato Netrin‑B o disattivato Frazzled, le protrusioni si sono accorciate, le cellule remote non sono state più rimpiazzate in modo efficiente e le mosche sono morte prima, sottolineando quanto sia vitale questa guida per la salute intestinale.
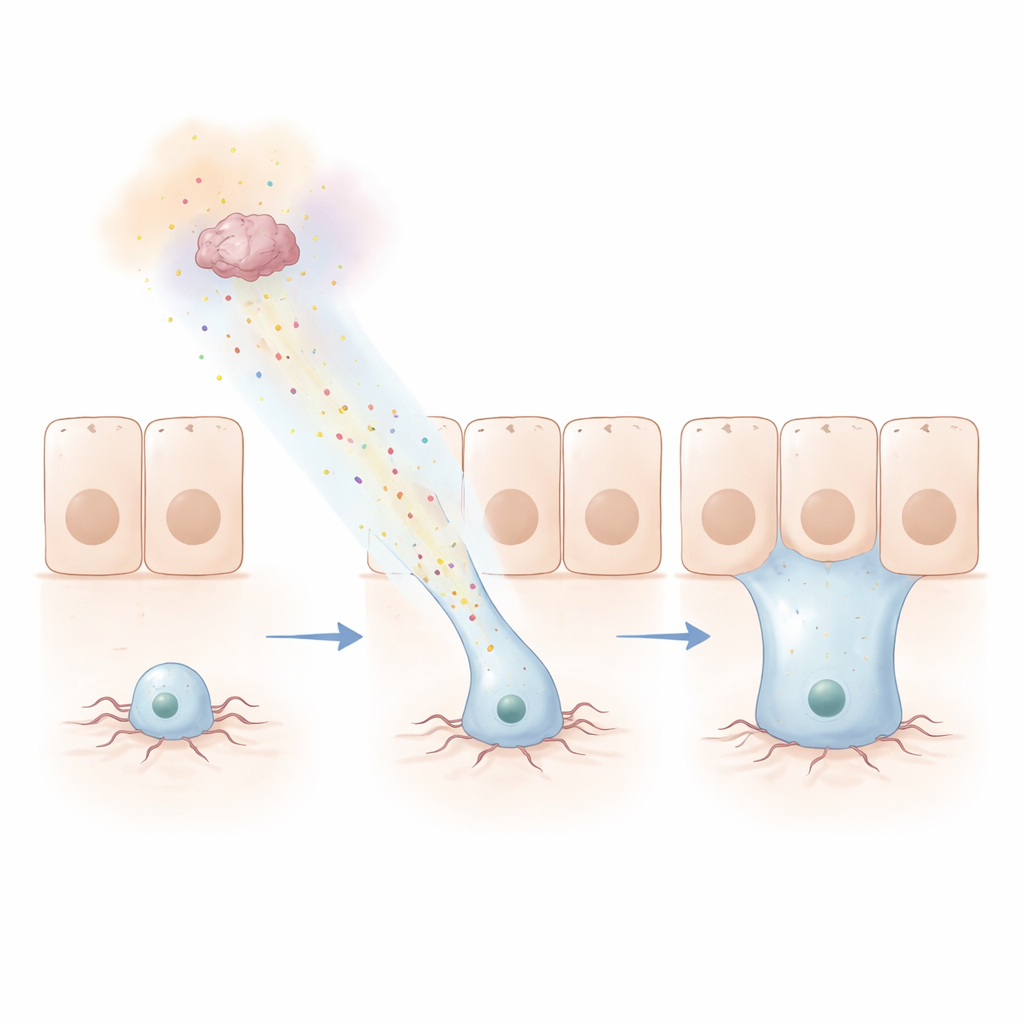
Seguire una traccia chimica
Per sondare quanto lontano possa arrivare questo segnale, il team ha messo a punto un ingegnoso saggio “Hamelin”, ispirato al Pifferaio Magico. Hanno fatto in modo che un anello di cellule al giunto tra regioni intestinali secernesse Netrine, marcando fluorescentemente le progenitrici a distanza. Nel corso di giorni, le progenitrici hanno migrato fino a decine di micrometri verso la sorgente, attraversando persino un confine netto in uno strato tissutale diverso e integrandosi lì. Versioni umane delle Netrine e del recettore DCC possono sostituire i corrispettivi della mosca e continuare a guidare questi movimenti, mostrando che il meccanismo è profondamente conservato. Anche la stessa macchina actinica che alimenta il movimento cellulare altrove nel corpo era necessaria: quando componenti chiave venivano rimossi, protrusioni e rinnovo a lungo raggio fallivano.
Perché questo è importante per salute e malattia
In termini semplici, questo lavoro rivela che l’intestino non si affida solo alla pressione locale di divisione cellulare per rinnovare il suo rivestimento. Invece, le cellule morenti inviano un segnale chimico di «aiuto», Netrin‑B, che attira progenitrici specifiche dotate dei recettori Frazzled/DCC. Queste progenitrici estendono sensori lungo il gradiente, strisciano verso la cellula invecchiata e si incastrano al loro posto per mantenere la barriera intatta. Poiché lo stesso sistema Netrin–DCC è attivo nei mammiferi ed è stato collegato all’invasione e alla metastasi tumorale, i risultati nella mosca forniscono un sostegno meccanicistico concreto all’idea che queste molecole siano a doppio taglio: essenziali per la riparazione ordinata nei tessuti sani, ma potenzialmente pericolose se malregolate nei tumori che imparano a muoversi e colonizzare nuovi organi.
Citazione: Zipper, L., Ramon-Cañellas, P., Akkas-Gazzoni, F. et al. Frazzled/DCC directs spatial progenitor integration ensuring steady-state intestinal turnover. Nat Commun 17, 2491 (2026). https://doi.org/10.1038/s41467-026-70704-9
Parole chiave: cellule staminali intestinali, migrazione cellulare, segnalazione netrina, omeostasi tissutale, metastasi del cancro