Clear Sky Science · it
Un attuatore mio-neurale con biofisica ingegnerizzata per sistemi bio-ibridi impiantabili
Ricostruire i muscoli come macchine viventi intelligenti
Immaginate se i medici potessero trasformare il muscolo di una persona in un motore vivente che non si stanca mai, pilotabile da un computer e in grado di stare in sicurezza vicino ad organi delicati per anni. Questo studio descrive un modo per farlo. I ricercatori progettano un “attuatore mio-neurale” nei ratti: un muscolo la cui innervazione viene deliberatamente riorganizzata in modo da poter essere guidato dall’elettronica, resistere alla fatica e mantenere comunque caratteristiche di tessuto naturale. Tali attuatori viventi potrebbero un giorno ripristinare il movimento, supportare organi in insufficienza o fornire sensazioni realistiche da protesi avanzate.
Perché i muscoli viventi sono motori migliori
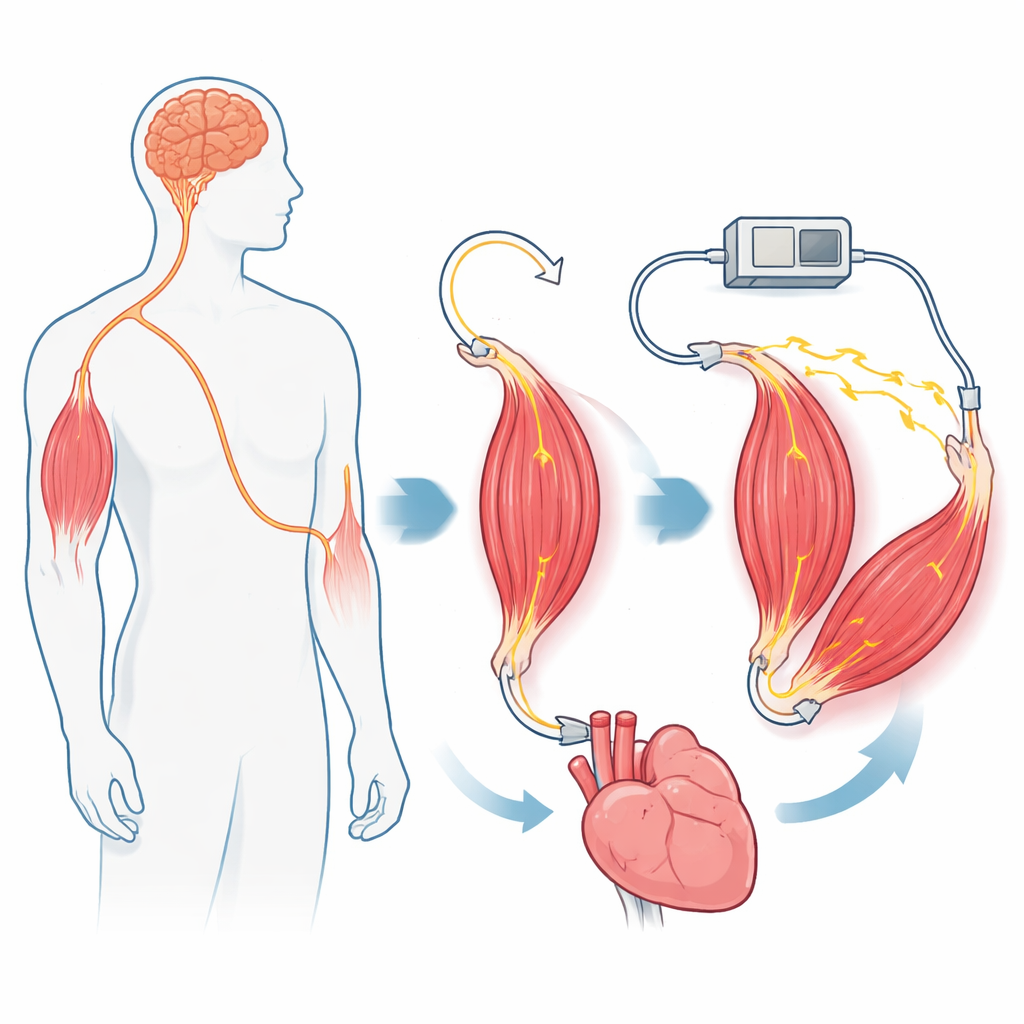
I motori artificiali che funzionano con elettricità, aria o fluidi sono potenti, ma sono pesanti, difficili da ridurre a dimensioni compatibili con il corpo e realizzati con materiali che non si integrano bene con i tessuti viventi. In confronto, il muscolo scheletrico è leggero, efficiente dal punto di vista energetico, in grado di autoripararsi e già progettato per funzionare all’interno del corpo. Può crescere, adattarsi e rispondere a segnali nervosi minimi. Tuttavia, quando i muscoli sono controllati direttamente da impulsi elettrici di un dispositivo impiantato, si affaticano rapidamente. Questa fatica si verifica perché la stimolazione elettrica standard tende a reclutare per prime le fibre più grandi e veloci ma meno resistenti. Per sfruttare il muscolo come un motore impiantabile e affidabile, il team ha dovuto modificare l’organizzazione e il reclutamento delle sue fibre nervose—senza compromettere la salute e la sostenibilità naturale del muscolo.
Scambiare i percorsi nervosi per riscrivere il controllo
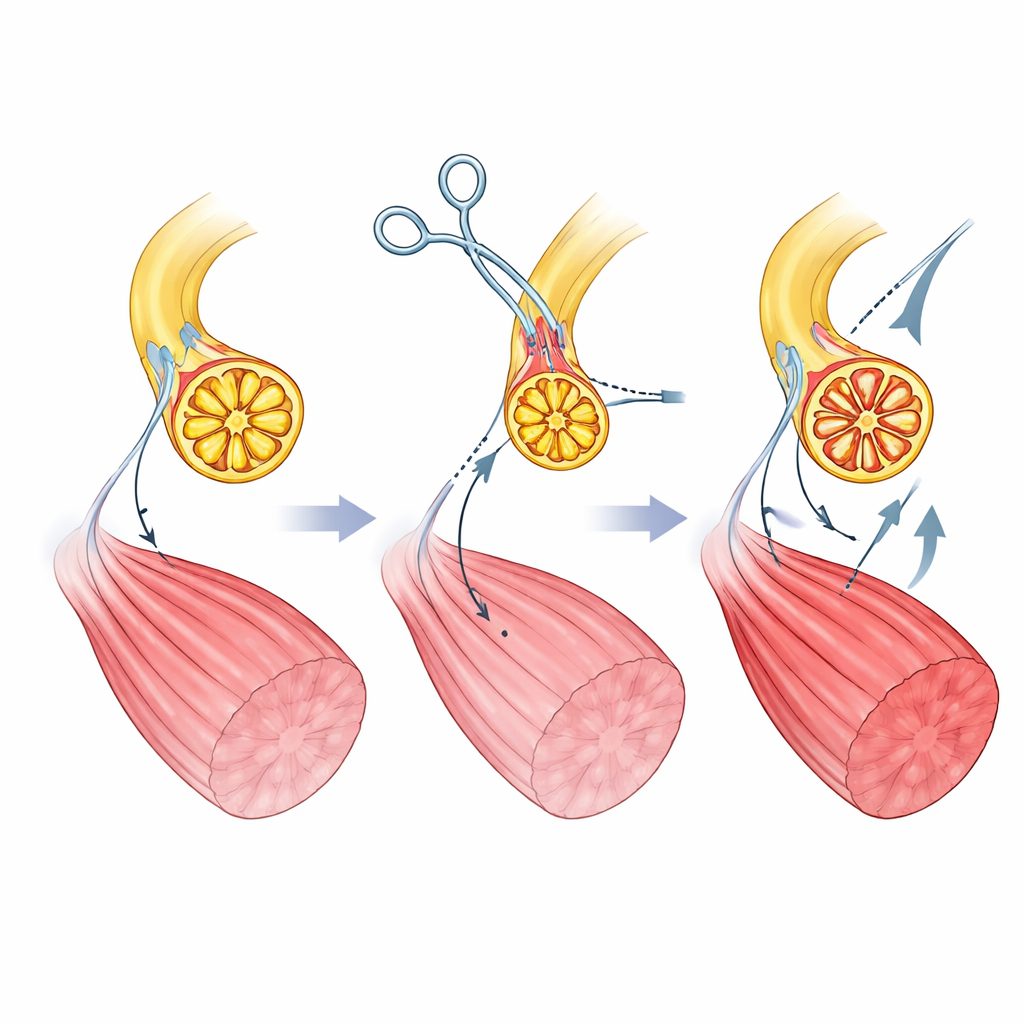
Gli autori creano il loro attuatore mio-neurale nei ratti ricollegando chirurgicamente un muscolo della gamba. Prima recidono il nervo motore normale che porta i comandi dal midollo spinale e ne impediscono la rigenerazione. Poi instradano un nervo diverso—quello che normalmente trasmette segnali di tatto e stiramento dalla pelle e dai tessuti—direttamente nel muscolo. Col tempo, questo nervo “sensitivo” rigenera all’interno del muscolo e forma nuovi punti di contatto con le fibre muscolari. La microscopia mostra che queste nuove giunzioni somigliano e si comportano come connessioni motorie normali, e il muscolo riacquista la capacità di contrarsi quando il nervo sensitivo è stimolato elettricamente. È importante che gli assoni di questo nervo sensitivo siano più uniformi e di dimensioni inferiori rispetto a quelli del nervo motore originale, creando le condizioni per un reclutamento delle fibre muscolari più equilibrato sotto controllo computazionale.
Muscoli che continuano a funzionare sotto stress
Una volta che i muscoli ricollegati si erano rimessi, il team li ha sottoposti a prove impegnative. Hanno confrontato i muscoli nativi con i nuovi attuatori durante singole contrazioni ripetute e durante lunghi periodi di contrazione continua. Gli attuatori mio-neurali hanno perso forza molto più lentamente e hanno mostrato un’uscita più stabile nel tempo, con un miglioramento del 260% nella resistenza alla fatica sotto lavoro continuo. Il loro comportamento su scale di minuti era fondamentalmente diverso dal muscolo non modificato: invece di un rapido calo della forza, lo sforzo diminuiva più gradualmente per poi stabilizzarsi. Nonostante avessero perso parte della massa durante il ricollegamento, gli attuatori hanno conservato una struttura fibrosa sana e hanno prodotto una forza per unità di massa simile a quella del muscolo nativo, mantenendo le condizioni per almeno 15 settimane anche senza esercizio o stimolazione aggiuntiva.
Controllo computerizzato senza disturbare il cervello
Poiché la nuova innervazione disconnette il muscolo dai segnali motori normali del cervello, tutte le contrazioni ora provengono da uno stimolatore esterno. I ricercatori integrano il muscolo in un loop di retroazione: un sensore misura la forza, un controllore regola la stimolazione del nervo e il sistema cerca di seguire un valore di forza obiettivo per molti cicli. I muscoli nativi falliscono rapidamente in questo schema, ma gli attuatori mio-neurali continuano a seguire i segnali di comando. Per rendere il sistema più sicuro e flessibile, il team introduce anche un “blocco nervoso” reversibile. Applicando un segnale elettrico ad alta frequenza sul nervo più vicino al midollo spinale, impediscono che gli impulsi di stimolazione inviino segnali indesiderati al sistema nervoso centrale pur consentendo alla parte muscolare di rispondere. Nei test, l’attuatore ha continuato a generare forze controllate mentre il cervello rimaneva praticamente isolato dalla stimolazione artificiale.
Da arti bionici ad aiutare organi in insufficienza
Per mostrare come questo motore vivente potrebbe essere impiegato, gli autori costruiscono due sistemi dimostrativi nei ratti. Nel primo, accoppiano l’attuatore in serie con un altro muscolo che funge da residuo muscolare in un sito di amputazione. Stringendo o rilassando questa coppia, modificano l’allungamento del muscolo residuo e, a sua volta, l’attività delle sue fibre nervose sensoriali—regolando in pratica la percezione di posizione e forza dell’arto. Questa “interfaccia mecanoneurale propriocettiva” potrebbe in futuro fornire un feedback dal senso naturale per arti robotici o avatar virtuali. Nel secondo sistema, avvolgono l’attuatore attorno a un tratto di piccolo intestino riempito di fluido. Se stimolato, il muscolo comprime e rilascia il segmento intestinale e il tracciamento del movimento mostra che l’organo si muove in sincronia con l’attuatore. Questo suggerisce dispositivi futuri in grado di fornire forza meccanica ad organi indeboliti come intestino, vescica o perfino cuore.
Cosa potrebbe significare per la medicina futura
Nel complesso, questo lavoro dimostra che, rimodulando con cura i percorsi nervosi, il muscolo di una persona può essere trasformato in un attuatore resistente alla fatica, pilotato da computer, che conserva il comportamento del tessuto nativo e può essere elettricamente isolato dal cervello quando necessario. Poiché l’approccio si basa su tecniche chirurgiche ed elettrodi che ricordano già gli strumenti clinici esistenti, potrebbe essere più facile da tradurre rispetto a impianti completamente sintetici o tessuti coltivati in laboratorio. Se attuatori mio-neurali simili potranno essere costruiti e controllati in sicurezza negli esseri umani, potrebbero costituire il nucleo di nuovi sistemi bio-ibridi che ripristinano la sensibilità degli arti, assistono organi in insufficienza e forniscono segnali meccanici precisi al corpo senza l’ingombro e la rigidità delle macchine tradizionali.
Citazione: Song, H., Herrera-Arcos, G., Friedman, G.N. et al. A myoneural actuator with engineered biophysics for implantable biohybrid systems. Nat Commun 17, 2584 (2026). https://doi.org/10.1038/s41467-026-70626-6
Parole chiave: attuatore bio-ibrido, neuroprotesi, affaticamento muscolare, rigenerazione nervosa, supporto d’organo