Clear Sky Science · it
Transizioni strutturali nell’assemblaggio graduale delle particelle core del proteasoma
Come le cellule smaltiscono i rifiuti molecolari
All’interno di ciascuna delle nostre cellule, le proteine consumate o danneggiate devono essere demolite prima che si accumulino come spazzatura. Una gigantesca macchina molecolare chiamata proteasoma svolge gran parte di questo lavoro di pulizia ed è già un bersaglio per farmaci antitumorali. Questo studio dà uno sguardo dietro le quinte su come il nucleo catalitico del proteasoma viene costruito passo dopo passo nelle cellule di lievito, rivelando scorciatoie inaspettate e meccanismi di sicurezza che aiutano a garantire che la macchina finale funzioni con precisione e solo quando è pronta.
Costruire un barile trituratore di proteine
La parte attiva del proteasoma è un nucleo a forma di barile formato da anelli impilati di subunità proteiche. Questo barile ospita i siti di taglio nascosti che frammentano le altre proteine in pezzi piccoli. Poiché attivare questi tagliatori troppo presto sarebbe pericoloso, le cellule assemblano il barile attraverso una serie di intermedi parziali. Gli autori si sono concentrati sulle prime versioni del nucleo, note come complessi precursori, che sono solitamente rare e fugaci. Rallentando leggermente uno degli ultimi passaggi dell’assemblaggio, sono riusciti a catturare e purificare queste forme iniziali dal lievito e a immaginarle mediante crio-microscopia elettronica ad alta risoluzione, che congela le molecole in azione e rivela le loro forme tridimensionali.
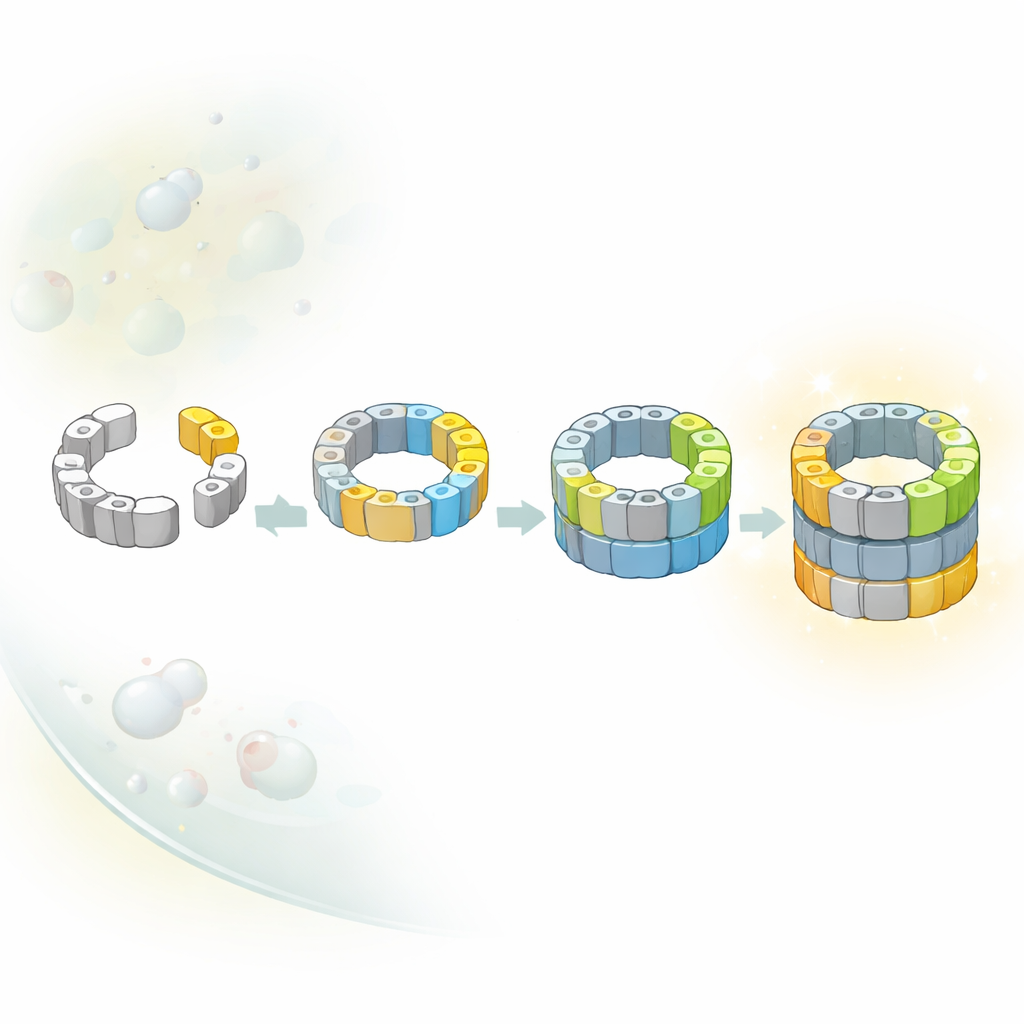
Più strade per lo stesso nucleo
I diagrammi classici da manuale spesso suggeriscono che le macchine complesse all’interno delle cellule si costruiscano lungo un’unica via fissa. Qui, i ricercatori hanno scoperto che non è così per il nucleo del proteasoma. Hanno identificato diversi intermedi distinti che differiscono per quali subunità catalitiche si sono unite al barile a metà costruzione. Combinando istantanee strutturali con astuzie genetiche che accendono o spengono singole subunità, hanno dimostrato che almeno due percorsi alternativi portano da un primo mezzo-barile a uno quasi completo. In un percorso, una subunità particolare chiamata β5 arriva per prima; in un altro, una diversa subunità, β1, può unirsi prima. L’equilibrio tra queste vie dipende probabilmente da quali mattoni di costruzione sono più disponibili nell’affollato ambiente cellulare.
Da pezzi sciolti a una camera di taglio bloccata
Le strutture rivelano anche come i siti di taglio del proteasoma vengano accuratamente predisposti durante l’assemblaggio. Negli intermedi precoci, regioni ad anello chiave che circondano i residui di taglio sepolti sono flessibili e poco ordinate, e i centri catalitici sono ancora ostruiti da brevi segmenti «propeptide». Man mano che ulteriori subunità si incastrano attorno all’anello, questi anelli assumono gradualmente forme più definite che allineano gli amminoacidi cruciali necessari per l’autoattivazione. Solo quando due mezzo-barili si uniscono infine, completando il barile a doppio anello, questi anelli si bloccano completamente nella loro disposizione attiva e scatenano la rimozione dei segmenti bloccanti. Questo accoppiamento di geometria e chimica contribuisce a garantire che l’attività di taglio potente compaia solo all’interno di una camera sigillata, proteggendo il resto della cellula.
I chaperoni guidano e poi si ritirano
Durante il processo, proteine helper specializzate chiamate chaperoni accompagnano il barile in formazione e prevengono combinazioni errate. Un chaperone, Ump1, inizia ampiamente non strutturato ma si ripiega progressivamente man mano che più subunità lo circondano, venendo infine intrappolato nella cavità centrale e poi distrutto una volta che il barile è attivo. Un’altra coppia di chaperoni, Pba1–Pba2, afferra la superficie dell’anello esterno in due modi ingegnosi. Un anello flessibile di Pba1 si infila tra due subunità dell’anello esterno come un distanziatore, tenendole leggermente separate e impedendo la chiusura prematura. Allo stesso tempo, l’estremità a coda di una subunità dell’anello esterno (α1) aiuta a posizionare i segmenti vicini in modo che, nella fase finale, i chaperoni possano essere rilasciati e l’anello possa chiudersi correttamente. Quando i ricercatori hanno cancellato la coda di α1, il barile si è bloccato in uno stato tardivo, quasi completo, che ha mantenuto ostinatamente i suoi chaperoni, confermando che questa piccola regione agisce come parte di un interruttore di rilascio.
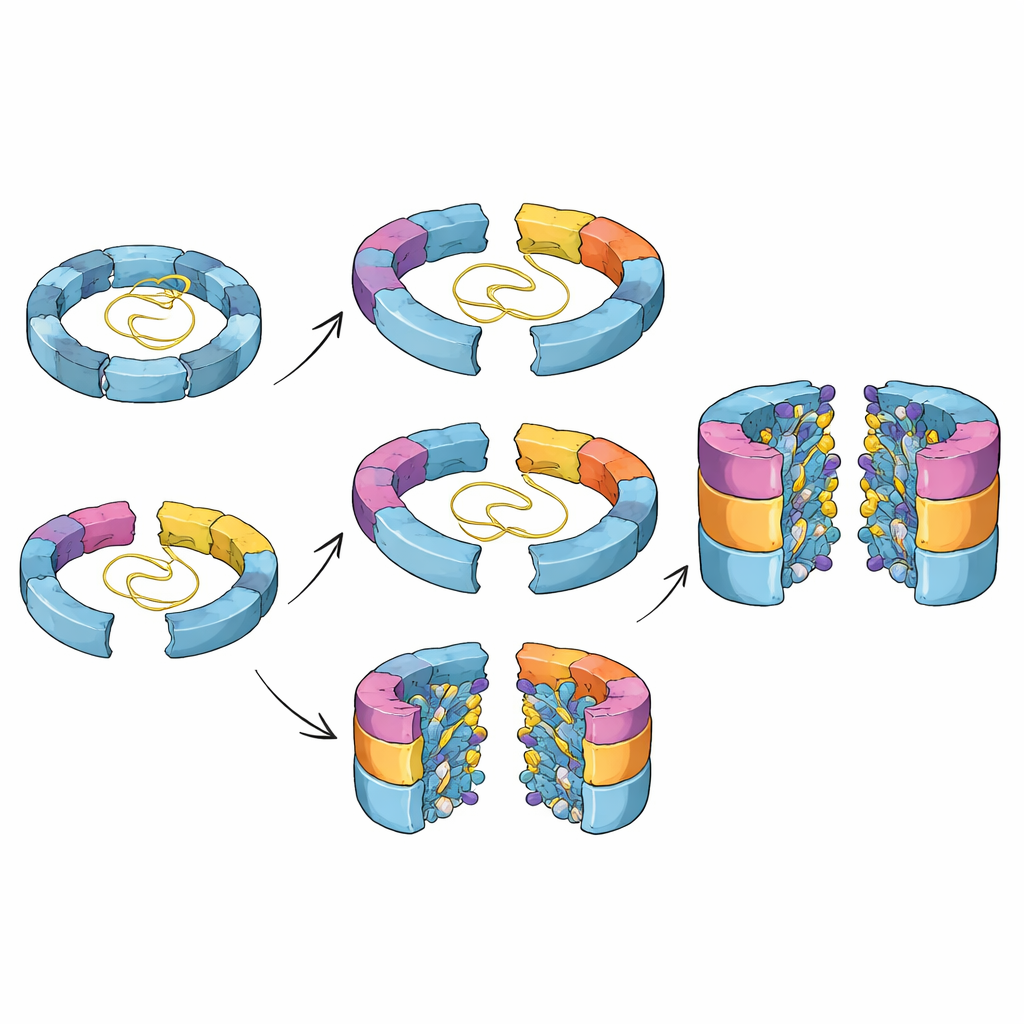
Perché questi passaggi nascosti sono importanti
Nel loro insieme, questi risultati dipingono un quadro dettagliato di come le cellule coreografano l’assemblaggio di un trituratore di proteine pericoloso ma essenziale. Il lavoro mostra che il nucleo del proteasoma può essere costruito tramite più di una via, che i suoi siti attivi vengono gradualmente scolpiti in posizione e che le proteine helper non solo stabilizzano gli intermedi precoci ma sono anche integrate in un circuito temporale che assicura la loro partenza al momento giusto. Comprendere questi passaggi nascosti aiuta a spiegare come piccole variazioni genetiche nei fattori di assemblaggio possano contribuire a malattie e potrebbe favorire la progettazione di farmaci che modulano finemente l’attività del proteasoma nel cancro, nei disturbi immunitari o nella neurodegenerazione colpendo la sua costruzione piuttosto che la sua forma finale.
Citazione: Mark, E., Ramos, P.C., Nunes, M.M. et al. Structural transitions in the stepwise assembly of proteasome core particles. Nat Commun 17, 2582 (2026). https://doi.org/10.1038/s41467-026-70525-w
Parole chiave: assemblaggio del proteasoma, degradazione delle proteine, chaperoni molecolari, crio microscopia elettronica, controllo qualità cellulare