Clear Sky Science · it
Chimerismo molecolare transiente per sfruttare organelli xenogenici
Pannelli solari presi in prestito in una singola cellula
Di solito pensiamo alla vita alimentata dal sole in termini di piante e alghe, ma alcuni predatori unicellulari seguono una scorciatoia: rubano i “pannelli solari” — i cloroplasti — alle loro prede. Questo studio esplora come un microbo di questo tipo, Rapaza viridis, mantenga queste parti rubate funzionanti per settimane, nonostante provengano da una specie completamente diversa. Scoprendo come le proteine dell’ospite entrino e supportino questi cloroplasti estranei, il lavoro getta luce su come componenti cellulari complessi come i cloroplasti possano essersi evoluti in epoche remote.
Come un microbo ruba e usa l’energia verde
Rapaza viridis è un piccolo flagellato che mangia una specifica alga verde chiamata Tetraselmis. Invece di digerire tutto, Rapaza conserva i cloroplasti catturati, ora chiamati “cleptoplasti”, e scarta il resto della cellula algale, incluso il suo nucleo. Questi cleptoplasti vengono tagliati in pezzi e trasmessi alle cellule figlie di Rapaza. Per circa due settimane, l’ospite può vivere quasi interamente dell’energia e del carbonio prodotti da questi cloroplasti presi in prestito, anche se non ricevono più istruzioni o ricambi dal genoma algale originale. Questo stile di vita insolito offre una finestra dal vivo su quali potrebbero essere stati i primi passi verso cloroplasti permanenti.
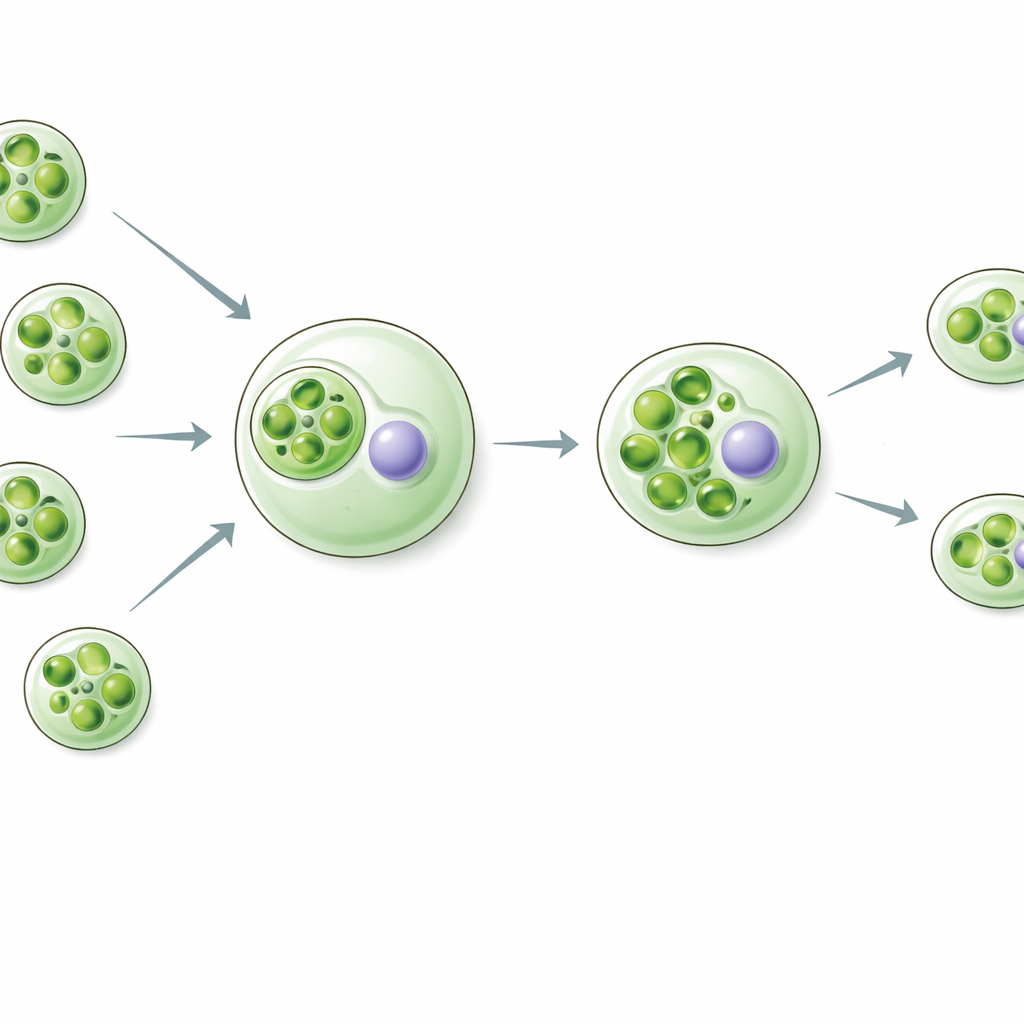
I geni dell’ospite intervengono per mantenere vive le parti rubate
I ricercatori si sono posti una domanda cruciale: se il nucleo dell’alga è assente, chi fornisce le proteine necessarie a far funzionare il cleptoplasto? Analizzando l’attività genica nel tempo in Rapaza, hanno identificato 37 geni dell’ospite i cui prodotti sembrano operare all’interno dei cloroplasti. Molti di questi geni somigliano a componenti della macchina fotosintetica — proteine raccoglitrici di luce, elementi della catena di trasporto elettronico e enzimi che fissano il carbonio. Due si sono distinti: una proteina simile alla piccola subunità della RuBisCO (RvRbcS-like) e una proteina simile alla attivasi della RuBisCO (RvRca-like). Entrambe sono correlate ad aiutanti chiave della RuBisCO, l’enzima centrale che cattura l’anidride carbonica. Questi geni dell’ospite si attivano intensamente dopo che la preda è stata ingerita, proprio quando i cleptoplasti vengono rimodellati e preparati per un uso di lungo periodo.
Dimostrare che le proteine dell’ospite entrano nei cleptoplasti
Trovare sequenze geniche indicative non basta; le proteine devono effettivamente raggiungere l’interno dei cleptoplasti. Usando anticorpi su misura e microscopia a fluorescenza, il team ha seguito dove si accumulano le proteine RvRbcS-like e RvRca-like. Hanno ingegnerizzato ceppi di Rapaza con minuscoli tag rilevabili su RvRbcS-like e hanno mostrato che il segnale si sovrapponeva ai cleptoplasti e alla RuBisCO stessa. Un’imaging simile con un anticorpo contro RvRca-like ha rivelato che anche questa proteina si concentra all’interno dei cleptoplasti. Su gel proteici, entrambe le proteine risultavano accorciate, coerente con la rimozione di un segmento frontale speciale durante il passaggio attraverso membrane — proprio come i segnali di trasporto che guidano le proteine nei cloroplasti ordinari.
Perché questi aiutanti presi in prestito sono importanti
Per verificare se queste proteine dell’ospite siano davvero importanti, gli autori hanno usato l’editing genomico basato su CRISPR per eliminare ciascun gene. Le cellule prive di RvRbcS-like crescevano male, perdevano potenza fotosintetica, producevano molte meno riserve energetiche e morivano molto prima del normale. I livelli della grande subunità della RuBisCO algale sono calati, suggerendo che senza la subunità piccola sostitutiva dell’ospite il complesso enzimatico si sfalda. L’eliminazione di RvRca-like ha avuto un effetto più lieve ma comunque evidente: la crescita iniziale rimaneva vicina al normale, ma in seguito la fotosintesi e l’accumulo di carbonio declinavano, rivelando una perdita graduale di efficienza. Nel loro insieme, questi risultati mostrano che Rapaza non si limita a parcheggiare cloroplasti rubati; li mantiene e li rimodella attivamente con il proprio arsenale proteico.
Tag di consegna su misura e strutture interne ricostruite
La maggior parte delle proteine putativamente destinate ai cleptoplasti in Rapaza condivide lunghe “teste” a bassa struttura all’estremità anteriore, spesso con segmenti predetti che attraversano membrane. Fusi una di queste teste a una proteina reporter luciferasi, gli autori hanno mostrato che questo segmento da solo è sufficiente a trasportare una proteina cargo nei cleptoplasti. L’analisi dettagliata delle sequenze ha rivelato diverse classi di queste regioni di targeting, che somigliano strettamente a quelle usate da un gruppo di alghe correlate per importare proteine nei loro cloroplasti permanenti a tripla membrana. Una proteina dell’ospite particolarmente notevole, RvRbcS-like, porta quattro domini correlati alla RuBisCO e una coda floscia ricca di motivi ripetuti pensati per favorire la separazione di fase delle proteine. Gli autori propongono che questa coda aiuti a riorganizzare il pirenoide — il denso nucleo di fissazione del carbonio all’interno del cleptoplasto — in molteplici gocce che possono essere ereditate dalle cellule figlie.
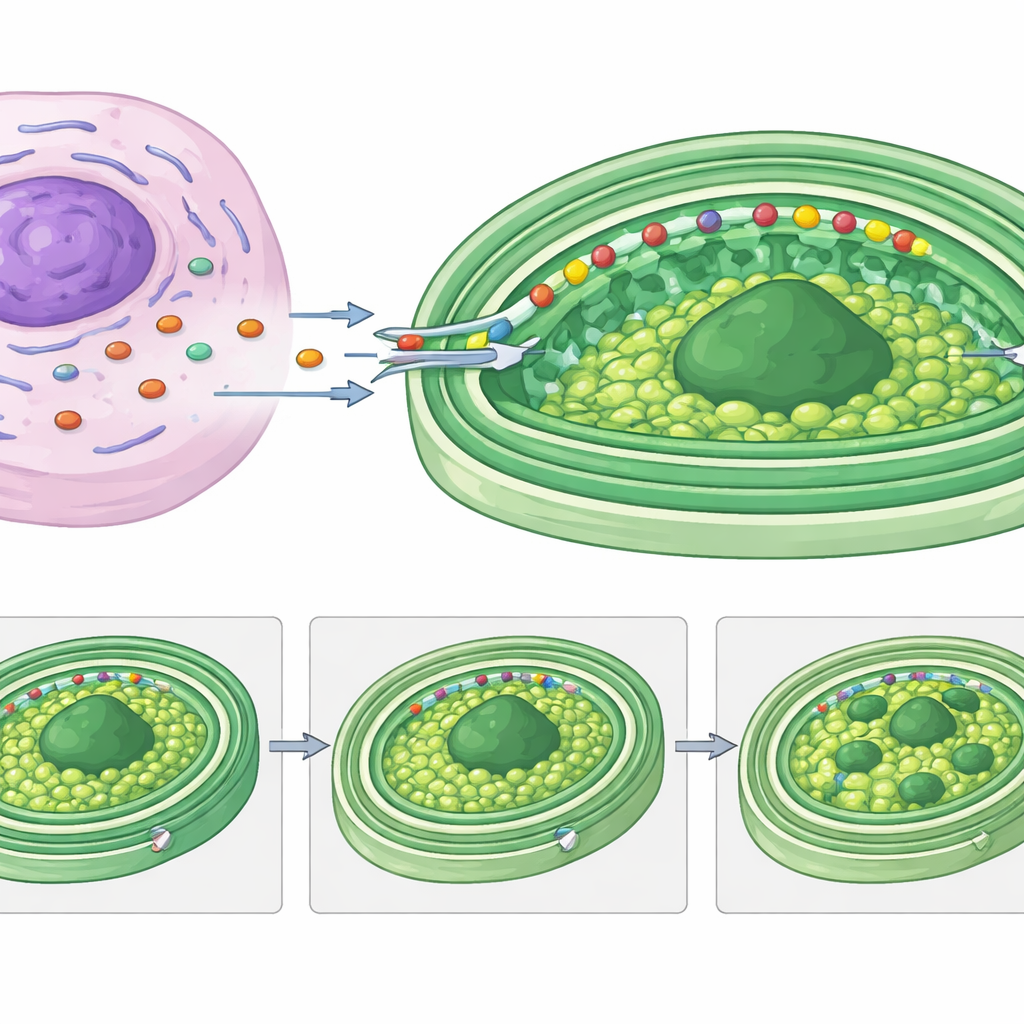
Cosa significa questo per la storia delle cellule complesse
Per un non specialista, il messaggio chiave è che Rapaza viridis mostra una versione vivente e reversibile di ciò che potrebbe essere accaduto quando cellule antiche trasformarono batteri liberi in componenti permanenti come i cloroplasti. Qui, l’ospite costruisce rapidamente una partnership molecolare temporanea: i suoi geni forniscono parti sostitutive cruciali e rimodellano persino la struttura interna dei cloroplasti rubati, il tutto guidato da tag di consegna specializzati. Questo “chimerismo molecolare transiente” dimostra che anche integrazioni di breve durata tra specie possono essere sofisticate e finemente regolate. Studiare questo sistema offre agli scienziati un modello potente per comprendere come le cellule complesse abbiano imparato a controllare, nutrire e usare in sicurezza fabbriche energetiche straniere — e come nuovi organelli possano ancora emergere nel corso dell’evoluzione.
Citazione: Kashiyama, Y., Maruyama, M., Nakazawa, M. et al. Transient molecular chimerism for exploiting xenogeneic organelles. Nat Commun 17, 2371 (2026). https://doi.org/10.1038/s41467-026-70516-x
Parole chiave: cleptoplastia, evoluzione dei cloroplasti, Rapaza viridis, <keyword>biogenesi degli organelli