Clear Sky Science · it
Caratterizzazione senza marcatori di massa e dimensione di biomolecole di poche kDa mediante microscopia a scattering nanofluidico potenziata da transformer visivo gerarchico
Osservare le molecole più piccole
Molti dei messaggeri più importanti dell’organismo — come ormoni e segnali del sistema immunitario — sono così piccoli da risultare praticamente invisibili ai microscopi potenti a meno che non vengano marcati con sonde fluorescenti. Queste etichette possono però alterare il comportamento delle molecole, un limite significativo per lo sviluppo di farmaci e per la biologia di base. Questo studio presenta un metodo per pesare e misurare singole molecole grandi quanto l’insulina senza alcun marcatore, impiegando una combinazione di chip nanofluidici e intelligenza artificiale avanzata. Si apre così la possibilità di osservare i principali biomolecola nel loro stato naturale, una per una.
Canali minuscoli come provette
Al centro del metodo c’è la microscopia a scattering nanofluidico, che utilizza un chip delle dimensioni di un’unghia inciso con canali estremamente stretti. Questi canali hanno solo alcune decine di nanometri di larghezza — migliaia di volte più sottili di un capello umano. Le molecole disciolte in un tampone fluiscono liberamente attraverso i canali invece di aderire a una superficie. Quando il chip è illuminato con luce visibile, sia le pareti del canale sia le molecole in transito diffondono la luce. Poiché il canale è molto più grande della molecola, la luce diffusa da entrambi interferisce in modo da amplificare notevolmente la firma ottica della molecola. Sottraendo immagini di un canale vuoto da immagini acquisite durante il passaggio di una molecola, i ricercatori ottengono una registrazione simile a un film (un cimografo) del suo transito attraverso il canale, che contiene informazioni sia sulla massa sia sulla velocità di diffusione.
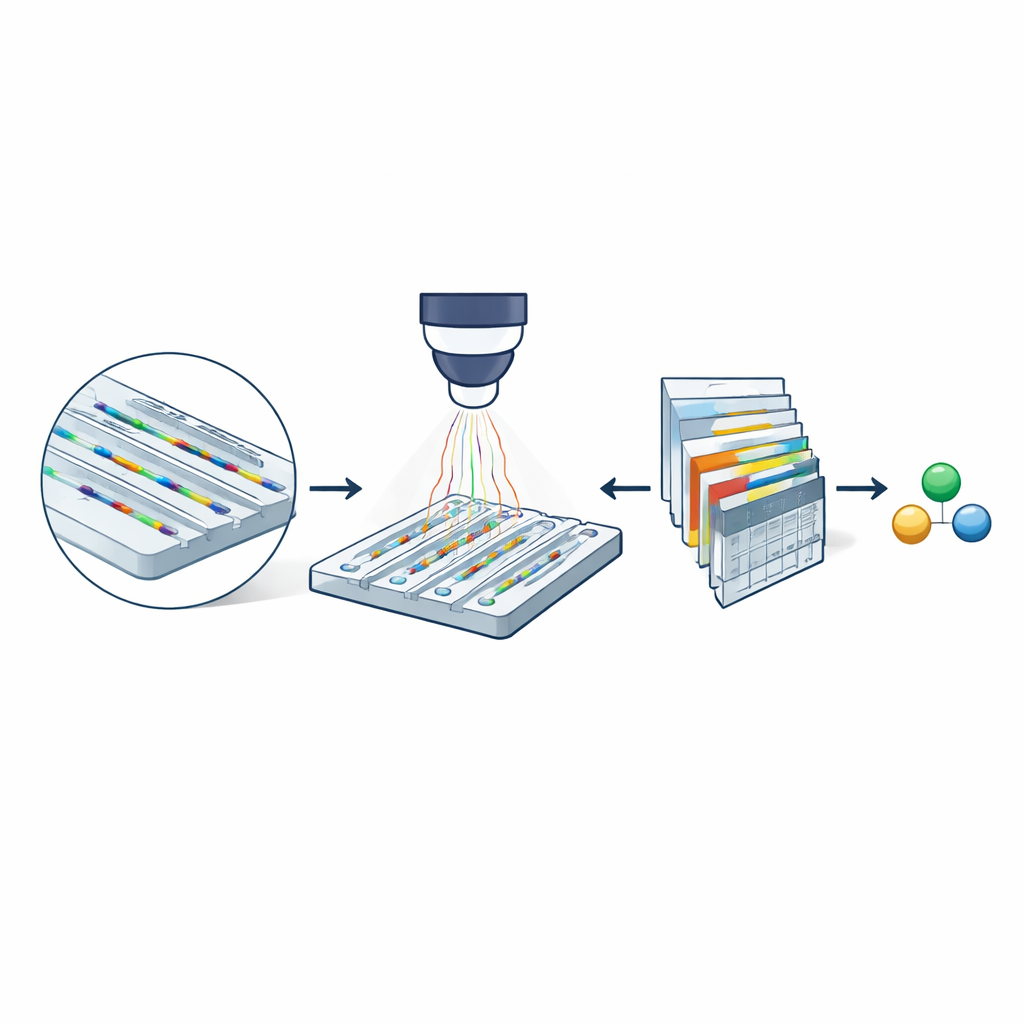
Perché i canali più stretti contano
Anche con questo potenziamento ottico, le versioni precedenti della tecnica riuscivano a caratterizzare solo molecole più pesanti di circa 60 kilodalton — tipiche proteine di grandi dimensioni — perché i segnali delle specie più piccole si perdeva nel rumore. Il team dimostra che ridurre la sezione trasversale dei nano-canali migliora drasticamente la sensibilità: il contrasto ottico di una molecola aumenta al diminuire dell’area del canale. Esperimenti che confrontano due dimensioni di canale con la proteina albumina sierica bovina mostrano che il suo percorso è chiaramente visibile nel canale più stretto ma quasi perduto in quello più largo. Questo semplice cambiamento geometrico suggerisce che, in linea di principio, biomolecole molto più piccole potrebbero essere rilevabili se i loro deboli segnali possono essere estratti in modo affidabile da sequenze di immagini rumorose.
Far interpretare film rumorosi all’IA
Per raggiungere questo regime, i ricercatori hanno sviluppato un modello di deep learning specializzato chiamato transformer visivo gerarchico. Invece di tentare di ricostruire la traccia esatta di ogni molecola pixel per pixel, il modello analizza il cimografo a più scale e produce due output: una mappa di probabilità che indica dove è probabile la presenza di una molecola in ogni punto di spazio e tempo, e una mappa di proprietà che codifica stime della massa molecolare e della dimensione idrodinamica. Pesando le stime delle proprietà con la mappa di probabilità, il modello può ignorare regioni costituite principalmente da rumore. L’addestramento si basa interamente su traiettorie simulate sovrapposte a rumore di fondo misurato sperimentalmente, permettendo al sistema di apprendere come dovrebbero apparire i segnali reali anche quando sono appena percettibili all’occhio.
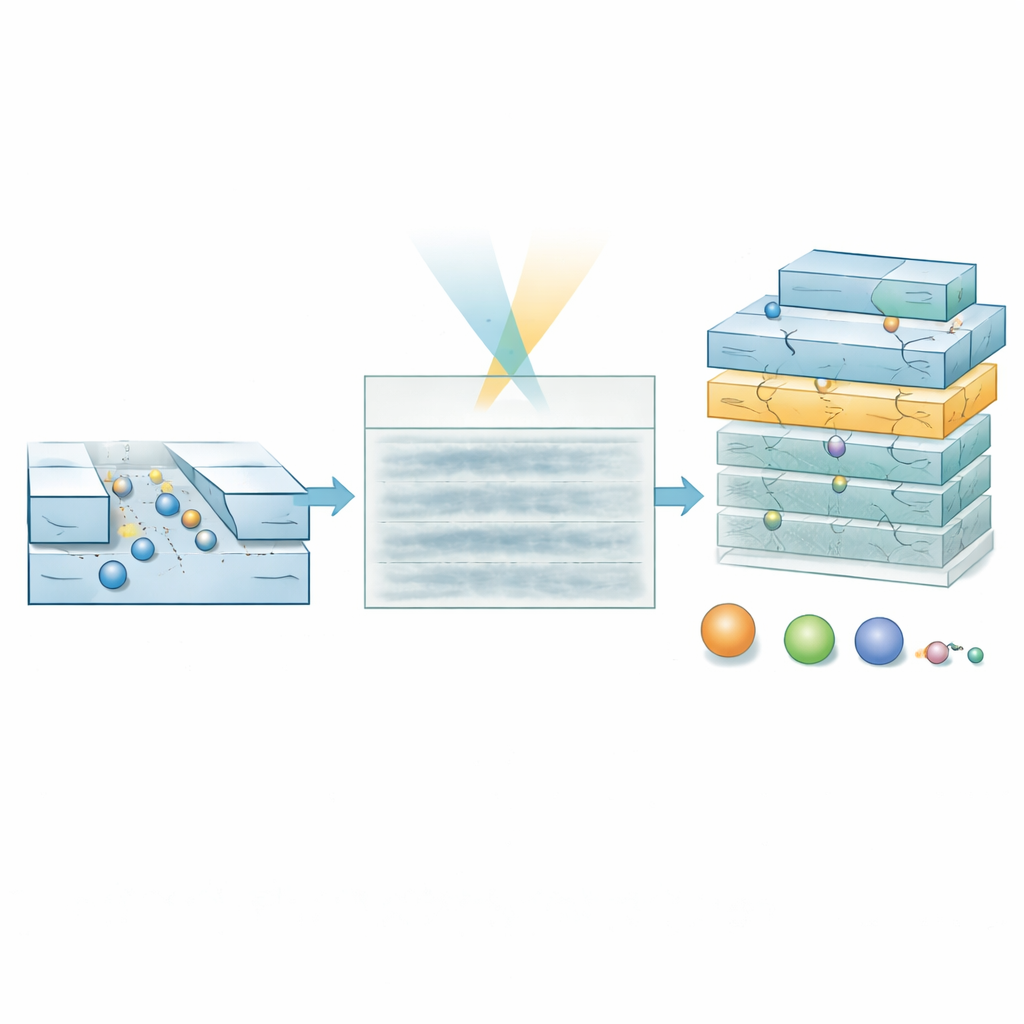
Test su DNA e molecole ormonali
Gli autori hanno prima validato l’approccio usando una “scala” di DNA standard, un mix di frammenti a doppio filamento di lunghezze e masse note, in canali relativamente larghi dove tutti i frammenti si trovano deliberatamente al di sotto del limite di rilevazione usuale. Nei film grezzi non si vedono tracce di DNA evidenti. Tuttavia il modello di IA produce mappe di probabilità che evidenziano correttamente dove passano le molecole e predice masse che corrispondono ai valori attesi una volta filtrati i dati a bassa confidenza. Il metodo riporta anche dimensioni effettive più piccole per i frammenti di DNA rigidi e a forma di asta rispetto alla loro lunghezza fisica completa, riflettendo come la forma influisca sulla diffusione. Il test più impegnativo ha utilizzato canali ultrasottili per studiare il peptide ormonale insulina, che pesa solo circa 5,8 kilodalton ed è grosso modo 1,5 nanometri di diametro. Anche qui i cimografi appaiono privi di caratteristiche, ma il modello estrae un gruppo stretto di valori di massa e dimensione in eccellente accordo con i dati della letteratura, nettamente separati dai controlli contenenti solo tampone.
Spingere contro i limiti
Per capire fino a che punto può spingersi questa strategia, il team ha confrontato la precisione del modello con il limite inferiore di Cramér–Rao, un vincolo statistico che definisce la migliore accuratezza possibile per qualsiasi stimatore non distorto dato il rumore nei dati. Usando grandi set di simulazioni, mostrano che man mano che il numero di fotogrammi che contribuiscono alla traiettoria di una molecola aumenta oltre circa diecimila, le stime di massa e dimensione del modello si avvicinano a questo ottimo teorico anche per una particella da sei kilodalton. Esperimenti sull’insulina a diverse concentrazioni riproducono la stessa tendenza: traiettorie efficaci più lunghe consentono misure più precise, limitate principalmente dal tempo in cui molecole piccolissime e a diffusione rapida rimangono in campo visivo. Gli autori propongono strategie future — come intrappolare delicatamente le molecole nei canali o riutilizzare i dati con bootstrapping — per aumentare ulteriormente il tempo di osservazione utile.
Cosa significa per biologia e medicina
In termini concreti, questo lavoro dimostra che è ora possibile pesare e misurare singolarmente alcune delle molecole più piccole e importanti dell’organismo, senza toccarle con etichette fluorescenti o farle aderire a una superficie. Unendo canali nanofabbricati a un’IA progettata per leggere film rumorosi di scattering della luce, il metodo riduce il limite di rilevazione di massa di questo approccio di microscopia senza marcatori di circa un ordine di grandezza. Si apre così la strada allo studio, a livello di singola molecola, di famiglie di piccole proteine segnale e ormoni peptidici — come citochine, chemochine e insulina — e alla caratterizzazione di nanoparticelle biologiche e vettori farmaceutici con sensibilità senza precedenti. Con il perfezionamento della tecnologia, potrebbe diventare uno strumento potente nella scoperta di farmaci, nella diagnostica e negli studi fondamentali su come le interazioni molecolari plasmano la vita alle scale più ridotte.
Citazione: K. Moberg, H., Yeroshenko, B., Fritzsche, J. et al. Label-free mass and size characterization of few-kDa biomolecules by hierarchical vision transformer augmented nanofluidic scattering microscopy. Nat Commun 17, 2533 (2026). https://doi.org/10.1038/s41467-026-70514-z
Parole chiave: microscopia a singola molecola senza marcatori, scattering nanofluidico, transformer visivo, piccole biomolecole, rilevazione dell’insulina